Валентность (химия) - Valence (chemistry)
В химии , то валентность или валентность из элемента является мерой его способности комбинирования с другими атомами , когда она образует химические соединения или молекулу .
Описание
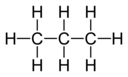
Комбинирующая способность или сродство атома данного элемента определяется количеством атомов водорода, с которыми он соединяется. В метане углерод имеет валентность 4; в аммиаке азот имеет валентность 3; в воде кислород имеет валентность 2; а в хлористом водороде хлор имеет валентность 1. Хлор, поскольку он имеет валентность, равную единице, может быть заменен на водород. Фосфор имеет валентность 5 в пентахлориде фосфора PCl 5 . Диаграммы валентности соединения представляют связь элементов с линиями, проведенными между двумя элементами, иногда называемыми связями, представляющими насыщенную валентность для каждого элемента. В двух таблицах ниже показаны некоторые примеры различных соединений, их диаграммы валентности и валентности для каждого элемента соединения.
| Сложный | H 2 Водород |
CH 4 Метан |
C 3 H 8 Пропан |
C 2 H 2 ацетилен |
|---|---|---|---|---|
| Диаграмма |
|

|
|
|
| Валентности |
| Сложный | NH 3 Аммиак |
NaCN цианистый натрий |
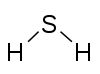
H 2 S сероводород |
H 2 SO 4 Серная кислота |
Cl 2 O 7 Гептоксид дихлора |
XeO 4 тетроксид ксенона |
|---|---|---|---|---|---|---|
| Диаграмма |

|
|
|

|

|

|
| Валентности |
Современные определения
Валентность определяется IUPAC как:
- Максимальное количество одновалентных атомов (первоначально атомов водорода или хлора), которые могут объединяться с атомом рассматриваемого элемента или с фрагментом, или для которых атом этого элемента может быть замещен.
Альтернативное современное описание:
- Число атомов водорода, которые могут соединяться с элементом в бинарном гидриде, или удвоенное число атомов кислорода, соединяющихся с элементом в его оксиде или оксидах.
Это определение отличается от определения IUPAC, поскольку можно сказать, что элемент имеет более одной валентности.
Очень похожее современное определение, данное в недавней статье, определяет валентность конкретного атома в молекуле как «количество электронов, которые атом использует для связывания», с двумя эквивалентными формулами для вычисления валентности:
- валентность = количество электронов в валентной оболочке свободного атома - количество несвязывающих электронов на атоме в молекуле ,
а также
- валентность = количество облигаций + формальный заряд .
Историческое развитие
Этимологии из слов валентности (множественное число валентностей ) и валентности (множественное число валентностей ) восходит к 1425 году , что означает «экстракт, препарат», от латинского Валентии «сила, способность», от ранее доблесть «стоит, значение», так и химические вещества значение, относящееся к «объединяющей силе элемента», записано с 1884 года в немецком Валенце .
Концепция валентности была разработана во второй половине 19 века и помогла успешно объяснить молекулярную структуру неорганических и органических соединений. Поиски основных причин валентности привели к современным теориям химической связи, включая кубический атом (1902 г.), структуры Льюиса (1916 г.), теорию валентных связей (1927 г.), молекулярные орбитали (1928 г.), теорию отталкивания электронных пар валентных оболочек. (1958) и все передовые методы квантовой химии .
В 1789 году Уильям Хиггинс опубликовал взгляды на то, что он называл комбинациями «предельных» частиц, которые предвосхитили концепцию валентных связей . Если, например, согласно Хиггинсу, сила между конечной частицей кислорода и конечной частицей азота составляла 6, тогда сила силы была бы разделена соответственно, и аналогично для других комбинаций конечных частиц (см. Иллюстрацию) .
Однако точное начало теории химических валентностей можно проследить до работы Эдварда Франкленда 1852 года , в которой он объединил старую радикальную теорию с мыслями о химическом сродстве, чтобы показать, что определенные элементы имеют тенденцию соединяться с другими элементами, чтобы образуют соединения, содержащие 3, т. е. в группах с 3 атомами (например, NO 3 , NH 3 , NI 3 и т. д.) или 5, т. е. в группах с 5 атомами (например, NO 5 , NH 4 O, PO 5 и др.), Эквиваленты присоединяемых элементов. По его словам, именно так их родство удовлетворяется лучше всего, и, следуя этим примерам и постулатам, он заявляет, насколько очевидно, что
(Здесь) преобладает тенденция или закон, и что, независимо от характера объединяющих атомов, объединяющая сила притягивающего элемента, если мне позволят термин, всегда удовлетворяется одним и тем же числом этих атомов. .
Эта «объединяющая сила» была впоследствии названа квантивалентностью или валентностью (и валентностью американские химики). В 1857 году Август Кекуле предложил фиксированные валентности для многих элементов, таких как 4 для углерода, и использовал их, чтобы предложить структурные формулы для многих органических молекул, которые до сих пор приняты.
Большинство химиков 19-го века определяли валентность элемента как количество его связей, не различая различных типов валентности или связи. Однако в 1893 году Альфред Вернер описал координационные комплексы переходных металлов, такие как [Co (NH 3 ) 6 ] Cl 3 , в которых он выделил основную и вспомогательную валентности (нем. «Hauptvalenz» и «Nebenvalenz»), соответствующие современным представлениям о степень окисления и координационное число соответственно.
Для элементов основной группы в 1904 году Ричард Абегг рассмотрел положительные и отрицательные валентности (максимальное и минимальное состояния окисления) и предложил правило Абегга, согласно которому их разница часто равна 8.
Электроны и валентность
Модель Резерфорда ядерного атома (1911) показала , что внешний вид атома занимают электроны , что свидетельствует , что электроны ответственны за взаимодействие атомов и образование химических связей. В 1916 году Гилберт Н. Льюис объяснил валентность и химическую связь в терминах тенденции атомов (основной группы) к достижению стабильного октета из 8 электронов валентной оболочки. Согласно Льюису, ковалентная связь приводит к октетам за счет разделения электронов, а ионная связь приводит к октетам за счет передачи электронов от одного атома к другому. Термин «ковалентность» приписывается Ирвингу Ленгмюру , который в 1919 году заявил, что «количество пар электронов, которые любой данный атом делит с соседними атомами, называется ковалентностью этого атома». Приставка co- означает «вместе», так что ковалентная связь означает, что атомы имеют общую валентность. После этого теперь чаще говорят о ковалентных связях, а не о валентности , которая вышла из употребления в высокоуровневых исследованиях из-за достижений теории химической связи, но все еще широко используется в элементарных исследованиях, где он обеспечивает эвристическое введение в предмет.
В 1930-х годах Линус Полинг предположил, что существуют также полярные ковалентные связи , которые занимают промежуточное положение между ковалентными и ионными, и что степень ионного характера зависит от разницы электроотрицательностей двух связанных атомов.
Полинг также рассматривал гипервалентные молекулы , в которых элементы основной группы имеют кажущуюся валентность больше, чем максимальное значение из 4, разрешенное правилом октетов. Например, в молекуле гексафторида серы (SF 6 ) Полинг считал, что сера образует 6 истинных двухэлектронных связей с использованием гибридных атомных орбиталей sp 3 d 2 , которые объединяют одну s, три p и две d орбитали. Однако недавно квантово-механические расчеты этой и подобных молекул показали, что роль d-орбиталей в связывании минимальна, и что молекула SF 6 должна быть описана как имеющая 6 полярных ковалентных (частично ионных) связей, образованных всего из четырех орбитали на сере (одна s и три p) в соответствии с правилом октетов вместе с шестью орбиталями на фторах. Подобные расчеты с молекулами переходных металлов показывают, что роль p-орбиталей незначительна, так что для описания связи достаточно одной s и пяти d-орбиталей на металле.
Общие валентности
Для элементов в основных группах в периодической таблице , валентность может варьироваться от 1 до 7.
| Группа | Валентность 1 | Валентность 2 | Валентность 3 | Валентность 4 | Валентность 5 | Валентность 6 | Валентность 7 | Валентность 8 | Типичные валентности |
|---|---|---|---|---|---|---|---|---|---|
| 1 (I) | NaCl | 1 | |||||||
| 2 (II) | MgCl 2 | 2 | |||||||
| 13 (III) |
BCl 3 AlCl 3 Al 2 O 3 |
3 | |||||||
| 14 (IV) | CO | CH 4 | 4 | ||||||
| 15 (В) | НЕТ |
NH 3 PH 3 As 2 O 3 |
НЕТ 2 |
N 2 O 5 PCl 5 |
3 и 5 | ||||
| 16 (VI) |
H 2 O H 2 S |
SO 2 | SO 3 | 2 и 6 | |||||
| 17 (VII) | HCl | HClO 2 | ClO 2 | HClO 3 | Cl 2 O 7 | 1 и 7 | |||
| 18 (VIII) | XeO 4 | 8 |
Многие элементы имеют общую валентность, связанную с их положением в периодической таблице, и в настоящее время это объясняется правилом октетов . Префиксы греческих / латинских цифр (моно- / уни-, ди- / би-, три- / тер- и т. Д.) Используются для описания ионов в зарядовых состояниях 1, 2, 3 и т. Д. Соответственно. Поливалентность или многовалентность относятся к видам , которые не ограничены определенным числом валентных связей . Однозарядные виды одновалентны (одновалентны). Например, катион Cs + является одновалентным или одновалентным катионом, тогда как катион Ca 2+ является двухвалентным катионом, а катион Fe 3+ является трехвалентным катионом. В отличие от Cs и Ca, Fe также может существовать в других зарядовых состояниях, особенно 2+ и 4+, и поэтому известен как многовалентный (поливалентный) ион. Переходные металлы и металлы справа обычно многовалентны, но не существует простой схемы, предсказывающей их валентность.
| Валентность | Более распространенное прилагательное ‡ | Менее распространенное синонимическое прилагательное ‡ § |
|---|---|---|
| 0-валентный | нулевой валент | не валентный |
| 1-валентный | одновалентный | однозначный |
| 2-валентный | двухвалентный | двухвалентный |
| 3-валентный | трехвалентный | трехвалентный |
| 4-валентный | четырехвалентный | четырехвалентный |
| 5-валентный | пятивалентный | пятивалентный /пятивалентный |
| 6-валентный | шестивалентный | сексуальный |
| 7-валентный | семивалентный | семилалентный |
| 8-валентный | октавалентный | - |
| 9-валентный | нелюбимый | - |
| 10-валентный | декавалентный | - |
| несколько / много / переменная | поливалентный | многовалентный |
| вместе | ковалентный | - |
| не вместе | нековалентный | - |
† Те же прилагательные также используются в медицине для обозначения валентности вакцины, с той небольшой разницей, что в последнем смысле квадри- более распространен, чем тетра- .
‡ Судя по количеству посещений в веб-поиске Google и поисковой системе Google Книг (по состоянию на 2017 г.).
§ Некоторые другие формы можно найти в больших англоязычных корпусах (например, * quintavalent, * quintivalent, * decivalent ), но они не являются общепринятыми формами в английском языке и поэтому не входят в основные словари.
Валентность в зависимости от степени окисления
Из-за двусмысленности термина валентность в настоящее время предпочтительны другие обозначения. Помимо системы степеней окисления (также называемых числами окисления ), используемой в номенклатуре запасов для координационных соединений , и лямбда-обозначений, используемых в номенклатуре неорганической химии ИЮПАК , степень окисления является более четким указанием электронного состояния атомов в молекула.
Степень окисления атома в молекуле дает количество валентных электронов, которые он получил или потерял. В отличие от числа валентности, степень окисления может быть положительной (для электроположительного атома) или отрицательной (для электроотрицательного атома).
Элементы с высокой степенью окисления могут иметь валентность выше четырех. Например, в перхлоратах хлор имеет семь валентных связей; рутений в степени окисления +8 в четырехокиси рутения имеет восемь валентных связей.
Примеры
| Сложный | Формула | Валентность | Состояние окисления |
|---|---|---|---|
| Хлористый водород | HCl | H = 1 Cl = 1 | H = +1 Cl = -1 |
| Хлорная кислота * | HClO 4 | H = 1 Cl = 7 O = 2 | H = +1 Cl = +7 O = −2 |
| Гидрид натрия | Неа | Na = 1 H = 1 | Na = +1 H = -1 |
| Закись железа ** | FeO | Fe = 2 O = 2 | Fe = +2 O = −2 |
| Оксид железа ** | Fe 2 O 3 | Fe = 3 O = 2 | Fe = +3 O = −2 |
* Одивалентный перхлорат-ион ( ClO-
4) имеет валентность 1.
** Оксид железа присутствует в кристаллической структуре , поэтому типичная молекула не может быть идентифицирована.
В закиси железа Fe имеет степень окисления II; в оксиде железа, степень окисления III.
| Сложный | Формула | Валентность | Состояние окисления |
|---|---|---|---|
| Хлор | Cl 2 | Cl = 1 | Cl = 0 |
| Пероксид водорода | Н 2 О 2 | Н = 1 О = 2 | H = +1 O = -1 |
| Ацетилен | С 2 Н 2 | С = 4 Н = 1 | С = -1 H = +1 |
| Хлорид ртути (I) | Hg 2 Cl 2 | Hg = 2 Cl = 1 | Hg = +1 Cl = -1 |
Валентности также могут отличаться от абсолютных значений степеней окисления из-за разной полярности связей. Например, в дихлорметане , CH 2 Cl 2 , углерод имеет валентность 4, но степень окисления 0.
Определение «Максимальное количество облигаций»
Франкланд придерживался мнения, что валентность (он использовал термин «атомарность») элемента - это единственное значение, которое соответствует максимальному наблюдаемому значению. Число неиспользуемых валентностей на атомах того, что сейчас называется p-блочными элементами, как правило, одинаково, и Франкланд предположил, что неиспользованные валентности насыщают друг друга. Например, азот имеет максимальную валентность 5, при образовании аммиака две валентности остаются несвязанными; сера имеет максимальную валентность 6, при образовании сероводорода четыре валентности не присоединяются.
Международный союз теоретической и прикладной химии (ИЮПАК) сделал несколько попыток , чтобы прийти к однозначному определению валентности. Текущая версия, принятая в 1994 году:
- Максимальное количество одновалентных атомов (первоначально атомов водорода или хлора), которые могут объединяться с атомом рассматриваемого элемента или с фрагментом, или для которых атом этого элемента может быть замещен.
Первоначально водород и хлор использовались в качестве примеров одновалентных атомов, поскольку по своей природе они образуют только одну одинарную связь. Водород имеет только один валентный электрон и может образовывать только одну связь с атомом, имеющим неполную внешнюю оболочку . Хлор имеет семь валентных электронов и может образовывать только одну связь с атомом, который отдает валентный электрон для завершения внешней оболочки хлора. Однако хлор также может иметь степень окисления от +1 до +7 и может образовывать более одной связи, отдавая валентные электроны .
Водород имеет только один валентный электрон, но он может образовывать связи более чем с одним атомом. В бифторид- ионе ( [HF
2]-
), например, он образует трехцентровую четырехэлектронную связь с двумя атомами фторида:
- [F – HF - ↔ F - H – F]
Другой пример - трехцентровая двухэлектронная связь в диборане (B 2 H 6 ).
Максимальные валентности элементов
Максимальные валентности элементов основаны на данных из списка степеней окисления элементов .
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Группа → | |||||||||||||||||||||
| ↓ Период | |||||||||||||||||||||
| 1 | 1 ЧАС |
2 Он |
|||||||||||||||||||
| 2 | 3 Ли |
4 Быть |
5 B |
6 C |
7 N |
8 О |
9 F |
10 Ne |
|||||||||||||
| 3 | 11 Na |
12 Mg |
13 Al |
14 Si |
15 п |
16 S |
17 Cl |
18 Ar |
|||||||||||||
| 4 | 19 K |
20 Ca |
21 год Sc |
22 Ti |
23 V |
24 Cr |
25 Mn |
26 Fe |
27 Co |
28 год Ni |
29 Cu |
30 Zn |
31 год Ga |
32 Ge |
33 В качестве |
34 Se |
35 год Br |
36 Kr |
|||
| 5 | 37 Руб. |
38 Sr |
39 Y |
40 Zr |
41 год Nb |
42 Пн |
43 год Tc |
44 год RU |
45 Rh |
46 Pd |
47 Ag |
48 CD |
49 В |
50 Sn |
51 Sb |
52 Te |
53 я |
54 Xe |
|||
| 6 | 55 CS |
56 Ба |
|
71 Лу |
72 Hf |
73 Та |
74 W |
75 Re |
76 Операционные системы |
77 Ir |
78 Pt |
79 Au |
80 Hg |
81 год Tl |
82 Pb |
83 Би |
84 По |
85 В |
86 Rn |
||
| 7 | 87 Пт |
88 Ра |
|
103 Lr |
104 Rf |
105 Db |
106 Sg |
107 Bh |
108 Hs |
109 Mt |
110 Ds |
111 Rg |
112 Cn |
113 Nh |
114 Fl |
115 Mc |
116 Ур. |
117 Ц |
118 Og |
||
|
|
57 год Ла |
58 Ce |
59 Pr |
60 Nd |
61 Вечера |
62 См |
63 ЕС |
64 Б-г |
65 Tb |
66 Dy |
67 Хо |
68 Э |
69 Тм |
70 Yb |
|||||||
|
|
89 Ac |
90 Чт |
91 Па |
92 U |
93 Np |
94 Пу |
95 Являюсь |
96 См |
97 Bk |
98 Cf |
99 Es |
100 FM |
101 Мкр |
102 Нет |
|||||||
| Максимальные валентности основаны на Списке степеней окисления элементов. | |||||||||||||||||||||
|
0 1 2 3 4 5 6 7 8 9 Неизвестный Цвет фона показывает максимальную валентность химического элемента. |
|||||||||||||||||||||

