Бор - Boron
 бор (β-ромбоэдрический)
| ||||||||||||||||
| Бор | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Произношение |
/ Б ɔːr ɒ н / ( БОР -он ) |
|||||||||||||||
| Аллотропы | α-, β-ромбоэдрические, β-тетрагональные (и другие ) | |||||||||||||||
| Появление | Черно-коричневый | |||||||||||||||
| Стандартный атомный вес A r, std (B) | [10.806 , 10.821 ] условный: 10,81 | |||||||||||||||
| Бор в периодической таблице | ||||||||||||||||
| ||||||||||||||||
| Атомный номер ( Z ) | 5 | |||||||||||||||
| Группа | группа 13 (группа бора) | |||||||||||||||
| Период | период 2 | |||||||||||||||
| Блокировать | p-блок | |||||||||||||||
| Электронная конфигурация | [ Он ] 2с 2 2п 1 | |||||||||||||||
| Электронов на оболочку | 2, 3 | |||||||||||||||
| Физические свойства | ||||||||||||||||
| Фаза на СТП | твердый | |||||||||||||||
| Температура плавления | 2349 К (2076 ° С, 3769 ° F) | |||||||||||||||
| Точка кипения | 4200 К (3927 ° C, 7101 ° F) | |||||||||||||||
| Плотность в жидком состоянии (при температуре плавления ) | 2,08 г / см 3 | |||||||||||||||
| Теплота плавления | 50,2 кДж / моль | |||||||||||||||
| Теплота испарения | 508 кДж / моль | |||||||||||||||
| Молярная теплоемкость | 11,087 Дж / (моль · К) | |||||||||||||||
Давление газа
| ||||||||||||||||
| Атомные свойства | ||||||||||||||||
| Состояния окисления | −5, −1, 0, +1, +2, +3 ( слабокислый оксид) | |||||||||||||||
| Электроотрицательность | Шкала Полинга: 2,04 | |||||||||||||||
| Энергии ионизации | ||||||||||||||||
| Радиус атома | эмпирический: 90 часов | |||||||||||||||
| Ковалентный радиус | 84 ± 15 часов | |||||||||||||||
| Радиус Ван-дер-Ваальса | 192 вечера | |||||||||||||||
| Спектральные линии бора | ||||||||||||||||
| Прочие свойства | ||||||||||||||||
| Естественное явление | изначальный | |||||||||||||||
| Кристальная структура | ромбоэдрическая | |||||||||||||||
| Скорость звука тонкого стержня | 16200 м / с (при 20 ° C) | |||||||||||||||
| Тепловое расширение | β-форма: 5–7 мкм / (м⋅K) (при 25 ° C) | |||||||||||||||
| Теплопроводность | 27,4 Вт / (м⋅K) | |||||||||||||||
| Удельное электрическое сопротивление | ~ 10 6 Ом⋅м (при 20 ° C) | |||||||||||||||
| Магнитный заказ | диамагнитный | |||||||||||||||
| Молярная магнитная восприимчивость | −6,7 × 10 −6 см 3 / моль | |||||||||||||||
| Твердость по шкале Мооса | ~ 9,5 | |||||||||||||||
| Количество CAS | 7440-42-8 | |||||||||||||||
| История | ||||||||||||||||
| Открытие | Жозеф Луи Гей-Люссак и Луи Жак Тенар (30 июня 1808 г.) | |||||||||||||||
| Первая изоляция | Хэмфри Дэви (9 июля 1808 г.) | |||||||||||||||
| Основные изотопы бора | ||||||||||||||||
| ||||||||||||||||
| В природных образцах содержание 10 B составляет 19,1–20,3%, остальное - 11 B. | ||||||||||||||||
Бор - химический элемент с символом B и атомным номером 5. В кристаллической форме это хрупкий, темный, блестящий металлоид ; в аморфном виде представляет собой порошок коричневого цвета. Как самый легкий элемент группы бора, он имеет три валентных электрона для образования ковалентных связей , в результате чего образуются многие соединения, такие как борная кислота , минеральная бура и сверхтвердый кристаллический карбид бора .
Бор полностью синтезируется расщеплением космических лучей и сверхновыми, а не звездным нуклеосинтезом , поэтому он является элементом с низким содержанием в Солнечной системе и в земной коре . Он составляет около 0,001 процента от веса земной коры. Бор концентрируется на Земле из-за растворимости в воде его наиболее распространенных природных соединений - боратных минералов . Их промышленно добывают в виде эвапоритов , таких как бура и кернит . Крупнейшие известные месторождения бора находятся в Турции , крупнейшем производителе минералов бора.
Элементарный бор - это металлоид, который в небольших количествах содержится в метеороидах, но химически несвязанный бор не встречается в естественных условиях на Земле. В промышленности очень чистый бор получается с трудом из-за загрязнения углеродом или другими элементами, которые трудно удалить. Существует несколько аллотропов бора : аморфный бор - коричневый порошок; кристаллический бор от серебристого до черного, чрезвычайно твердый (около 9,5 по шкале Мооса ) и плохой проводник при комнатной температуре. Основное применение элементарного бора - это борные нити, которые используются, как углеродные волокна, в некоторых высокопрочных материалах.
Бор в основном используется в химических соединениях. Около половины всего потребляемого в мире бора составляет добавка в стекловолокно для изоляционных и конструкционных материалов. Следующим по популярности является применение в полимерах и керамике в высокопрочных, легких конструкционных и жаропрочных материалах. Желательно, чтобы боросиликатное стекло обладало большей прочностью и термостойкостью, чем обычное натриево-известковое стекло. Бор в виде пербората натрия используется в качестве отбеливателя . Небольшое количество бора используется в качестве легирующей примеси в полупроводниках и в качестве промежуточных реагентов при синтезе тонкой органической химии . Несколько борсодержащих органических фармацевтических препаратов используются или изучаются. Природный бор состоит из двух стабильных изотопов, один из которых ( бор-10 ) имеет ряд применений в качестве улавливающего нейтроны агента.
Пересечение бора с биологией очень мало. Единого мнения о боре как о важном элементе для жизни млекопитающих нет. Бораты обладают низкой токсичностью для млекопитающих (подобно поваренной соли ), но более токсичны для членистоногих и иногда используются в качестве инсектицидов . Известны борсодержащие органические антибиотики. Хотя требуются только следы, бор является важным питательным веществом для растений.
История
Слово бор образовано от слова бура , минерала, из которого он был выделен, по аналогии с углеродом , на который бор похож по химическому составу.
Бура в минеральной форме (тогда известная как тинкал) впервые использовалась в качестве глазури в Китае примерно в 300 году нашей эры. Некоторая неочищенная бура распространилась на запад и, очевидно, была упомянута алхимиком Джабиром ибн Хайяном около 700 года нашей эры. Марко Поло вернул немного глазури в Италию в 13 веке. Георгий Агрикола примерно в 1600 году нашей эры сообщил об использовании буры в качестве флюса в металлургии . В 1777 году борная кислота была обнаружена в горячих источниках ( soffioni ) недалеко от Флоренции , Италия, после чего она стала известна как sal sedativum с явными медицинскими преимуществами. Минерал был назван сассолитом в честь Сассо Пизано в Италии. Сассо был основным источником европейской буры с 1827 по 1872 год, когда ее заменили американские источники. Соединения бора были сравнительно редко до конца 1800 - х годов , когда Фрэнсис Марион Смит «s Pacific Coast Бура Company первым популяризировал и произвел их в объеме при низкой стоимости.
Бор не был признан элементом, пока он не был изолирован сэром Хамфри Дэви , Жозефом Луи Гей-Люссаком и Луи Жаком Тенаром . В 1808 году Дэви заметил, что электрический ток, пропущенный через раствор боратов, вызывает образование коричневого осадка на одном из электродов. В своих последующих экспериментах он использовал калий для восстановления борной кислоты вместо электролиза . Он произвел достаточно бора, чтобы подтвердить новый элемент, и назвал этот элемент борацием . Гей-Люссак и Тенар использовали железо для восстановления борной кислоты при высоких температурах. Окисляя бор воздухом, они показали, что борная кислота является продуктом окисления бора. Йенс Якоб Берцелиус определил бор как элемент в 1824 году. Возможно, впервые чистый бор был получен американским химиком Иезекилем Вайнтраубом в 1909 году.
Приготовление элементарного бора в лаборатории
Самые ранние способы получения элементарного бора включали восстановление оксида бора такими металлами, как магний или алюминий . Однако продукт почти всегда загрязнен боридами этих металлов. Чистый бор может быть получен восстановлением летучих галогенидов бора водородом при высоких температурах. Сверхчистый бор для использования в полупроводниковой промышленности получают разложением диборана при высоких температурах, а затем очищают с помощью зонной плавки или процессов Чохральского .
Производство соединений бора не связано с образованием элементарного бора, но использует удобную доступность боратов.
Характеристики
Аллотропы
Бор похож на углерод по способности образовывать стабильные ковалентно связанные молекулярные сети. Даже номинально неупорядоченный ( аморфный ) бор содержит правильные икосаэдры бора, которые, однако, связаны друг с другом случайным образом без дальнего порядка . Кристаллический бор - это очень твердый материал черного цвета с температурой плавления выше 2000 ° C. Он образует четыре основных аллотропа : α-ромбоэдрический и β-ромбоэдрический (α-R и β-R), γ-орторомбический (γ) и β-тетрагональный (β-T). Все четыре фазы стабильны в условиях окружающей среды , и β-ромбоэдр является наиболее распространенным и стабильным. Также существует α-тетрагональная фаза (α-T), но ее очень трудно получить без значительного загрязнения. Большинство фаз основано на икосаэдрах B 12 , но γ-фаза может быть описана как расположение икосаэдров и пар атомов B 2 типа каменной соли . Его можно получить путем сжатия других фаз бора до 12–20 ГПа и нагрева до 1500–1800 ° C; он остается стабильным после сброса температуры и давления. Фаза β-T производится при аналогичных давлениях, но более высоких температурах 1800–2200 ° C. Фазы α-T и β-T могут сосуществовать в условиях окружающей среды, причем фаза β-T является более стабильной. Сжатие бора выше 160 ГПа дает фазу бора с пока неизвестной структурой, и эта фаза является сверхпроводником при температурах ниже 6–12 К. Боросферен ( фуллереноподобные молекулы B 40 ) и борофен (предложенная графеноподобная структура) были описан в 2014 году.
| Борная фаза | α-R | β-R | γ | β-Т |
|---|---|---|---|---|
| Симметрия | Ромбоэдрический | Ромбоэдрический | Орторомбический | Тетрагональный |
| Атомы / элементарная ячейка | 12 | ~ 105 | 28 год | |
| Плотность (г / см 3 ) | 2,46 | 2.35 | 2,52 | 2.36 |
| Твердость по Виккерсу (ГПа) | 42 | 45 | 50–58 | |
| Объемный модуль (ГПа) | 185 | 224 | 227 | |
| Ширина запрещенной зоны (эВ) | 2 | 1.6 | 2.1 |
Химия элемента
Элементарный бор встречается редко и плохо изучен, потому что чистый материал чрезвычайно сложно приготовить. Большинство исследований «бора» включают образцы, содержащие небольшое количество углерода. По химическому поведению бор больше напоминает кремний, чем алюминий . Кристаллический бор химически инертен и устойчив к воздействию кипящей фтористоводородной или соляной кислоты . В тонкоизмельченном состоянии он медленно разрушается горячей концентрированной перекисью водорода , горячей концентрированной азотной кислотой , горячей серной кислотой или горячей смесью серной и хромовой кислот .
Скорость окисления бора зависит от кристалличности, размера частиц, чистоты и температуры. Бор не реагирует с воздухом при комнатной температуре, но при более высоких температурах горит с образованием триоксида бора :
- 4 В + 3 О 2 → 2 В 2 О 3

Бор подвергается галогенированию с образованием тригалогенидов; Например,
- 2 Б + 3 Бр 2 → 2 ББр 3
На практике трихлорид обычно получают из оксида.
Атомная структура
Бор - самый легкий элемент, имеющий электрон на p-орбитали в основном состоянии. Но, в отличие от большинства других p-элементов , он редко подчиняется правилу октетов и обычно помещает только шесть электронов (на трех молекулярных орбиталях ) на свою валентную оболочку . Бор является прототипом группы бора ( группа 13 ИЮПАК ), хотя другие члены этой группы являются металлами и более типичными р-элементами (только алюминий в некоторой степени разделяет отвращение бора к правилу октетов).
Химические соединения

В наиболее известных соединениях бор имеет формальную степень окисления III. К ним относятся оксиды, сульфиды, нитриды и галогениды.
Тригалогениды имеют плоскую тригональную структуру. Эти соединения являются кислотами Льюиса в том смысле, что они легко образуют аддукты с донорами электронных пар, которые называются основаниями Льюиса . Например, фторид (F - ) и трифторид бора (BF 3 ) объединяются с образованием тетрафторборат- аниона, BF 4 - . Трифторид бора используется в нефтехимической промышленности в качестве катализатора. Галогениды реагируют с водой с образованием борной кислоты .
Бор встречается в природе на Земле почти полностью в виде различных оксидов B (III), часто связанных с другими элементами. Более ста боратных минералов содержат бор в степени окисления +3. Эти минералы в чем-то напоминают силикаты, хотя бор часто встречается не только в тетраэдрической координации с кислородом, но и в тригональной планарной конфигурации. В отличие от силикатов борсодержащие минералы никогда не содержат бор с координационным числом больше четырех. Типичный мотив представлен анионами тетрабората обычного минерала буры , показанных слева. Формальный отрицательный заряд тетраэдрического боратного центра уравновешивается катионами металлов в минералах, такими как натрий (Na + ) в буре. Группа борат-силикатов турмалина также является очень важной группой борсодержащих минералов, и также известно, что в естественных условиях существует ряд боросиликатов.
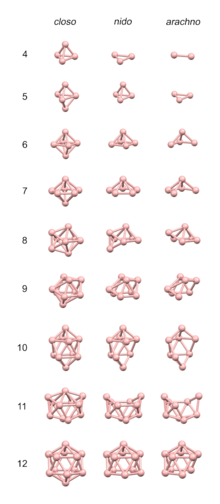
Бораны - это химические соединения бора и водорода с общей формулой B x H y . Эти соединения не встречаются в природе. Многие из боранов легко окисляются при контакте с воздухом, некоторые - бурно. Родительский член BH 3 называется бораном, но он известен только в газообразном состоянии и димеризуется с образованием диборана B 2 H 6 . Все более крупные бораны состоят из многогранных кластеров бора, некоторые из которых существуют в виде изомеров. Например, изомеры B 20 H 26 основаны на слиянии двух 10-атомных кластеров.
Наиболее важными боранами являются диборан B 2 H 6 и два продукта его пиролиза, пентаборан B 5 H 9 и декаборан B 10 H 14 . Известно большое количество анионных гидридов бора, например [B 12 H 12 ] 2- .
Формальная степень окисления борана положительна и основана на предположении, что водород считается как -1, как в гидридах активных металлов. Тогда средняя степень окисления бора - это просто отношение водорода к бору в молекуле. Например, в диборане B 2 H 6 , степень окисления бора +3, но в Декаборане В 10 Н 14 , это 7 / 5 или 1,4. В этих соединениях степень окисления бора часто не является целым числом.
В нитриды бора отличаются разнообразием структур , которые они принимают. Они имеют структуры, аналогичные различным аллотропам углерода , включая графит, алмаз и нанотрубки. В алмазоподобной структуре, называемой кубическим нитридом бора (торговое название боразон ), атомы бора существуют в тетраэдрической структуре атомов углерода в алмазе, но каждую четвертую связь BN можно рассматривать как координационную ковалентную связь , в которой пожертвованы два электрона. атомом азота, который действует как основание Льюиса по отношению к льюисовскому кислотному центру бора (III). Кубический нитрид бора, помимо прочего, используется в качестве абразива, поскольку он имеет твердость, сравнимую с алмазом (эти два вещества могут оставлять царапины друг на друге). В составном аналоге графита BN, гексагональном нитриде бора (h-BN), положительно заряженные атомы бора и отрицательно заряженные атомы азота в каждой плоскости лежат рядом с противоположно заряженным атомом в следующей плоскости. Следовательно, графит и h-BN имеют очень разные свойства, хотя оба являются смазочными материалами, поскольку эти плоскости легко скользят друг мимо друга. Однако h-BN является относительно плохим проводником электричества и тепла в плоских направлениях.
Борорганическая химия
Известно большое количество борорганических соединений, многие из которых используются в органическом синтезе . Многие из них производятся гидроборированием , в котором используется диборан , B 2 H 6 , простой боран . Боровоорганические (III) соединения обычно являются тетраэдрическими или тригонально плоскими, например, тетрафенилборат , [B (C 6 H 5 ) 4 ] - против трифенилборана , B (C 6 H 5 ) 3 . Однако несколько атомов бора, взаимодействуя друг с другом, имеют тенденцию образовывать новые додекаэдрические (12-сторонние) и икосаэдрические (20-сторонние) структуры, полностью состоящие из атомов бора или с различным количеством гетероатомов углерода.
Борорганические химические вещества использовались в самых разных областях, от карбида бора (см. Ниже), сложной очень твердой керамики, состоящей из бороуглеродных кластерных анионов и катионов, до карборанов , соединений углеродно-борной кластерной химии, которые могут быть галогенированы с образованием реактивных структур, включая карборановая кислота , суперкислота . В качестве одного примера, карбораны образуют полезные молекулярные фрагменты, которые добавляют значительные количества бора к другим биохимическим веществам, чтобы синтезировать борсодержащие соединения для борной нейтронно-захватной терапии рака.
Соединения B (I) и B (II)
Как и ожидалось по его гидридным кластерам , бор образует множество стабильных соединений с формальной степенью окисления менее трех. B 2 F 4 и B 4 Cl 4 хорошо охарактеризованы.
Бинарные соединения металла и бора, бориды металлов, содержат бор в отрицательной степени окисления. Примером является диборид магния (MgB 2 ). Каждый атом бора имеет формальный заряд -1, а магнию соответствует формальный заряд +2. В этом материале центры бора тригонально плоские с дополнительной двойной связью для каждого бора, образуя листы, похожие на углерод в графите . Однако, в отличие от гексагонального нитрида бора, у которого отсутствуют электроны в плоскости ковалентных атомов, делокализованные электроны в дибориде магния позволяют ему проводить электричество подобно изоэлектронному графиту. В 2001 году этот материал был признан высокотемпературным сверхпроводником . Это сверхпроводник, который находится в стадии активной разработки. В результате проекта ЦЕРНа по производству кабелей MgB 2 были созданы сверхпроводящие испытательные кабели, способные выдерживать ток 20 000 ампер для применения в распределительных устройствах с чрезвычайно высоким током, таких как предполагаемая версия большого адронного коллайдера с высокой светосилой .
Некоторые другие бориды металлов находят специализированное применение в качестве твердых материалов для режущих инструментов. Часто бор в боридах имеет фракционные степени окисления, такие как -1/3 в гексабориде кальция (CaB 6 ).
Со структурной точки зрения наиболее отличительными химическими соединениями бора являются гидриды. В эту серию включены кластерные соединения додекаборат ( B
12ЧАС2-
12), декаборан (B 10 H 14 ) и карбораны, такие как C 2 B 10 H 12 . Обычно такие соединения содержат бор с координационными числами больше четырех.
Изотопы
Бор имеет два природных и стабильных изотопа : 11 B (80,1%) и 10 B (19,9%). Разница масс приводит к широкому диапазону значений δ 11 B, которые определяются как дробная разница между 11 B и 10 B и традиционно выражаются в частях на тысячу в природных водах в диапазоне от -16 до +59. Известно 13 изотопов бора, самый короткоживущий изотоп - 7 B, который распадается в результате испускания протонов и альфа-распада . Его период полураспада составляет 3,5 × 10 −22 с. Изотопное фракционирование бора регулируется реакциями обмена частиц бора B (OH) 3 и [B (OH) 4 ] - . Изотопы бора также фракционировали в ходе кристаллизации минералов, в течение H 2 фазовых превращений O в гидротермальных системах, а также в ходе гидротермального изменения в породе . Последний эффект приводит к преимущественному удалению иона [ 10 B (OH) 4 ] - на глины. В результате получаются растворы, обогащенные 11 B (OH) 3, и поэтому они могут быть ответственны за большое обогащение 11 B в морской воде по сравнению как с океанической корой, так и с континентальной корой; это различие может действовать как изотопная сигнатура .
Экзотический 17 B имеет ядерный гало , т.е. его радиус значительно больше, чем предсказывается моделью жидкой капли .
10 В изотоп полезно для захвата тепловых нейтронов (см нейтронов сечение # Типичные сечений ). В атомной промышленности природный бор обогащается почти до 10 B. Менее ценный побочный продукт, обедненный бор, имеет почти чистый 11 B.
Коммерческое обогащение изотопов
Из-за своего высокого нейтронного сечения бор-10 часто используется для контроля деления в ядерных реакторах в качестве нейтронно-улавливающего вещества. Было разработано несколько промышленных процессов обогащения; однако используются только фракционная вакуумная перегонка диметилового эфира аддукта трифторида бора (DME-BF 3 ) и колоночная хроматография боратов.
Обогащенный бор (бор-10)
Обогащенный бор или 10 B используется как для защиты от излучения, так и является основным нуклидом, используемым в нейтронно-захватной терапии рака . В последнем случае («борная нейтронно-захватная терапия» или BNCT) соединение, содержащее 10 B, включается в фармацевтический препарат, который избирательно поглощается злокачественной опухолью и тканями рядом с ней. Затем пациента лечат пучком нейтронов низкой энергии при относительно низкой дозе нейтронного излучения. Нейтроны, однако, вызывают энергетическую и короткодействующую вторичную альфа-частицу и тяжелое ионное излучение лития-7, которые являются продуктами ядерной реакции бор + нейтрон , и это ионное излучение дополнительно бомбардирует опухоль, особенно изнутри опухолевых клеток.
В ядерных реакторах 10 B используется для контроля реактивности и в системах аварийного останова . Он может выполнять функцию боросиликатных регулирующих стержней или борной кислоты . В герметичных реакторах с водой , 10 В борной кислоте добавляют в теплоноситель реактора , когда установка закрыта для дозаправки. Затем его медленно отфильтровывают в течение многих месяцев, поскольку делящийся материал израсходован и топливо становится менее реактивным.
В будущих пилотируемых межпланетных космических кораблях 10 B теоретически будет играть роль конструкционного материала (например, борных волокон или материала нанотрубок BN ), который также будет играть особую роль в радиационной защите. Одна из трудностей при работе с космическими лучами , которые в основном представляют собой протоны высоких энергий, заключается в том, что некоторое вторичное излучение от взаимодействия космических лучей и материалов космического корабля представляет собой нейтроны отщепления высокой энергии . Такие нейтроны могут замедляться материалами с высоким содержанием легких элементов, такими как полиэтилен , но замедленные нейтроны продолжают представлять радиационную опасность, если они активно не поглощаются защитой. Среди легких элементов, поглощающих тепловые нейтроны, 6 Li и 10 B являются потенциальными конструкционными материалами космического корабля, которые служат как для механического усиления, так и для защиты от радиации.
Обедненный бор (бор-11)
Радиационно-стойкие полупроводники
Космическое излучение будет производить вторичные нейтроны, если попадет в конструкцию космического корабля. Эти нейтроны будут захвачены в 10 B, если они присутствуют в полупроводниках космического корабля , производя гамма-излучение , альфа-частицу и ион лития . Эти результирующие продукты распада могут затем облучать близлежащие полупроводниковые «чипы», вызывая потерю данных (переключение битов или нарушение единичного события ). В конструкции радиационно-стойких полупроводников одной из мер противодействия является использование обедненного бора , который значительно обогащен 11 B и почти не содержит 10 B. Это полезно, поскольку 11 B в значительной степени невосприимчив к радиационному повреждению. Обедненный бор - это побочный продукт ядерной промышленности .
Протонно-борный синтез
11 Б также является кандидат в качестве топлива для безнейтронных слияний . При ударе протона с энергией около 500 кэВ он производит три альфа-частицы и энергию 8,7 МэВ. Большинство других термоядерных реакций с участием водорода и гелия производят проникающее нейтронное излучение, которое ослабляет конструкции реактора и вызывает длительную радиоактивность, тем самым подвергая опасности обслуживающий персонал. Однако альфа-частицы от синтеза 11 B могут быть превращены непосредственно в электроэнергию, и все излучение прекращается, как только реактор выключается.
ЯМР спектроскопия
И 10 B, и 11 B обладают ядерным спином . Ядерный спин 10 B равен 3, а спин 11 B равен3/2. Следовательно, эти изотопы используются в спектроскопии ядерного магнитного резонанса ; и спектрометры, специально приспособленные для обнаружения ядер бора-11, имеются в продаже. В 10 В и 11 ядер B также вызывают расщепление в резонансов присоединенных ядер.
Вхождение
Бор редко встречается во Вселенной и Солнечной системе из-за образования следов в результате Большого взрыва и в звездах. В незначительных количествах он образуется в процессе нуклеосинтеза расщеплением космических лучей и может быть обнаружен в несвязанном виде в космической пыли и материалах метеороидов .
В среде Земли с высоким содержанием кислорода бор всегда полностью окислен до бората. Бор не появляется на Земле в элементарной форме. В лунном реголите обнаружены очень маленькие следы элементарного бора.
Хотя бор - относительно редкий элемент в земной коре, составляющий всего 0,001% от массы земной коры, он может быть сильно сконцентрирован под действием воды, в которой растворимы многие бораты. Он содержится в естественных соединениях, таких как бура и борная кислота (иногда обнаруживается в водах вулканических источников). Известно около сотни боратных минералов .
5 сентября 2017 года ученые сообщили, что марсоход Curiosity обнаружил бор, важный ингредиент для жизни на Земле , на планете Марс . Такое открытие, наряду с предыдущими открытиями того, что вода могла присутствовать на древнем Марсе, еще раз подтверждает возможную раннюю обитаемость кратера Гейла на Марсе.
Производство
Экономически важными источниками бора являются минералы колеманит , разорит ( кернит ), улексит и тинкал . Вместе они составляют 90% добываемой борсодержащей руды. Крупнейшие известные месторождения буры в мире, многие из которых еще не освоены, находятся в Центральной и Западной Турции , включая провинции Эскишехир , Кютахья и Балыкесир . Мировые подтвержденные запасы полезных ископаемых, содержащих бор, превышающие один миллиард метрических тонн, при годовой добыче около четырех миллионов тонн.
Турция и США являются крупнейшими производителями борной продукции. Турция обеспечивает около половины мирового годового спроса через Eti Mine Works ( турецкий : Eti Maden İşletmeleri ), турецкую государственную горнодобывающую и химическую компанию, специализирующуюся на продуктах из бора. Он имеет государственную монополию на добычу боратных минералов в Турции, которая владеет 72% известных в мире месторождений. В 2012 году он занимал 47% на долю производства глобальных минералов бората, впереди своего главного конкурента, Rio Tinto Group .
Почти четверть (23%) мирового производства бора приходится на единственный рудник Rio Tinto Borax Mine (также известный как борный / 35.04290194°N 117.67928111°W рудник Borax в США) 35 ° 2′34,447 ″ с.ш., 117 ° 40′45,412 ″ з.д. недалеко от Бора , Калифорния .
Тенденция рынка
Средняя стоимость кристаллического бора составляет 5 долларов за г. Свободный бор в основном используется при изготовлении борных волокон, где он осаждается путем химического осаждения из паровой фазы на вольфрамовый сердечник (см. Ниже). Волокна бора используются в легких композитных материалах, таких как высокопрочные ленты. Это использование составляет очень небольшую долю от общего использования бора. Бор вводится в полупроводники в виде соединений бора путем ионной имплантации.
Расчетное глобальное потребление бора (почти полностью в виде соединений бора) составило около 4 миллионов тонн B 2 O 3 в 2012 году. Мощности по добыче и переработке бора считаются достаточными для удовлетворения ожидаемых уровней роста в течение следующего десятилетия.
Форма потребления бора за последние годы изменилась. Использование таких руд, как колеманит , сократилось из-за опасений по поводу содержания мышьяка . Потребители перешли на использование очищенных боратов и борной кислоты с более низким содержанием загрязняющих веществ.
Растущий спрос на борную кислоту побудил ряд производителей инвестировать в дополнительные мощности. Турецкая государственная компания Eti Mine Works открыла новый завод по производству борной кислоты производственной мощностью 100 000 тонн в год на Emet в 2003 году. Группа компаний Rio Tinto увеличила мощность своего завода по производству бора с 260 000 тонн в год в 2003 году до 310 000 тонн в год. Май 2005 года, с планами по увеличению этого объема до 366 000 тонн в год в 2006 году. Китайские производители бора не могут удовлетворить быстро растущий спрос на высококачественные бораты. Это привело к увеличению импорта тетрабората натрия ( буры ) в сто раз в период с 2000 по 2005 год, а импорт борной кислоты увеличивался на 28% в год за тот же период.
Рост мирового спроса был обусловлен высокими темпами роста производства стекловолокна , стекловолокна и боросиликатной стеклянной посуды. Быстрый рост производства армирующего борсодержащего стекловолокна в Азии остановил развитие безборного армирующего стекловолокна в Европе и США. Недавний рост цен на энергоносители может привести к более широкому использованию стекловолокна изоляционного качества с последующим ростом потребления бора. Roskill Consulting Group прогнозирует, что мировой спрос на бор будет расти на 3,4% в год и достигнет 21 миллиона тонн к 2010 году. Самый высокий рост спроса ожидается в Азии, где спрос может расти в среднем на 5,7% в год.
Приложения
Практически вся борная руда, добываемая на Земле, предназначена для переработки в борную кислоту и пентагидрат тетрабората натрия . В США 70% бора используется для производства стекла и керамики. Основное глобальное промышленное использование соединений бора (около 46% конечного использования) связано с производством стекловолокна для борсодержащих изоляционных и конструкционных стекловолокон , особенно в Азии. Бор добавляется в стекло в виде пентагидрата буры или оксида бора, чтобы влиять на прочность или флюсующие качества стекловолокна. Еще 10% мирового производства бора приходится на боросиликатное стекло, используемое в высокопрочной стеклянной посуде. Около 15% всего бора используется в борной керамике, в том числе в сверхтвердых материалах, обсуждаемых ниже. На сельское хозяйство приходится 11% мирового производства бора, а на отбеливатели и моющие средства - около 6%.
Элементное борное волокно
Волокна из бора (борные нити) - это высокопрочные и легкие материалы, которые используются в основном в современных аэрокосмических конструкциях в качестве компонента композиционных материалов , а также в потребительских и спортивных товарах ограниченного производства, таких как клюшки для гольфа и удочки . Волокна могут быть получены путем химического осаждения бора из паровой фазы на вольфрамовую нить.
Борные волокна и суб-миллиметрового размер кристаллических бора пружина , производимый лазер -поддерживаемых химического осаждения из паровой фазы . Трансляция сфокусированного лазерного луча позволяет изготавливать даже сложные спиральные конструкции. Такие конструкции обладают хорошими механическими свойствами ( модуль упругости 450 ГПа, деформация разрушения 3,7%, напряжение разрушения 17 ГПа) и могут применяться в качестве армирования керамики или в микромеханических системах .
Борированное стекловолокно
Стекловолокно - это армированный волокном полимер, сделанный из пластика, армированного стекловолокном , обычно тканный в мат. Стекловолокно, используемое в материале, изготовлено из различных типов стекла в зависимости от использования стекловолокна. Все эти стекла содержат кремнезем или силикат с различным количеством оксидов кальция, магния и иногда бора. Бор присутствует в виде боросиликата, буры или оксида бора и добавляется для увеличения прочности стекла или в качестве флюса для снижения температуры плавления диоксида кремния , который слишком высок, чтобы его можно было легко обрабатывать в чистом виде. сделать стекловолокно.
Стекло с высоким содержанием бора, используемое в стекловолокне, - это стекло E (названное от «электрического» использования, но в настоящее время наиболее распространенное стекловолокно для общего использования). Е-стекло - это алюмоборосиликатное стекло с содержанием оксидов щелочных металлов менее 1% по весу, которое в основном используется для изготовления стеклопластиков. Другие распространенные стекла с высоким содержанием бора включают C-стекло, щелочно-известковое стекло с высоким содержанием оксида бора, используемое для стеклянных штапельных волокон и изоляции, и D-стекло, боросиликатное стекло , названное из-за его низкой диэлектрической проницаемости).
Не все стекловолокна содержат бор, но в глобальном масштабе большая часть используемых стекловолокон действительно содержит его. Из-за повсеместного использования стекловолокна в строительстве и изоляции борсодержащие стекловолокна потребляют половину мирового производства бора и являются крупнейшим коммерческим рынком бора.
Боросиликатное стекло
Боросиликатное стекло , которое обычно состоит из 12–15% B 2 O 3 , 80% SiO 2 и 2% Al 2 O 3 , имеет низкий коэффициент теплового расширения , что придает ему хорошую стойкость к тепловому удару . Duran от Schott AG и Pyrex, зарегистрированный под торговой маркой Owens-Corning, являются двумя основными торговыми марками этого стекла, которое используется как в лабораторной посуде, так и в потребительской посуде и формах для выпечки , главным образом из-за этого сопротивления.
Керамика из карбида бора
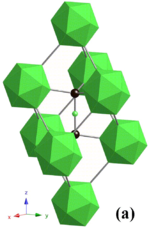
Некоторые соединения бора известны своей чрезвычайной твердостью и вязкостью. Карбид бора - это керамический материал, который получают разложением B 2 O 3 углеродом в электрической печи:
- 2 В 2 О 3 + 7 С → В 4 С + 6 СО
Структура карбида бора составляет лишь приблизительно B 4 C, и это показывает явное обеднение углерода из этого предложенного стехиометрического соотношения. Это связано с его очень сложной структурой. Вещество можно увидеть с помощью эмпирической формулы B 12 C 3 (т. Е. С додекаэдрами B 12, являющимися мотивом), но с меньшим количеством углерода, поскольку предлагаемые звенья C 3 заменены цепями CBC, а некоторые меньшие (B 6 ) октаэдры являются также присутствуют (см. статью о карбиде бора для структурного анализа). Повторяющийся полимер плюс полукристаллическая структура карбида бора придает ему большую структурную прочность на вес. Он используется в танковой броне , бронежилетах и многих других конструкциях.
Способность карбида бора поглощать нейтроны без образования долгоживущих радионуклидов (особенно при добавлении дополнительного бора-10) делает этот материал привлекательным в качестве поглотителя нейтронного излучения, возникающего на атомных электростанциях . Карбид бора применяется в ядерной области, включая экранирование, регулирующие стержни и запорные гранулы. В регулирующих стержнях карбид бора часто измельчается в порошок, чтобы увеличить площадь его поверхности.
Высокотвердые и абразивные составы
| Материал | Алмаз | кубический-BC 2 N | кубический-BC 5 | кубический-БН | В 4 С | ReB 2 |
|---|---|---|---|---|---|---|
| Твердость по Виккерсу (ГПа) | 115 | 76 | 71 | 62 | 38 | 22 |
| Вязкость разрушения (МПа м 1⁄2 ) | 5,3 | 4.5 | 9,5 | 6,8 | 3.5 |
Порошки карбида бора и кубического нитрида бора широко используются в качестве абразивов. Нитрид бора - это материал, изоэлектронный углероду . Подобно углероду, он имеет как гексагональную (мягкий графитоподобный h-BN), так и кубическую (твердый, алмазоподобный c-BN) формы. h-BN используется как высокотемпературный компонент и смазка. c-BN, также известный под коммерческим названием боразон , является превосходным абразивом. Его твердость лишь немного меньше, но его химическая стабильность выше, чем у алмаза. Гетеродиалмаз (также называемый BCN) - еще одно алмазоподобное соединение бора.
Металлургия
Бор добавляется к борсодержащим сталям на уровне нескольких частей на миллион для повышения прокаливаемости. Более высокие проценты добавляются в стали, используемые в ядерной промышленности, из-за способности бора поглощать нейтроны.
Бор может также повысить твердость поверхности сталей и сплавов за счет борирования . Кроме того, бориды металлов используются для покрытия инструментов путем химического осаждения из паровой фазы или физического осаждения из паровой фазы . Имплантация ионов бора в металлы и сплавы посредством ионной имплантации или ионно-лучевого осаждения приводит к впечатляющему увеличению поверхностного сопротивления и микротвердости. С той же целью успешно применялось лазерное легирование. Эти бориды являются альтернативой инструментам с алмазным покрытием, и их (обработанные) поверхности имеют свойства, аналогичные свойствам массивного борида.
Например, диборид рения можно производить при атмосферном давлении, но он довольно дорог из-за рения. Твердость ReB 2 проявляет значительную анизотропию из-за его гексагональной слоистой структуры. Его величина сравнима с таковой из карбида вольфрама , карбида кремния , диборида титана или диборида циркони . Точно так же композиты AlMgB 14 + TiB 2 обладают высокой твердостью и износостойкостью и используются либо в объемном виде, либо в качестве покрытий для компонентов, подверженных высоким температурам и нагрузкам от износа.
Составы моющих средств и отбеливатели
Borax используется в различных бытовых средствах для стирки и чистки, включая средство для стирки « 20 Mule Team Borax » и порошковое мыло для рук « Boraxo ». Он также присутствует в некоторых формулах для отбеливания зубов .
Перборат натрия служит источником активного кислорода во многих моющих средствах , средствах для стирки , чистящих средствах и отбеливателях для стирки . Однако, несмотря на свое название, отбеливатель для стирки «Borateem» больше не содержит соединений бора, а в качестве отбеливающего агента используется перкарбонат натрия .
Инсектициды
Борная кислота используется как инсектицид, особенно против муравьев, блох и тараканов.
Полупроводники
Бор - полезная легирующая добавка для таких полупроводников, как кремний , германий и карбид кремния . Имея на один валентный электрон меньше, чем основной атом, он дает дырку, что приводит к проводимости p-типа . Традиционный метод введения бора в полупроводники - его атомная диффузия при высоких температурах. В этом процессе используются твердые (B 2 O 3 ), жидкие (BBr 3 ) или газообразные источники бора (B 2 H 6 или BF 3 ). Однако после 1970-х годов его в основном заменили ионной имплантацией , которая в основном полагается на BF 3 в качестве источника бора. Газообразный трихлорид бора также является важным химическим веществом в полупроводниковой промышленности, однако не для легирования, а, скорее, для плазменного травления металлов и их оксидов. Триэтилборан также вводят в реакторы осаждения из паровой фазы в качестве источника бора. Примеры являются плазменным осаждением из борсодержащих твердых углеродных пленок, пленок нитрида кремния нитрида бора-, а также для легирования из алмазной пленки с бором.
Магниты
Бор входит в состав неодимовых магнитов (Nd 2 Fe 14 B), которые являются одними из самых сильных типов постоянных магнитов. Эти магниты используются в различных электромеханических и электронных устройствах, таких как системы медицинской визуализации с помощью магнитно-резонансной томографии (МРТ), в компактных и относительно небольших двигателях и исполнительных механизмах . Например, компьютерные жесткие диски (жесткие диски), CD (компакт-диски) и DVD (универсальные цифровые диски) проигрыватели полагаются на двигатели с неодимовыми магнитами, обеспечивающие высокую мощность вращения в удивительно компактном корпусе. В мобильных телефонах магниты Neo создают магнитное поле, которое позволяет крошечным динамикам передавать значительную мощность звука.
Защита и поглотитель нейтронов в ядерных реакторах
Экранирование бором используется в качестве средства управления ядерными реакторами , благодаря его высокому поперечному сечению для захвата нейтронов.
В реакторах с водой под давлением переменная концентрация бороновой кислоты в охлаждающей воде используется в качестве нейтронного яда для компенсации переменной реакционной способности топлива. Когда вставляются новые стержни, концентрация бороновой кислоты максимальна и снижается в течение срока службы.
Другое немедицинское использование
- Из-за характерного зеленого пламени аморфный бор используется в пиротехнических факелах .
- Клеи на основе крахмала и казеина содержат декагидрат тетрабората натрия (Na 2 B 4 O 7 · 10 H 2 O).
- Некоторые антикоррозионные системы содержат бура.
- Бораты натрия используются в качестве флюса для пайки серебра и золота и с хлоридом аммония для сварки черных металлов. Они также являются огнезащитными добавками к пластмассам и резиновым изделиям.
- Борная кислота (также известная как ортоборная кислота) H 3 BO 3 используется в производстве текстильных стекловолоконных дисплеев и плоских панелей, а также во многих клеях на основе PVAc и PVOH .
- Триэтилборан - это вещество, которое воспламеняет топливо JP-7 турбореактивных / прямоточных двигателей Pratt & Whitney J58, установленных на Lockheed SR-71 Blackbird . Она также используется, чтобы зажечь F-1 Двигатели на Saturn V Rocket , используемой NASA «s Apollo и Skylab программ с 1967 до 1973. В настоящее время SpaceX использует его , чтобы зажечь двигатели на их Фалькон 9 ракеты. Триэтилборан подходит для этого из-за его пирофорных свойств, особенно из-за того, что он горит при очень высокой температуре. Триэтилборан является промышленным инициатором в радикальных реакциях, где он эффективен даже при низких температурах.
- Бораты используются как экологически безопасные консерванты для древесины .
Фармацевтические и биологические применения
Борная кислота обладает антисептическими, противогрибковыми и противовирусными свойствами и по этим причинам применяется в качестве осветлителя воды при очистке воды в плавательных бассейнах. Мягкие растворы борной кислоты использовались в качестве антисептиков для глаз.
Бортезомиб (продается как Велкейд и Цитомиб ). Бор выступает в качестве активного элемента в его первом одобренном органическом фармацевтическом препарате бортезомибе, новом классе препаратов, называемых ингибиторами протеасом, которые активны при миеломе и одной из форм лимфомы (в настоящее время он проходит экспериментальные испытания против других типов лимфома). Атом бора в бортезомибе связывает каталитический сайт протеасомы 26S с высоким сродством и специфичностью.
- Ряд потенциальных борсодержащих фармацевтических препаратов, использующих бор-10 , был подготовлен для использования в борной нейтронно-захватной терапии (BNCT).
- Некоторые соединения бора перспективны при лечении артрита , хотя ни одно из них еще не одобрено для этой цели.
Таваборол (продаваемый как Керидин ) представляет собойингибитор аминоацил тРНК синтетазы , который используется для лечения грибка ногтей на ногах. Он получил одобрение FDA в июле 2014 года.
Химический состав диоксаборолана позволяет маркировать антитела или эритроциты радиоактивным фторидом ( 18 F ) , что позволяет получать изображения рака и кровоизлияний с помощью позитронно-эмиссионной томографии (ПЭТ) соответственно. A H uman- D erived, G enetic, Р ositron-излучающее и F luorescent (HD-ГПФ) Система репортера использует белка человека, ПСМ и неиммуногенный, и небольшая молекула , которая является позитроном-излучающим (бор связаны 18 F ) и флуоресцентный для двойной модальности ПЭТ и флуоресцентной визуализации модифицированных геномных клеток, например раковых , CRISPR / Cas9 или CAR Т- клеток, у всей мыши. Двухкомпонентная малая молекула, нацеленная на PSMA, была протестирована на людях и обнаружила локализацию первичного и метастатического рака простаты , удаление рака под контролем флуоресценции и обнаружение единичных раковых клеток на краях тканей.
Области исследований
Диборид магния - важный сверхпроводящий материал с температурой перехода 39 К. Проволока MgB 2 производится методом порошка в трубке и применяется в сверхпроводящих магнитах.
Аморфный бор используется в качестве депрессора точки плавления в никель-хромовых припоях.
Гексагональный нитрид бора образует атомарно тонкие слои, которые используются для увеличения подвижности электронов в графеновых устройствах. Он также образует нанотрубчатые структуры ( BNNT ), которые обладают высокой прочностью, высокой химической стабильностью и высокой теплопроводностью , что входит в список желаемых свойств.
Биологическая роль
Бор - это важное питательное вещество для растений , необходимое в первую очередь для поддержания целостности клеточных стенок. Однако высокие концентрации в почве, превышающие 1,0 ppm, приводят к некрозу краев и кончиков листьев, а также к снижению общих показателей роста. Уровни всего 0,8 ppm вызывают те же симптомы у растений, которые особенно чувствительны к бору в почве. Почти все растения, даже те, которые в некоторой степени устойчивы к почвенному бору, проявляют по крайней мере некоторые симптомы токсичности бора, когда содержание бора в почве превышает 1,8 ppm. Когда это содержание превышает 2,0 ppm, немногие растения будут хорошо себя чувствовать, а некоторые могут не выжить.
Считается, что бор играет несколько важных ролей у животных, включая человека, но точная физиологическая роль плохо изучена. В небольшом исследовании на людях, опубликованном в 1987 году, сообщалось о женщинах в постменопаузе, у которых сначала наблюдался дефицит бора, а затем вводилось 3 мг / день. Добавки бора заметно снижали выведение кальция с мочой и повышали сывороточные концентрации 17-бета-эстрадиола и тестостерона.
Институт медицины США не подтвердил, что бор является важным питательным веществом для человека, поэтому ни рекомендованная диета (RDA), ни адекватное потребление не установлены. Потребление с пищей взрослыми составляет от 0,9 до 1,4 мг / день, при этом всасывается около 90%. То, что всасывается, в основном выводится с мочой. Допустимый верхний уровень потребления для взрослых составляет 20 мг / день.
В 2013 году была выдвинута гипотеза, согласно которой бор и молибден могли катализировать образование РНК на Марсе, при этом жизнь переносилась на Землю через метеорит около 3 миллиардов лет назад.
Существует несколько известных борсодержащих природных антибиотиков . Первым был обнаружен боромицин , выделенный из стрептомицетов .
Врожденная эндотелиальная дистрофия 2 типа , редкая форма дистрофии роговицы , связана с мутациями в гене SLC4A11 , который кодирует переносчик, который, как сообщается, регулирует внутриклеточную концентрацию бора.
Аналитическая количественная оценка
Для определения содержания бора в продуктах питания или материалах используется колориметрический метод куркумина . Бора преобразуется в борную кислоту или бораты и реакция с куркумином в кислом растворе, красного цвет бора хелат комплекс, rosocyanine , формируются.
Проблемы со здоровьем и токсичность
| Опасности | |
|---|---|
| Пиктограммы GHS |

|
| Сигнальное слово GHS | Предупреждение |
| H302 | |
| NFPA 704 (огненный алмаз) | |
Элементарный бор, оксид бора , борная кислота , бораты и многие борорганические соединения относительно нетоксичны для людей и животных (с токсичностью, аналогичной таковой у поваренной соли). LD 50 (доза , при которой происходит 50% смертность) для животных составляет около 6 г на кг массы тела. Вещества с LD 50 выше 2 г считаются нетоксичными. Сообщалось о приеме 4 г борной кислоты в день без происшествий, но большее количество считается токсичным при более чем нескольких дозах. Прием более 0,5 грамма в день в течение 50 дней вызывает незначительные проблемы с пищеварением и другие проблемы, указывающие на токсичность. Пищевые добавки бора могут быть полезны для роста костей, заживления ран и антиоксидантной активности, а недостаточное количество бора в рационе может привести к его дефициту .
Разовые медицинские дозы 20 г борной кислоты для нейтронно-захватной терапии использовались без чрезмерной токсичности.
Борная кислота более токсична для насекомых, чем для млекопитающих, и обычно используется в качестве инсектицида.
В боранах (бор соединений водорода) и аналогичные газообразные соединения являются весьма ядовитыми. Как обычно, бор не является ядовитым элементом по своей природе, но токсичность этих соединений зависит от структуры (другой пример этого явления см. В фосфине ). Бораны также легко воспламеняются и требуют особой осторожности при обращении. Боргидрид натрия представляет опасность пожара из-за его восстанавливающей природы и выделения водорода при контакте с кислотой. Галогениды бора вызывают коррозию.
Бор необходим для роста растений, но его избыток токсичен для растений, особенно в кислой почве. Это проявляется в виде пожелтения кончиков внутрь самых старых листьев и черных пятен на листьях ячменя, но его можно спутать с другими стрессами, такими как дефицит магния у других растений.
Смотрите также
использованная литература
внешние ссылки
- Бор в Периодической таблице видео (Ноттингемский университет)
- JB Calvert: Boron , 2004, частный сайт ( архивная версия )











