Диборан - Diborane

|
|

|
|
| Имена | |
|---|---|
|
Название ИЮПАК
Диборан (6)
|
|
| Другие имена
Бороэтан
Гидрид бора Гексагидрид дибора |
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard |
100.039.021 |
| Номер ЕС | |
|
PubChem CID
|
|
| Номер RTECS | |
| UNII | |
| Номер ООН | 1911 г. |
|
Панель управления CompTox ( EPA )
|
|
|
|
|
|
| Характеристики | |
| B 2 H 6 | |
| Молярная масса | 27,67 г · моль -1 |
| Появление | Бесцветный газ |
| Запах | отталкивающий и сладкий |
| Плотность | 1,131 г / л |
| Температура плавления | -164,85 ° С (-264,73 ° F, 108,30 К) |
| Точка кипения | -92,49 ° С (-134,48 ° F, 180,66 К) |
| Реагирует | |
| Растворимость в других растворителях | Слабо растворим в диглиме и диэтиловом эфире , |
| Давление газа | 39,5 атм (16,6 ° C) |
| Состав | |
| Тетраэдр (для бора) | |
| см. текст | |
| 0 Д | |
| Термохимия | |
|
Теплоемкость ( C )
|
56,7 Дж / (моль · К) |
|
Стандартная мольная
энтропия ( S |
232,1 Дж / (моль · К) |
|
Std энтальпия
формации (Δ F H ⦵ 298 ) |
36,4 кДж / моль |
| Опасности | |
| Основные опасности | легко воспламеняется, реагирует с водой |
| Паспорт безопасности | См .: страницу данных |
| Пиктограммы GHS |
    
|
| Сигнальное слово GHS | Опасность |
| H220 , H280 , H314 , H318 , H330 , H370 , H372 | |
| Р210 , Р260 , Р264 , Р270 , Р271 , Р280 , Р284 , Р301 + 330 + 331 , P303 + 361 + 353 , Р304 + 340 , P305 + 351 + 338 , P307 + 311 , P310 , P314 , P320 , P321 , P363 , P377 , P381 , P403 , P403 + 233 , Р405 , Р410 + 403 , Р501 | |
| NFPA 704 (огненный алмаз) | |
| 38 ° С (100 ° F, 311 К) | |
| Пределы взрываемости | 0,8–88% |
| Смертельная доза или концентрация (LD, LC): | |
|
ЛК 50 ( средняя концентрация )
|
40 частей на миллион (крыса, 4 часа ) 29 частей на миллион (мышь, 4 часа) 40–80 частей на миллион (крыса, 4 часа) 159–181 частей на миллион (крыса, 15 минут ) |
|
LC Lo ( самый низкий опубликованный )
|
125 частей на миллион (собака, 2 часа) 50 частей на миллион (хомяк, 8 часов) |
| NIOSH (пределы воздействия на здоровье в США): | |
|
PEL (Допустимо)
|
TWA 0,1 частей на миллион (0,1 мг / м 3 ) |
|
REL (рекомендуется)
|
TWA 0,1 частей на миллион (0,1 мг / м 3 ) |
|
IDLH (Непосредственная опасность)
|
15 частей на миллион |
| Родственные соединения | |
|
Родственные соединения бора
|
Декаборан BF 3 |
| Страница дополнительных данных | |
|
Показатель преломления ( n ), диэлектрическая проницаемость (ε r ) и т. Д. |
|
|
Термодинамические
данные |
Фазовое поведение твердое тело – жидкость – газ |
| УФ , ИК , ЯМР , МС | |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
Диборан (6) , обычно известный как диборан , представляет собой химическое соединение, состоящее из бора и водорода с формулой B 2 H 6 . Это бесцветный пирофорный газ с отвратительно сладким запахом. Синонимы включают борэтан, гидрид бора и гексагидрид дибора. Диборан - это ключевое соединение бора, имеющее множество применений. Он привлек широкое внимание своей электронной структурой. Его производные - полезные реагенты.
Структура и склеивание
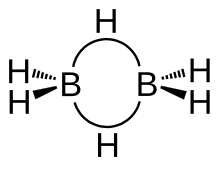
Структура диборана имеет симметрию D 2h . Четыре гидрида являются терминальными, а два - мостиковыми между центрами бора. Длины мостиковых связей B – H и концевых связей B – H составляют 1,33 и 1,19 Å соответственно. Эта разница в длине связи отражает разницу в их прочности, причем мостиковые связи B – H относительно слабее. На слабость моста B – H по сравнению с концевыми связями B – H указывают их колебательные сигнатуры в инфракрасном спектре , составляющие ≈2100 и 2500 см –1 соответственно.
Модель, определяемая теорией молекулярных орбиталей, описывает связи между бором и концевыми атомами водорода как обычные двухцентровые двухэлектронные ковалентные связи . Однако связь между атомами бора и мостиковыми атомами водорода отличается от связи в молекулах, таких как углеводороды. Каждый бор использует два электрона для связи с концевыми атомами водорода и имеет один валентный электрон, оставшийся для дополнительной связи. Мостиковые атомы водорода обеспечивают по одному электрону каждый. Кольцо B 2 H 2 удерживается вместе четырьмя электронами, образующими две трехцентровые двухэлектронные связи . Этот тип облигации иногда называют «банановой облигацией».
В 2 Н 6 является изоэлектронным с C 2 H 6 2+ , который бы возникнуть из diprotonation из планарных молекул этилена . Диборан - одно из многих соединений с такой необычной связью.
Из других элементов группы IIIA известно, что галлий образует аналогичное соединение дигаллан , Ga 2 H 6 . Алюминий образует полимерный гидрид (AlH 3 ) n ; хотя и нестабилен, Al 2 H 6 был изолирован в твердом водороде и изоструктурен диборану.
Производство и синтез
Обширные исследования диборана привели к развитию множественных синтезов. Большинство препаратов включает реакции доноров гидридов с галогенидами или алкоксидами бора. Промышленный синтез диборана включает восстановление BF 3 с помощью гидрида натрия , гидрид лития или гидрид лития и алюминия :
- 8 BF 3 + 6 LiH → B 2 H 6 + 6 LiBF 4
Два лабораторных метода начинаются с треххлористого бора с алюмогидридом лития или с раствора эфира трифторида бора с борогидридом натрия . Оба метода дают доходность до 30%:
- 4 BCl 3 + 3 LiAlH 4 → 2 B 2 H 6 + 3 LiAlCl 4
- 4 BF 3 + 3 NaBH 4 → 2 B 2 H 6 + 3 NaBF 4
Старые методы предполагают прямую реакцию солей боргидрида с неокисляющей кислотой , такой как фосфорная кислота или разбавленная серная кислота .
- 2 ЧД 4 - + 2 Н + → 2 Н 2 + В 2 Н 6
Точно так же было продемонстрировано окисление боргидридных солей, и оно остается удобным для получения в небольших количествах. Например, используя йод в качестве окислителя:
- 2 NaBH
4 + Я
2 → 2 NaI + B
2ЧАС
6 + H
2
Другой маломасштабный синтез использует гидроборат калия и фосфорную кислоту в качестве исходных материалов.
Реакции

Диборан - очень реактивный и универсальный реагент.
Воздух, вода, кислород
Как пирофорное вещество, диборан экзотермически реагирует с кислородом с образованием триоксида бора и воды:
Диборан бурно реагирует с водой с образованием водорода и борной кислоты :
- B 2 H 6 + 6 H 2 O → 2 B (OH) 3 + 6 H 2 (Δ H r = -466 кДж / моль = -16,82 кДж / г )
Диборан также реагирует со спиртами аналогичным образом. Метанол например дает водород и триметилборат :
- B 2 H 6 + 6 MeOH → 2 B (OMe) 3 + 6 H 2
Кислотность Льюиса
Один доминирующий образец реакции включает образование аддуктов с основаниями Льюиса . Часто такие начальные аддукты быстро переходят в другие продукты. Например, боран-тетрагидрофуран, который часто ведет себя как эквивалент диборана, разлагается до сложных эфиров бората. Его аддукт с диметилсульфидом является важным реагентом в органическом синтезе .
С дибораном аммиака с образованием диаммониата диборана, DADB, с меньшими количествами борана аммиака , в зависимости от условий.
Гидроборация
В гидроборировании реакции, диборан также легко реагирует с алкенами с образованием три- алкилборанов . Этот образец реакции является довольно общим, и полученные алкилбораты могут быть легко преобразованы в производные, например, в спирты. Хотя ранние работы по гидроборированию основывались на диборане, его заменили диметилсульфидом борана, с которым более безопасно обращаться.
Другой
Пиролиз диборана дает водород и разнообразные кластеры гидрида бора. Например, пентаборан был сначала получен пиролизом диборана при температуре около 200 ° C. Хотя этот путь пиролиза используется редко, он положил начало большой исследовательской теме химии борановых кластеров .
Обработка диборана амальгамой натрия дает NaBH 4 и Na [B 3 H 8 ]. Когда диборан обрабатывают гидридом лития в диэтиловом эфире , образуется боргидрид лития:
- B 2 H 6 + 2 LiH → 2 LiBH 4
Диборан реагирует с безводным хлористым водородом или газообразным бромистым водородом с образованием галогенгидрида бора:
- В 2 Н 6 + НХ → В 2 Н 5 Х + Н 2 (X = Cl, Br)
Обработка диборана оксидом углерода при 470 К и 20 бар дает H 3 BCO .
Реагент в органическом синтезе
Диборан и его варианты являются центральными реагентами органического синтеза для гидроборирования . Алкены присоединяются по связям B – H с образованием триалкилборанов, которые могут быть дополнительно разработаны. Диборан используется в качестве восстановителя, примерно дополняющего реакционную способность алюмогидрида лития . Соединение легко восстанавливает карбоновые кислоты до соответствующих спиртов , тогда как кетоны реагируют очень медленно.
История
Диборан был впервые синтезирован в 19 веке путем гидролиза боридов металлов, но никогда не анализировался. С 1912 по 1936 год Альфред Сток , главный пионер химии гидридов бора, провел свои исследования, которые привели к разработке методов синтеза и обращения с высокореактивными, летучими и часто токсичными гидридами бора. Он предложил первый этан -like структуры диборана. Изначально измерения дифракции электронов, выполненные С. Х. Бауэром, подтвердили его предложенную структуру.
Из-за личного общения с Л. Полингом (который поддерживал этаноподобную структуру) Х. И. Шлессинджер и А. Б. Бург не обсуждали конкретно трехцентровую и двухэлектронную связь в своем тогдашнем классическом обзоре в начале 1940-х годов. В обзоре, однако, довольно подробно обсуждается мостиковая структура D 2h : «Следует признать, что этот состав легко объясняет многие химические свойства диборана ...»
В 1943 году Х. Кристофер Лонге-Хиггинс , еще будучи студентом Оксфорда, был первым, кто объяснил структуру и связь гидридов бора. В статье о работе, написанной с его наставником Р. П. Беллом , также рассматривается история предмета, начиная с работ Дильтея. Вскоре после этого теоретическая работа Лонге-Хиггинса была подтверждена Прайсом в инфракрасном исследовании диборана. Структура была повторно подтверждена измерениями дифракции электронов в 1951 г. К. Хедбергом и В. Шомакером, с подтверждением структуры, показанной на схемах на этой странице.
Уильям Нанн Липскомб- младший дополнительно подтвердил молекулярную структуру борана с помощью рентгеновской кристаллографии в 1950-х годах и разработал теории, объясняющие их связь. Позже он применил ту же методу к проблемам , связанным, в том числе структуры карборанов, на которой он руководил исследованием будущих 1981 Нобелевской премии победителя Роальд Гофман . Нобелевская премия по химии 1976 г. была присуждена Липскомбу «за исследования структуры боранов, освещающие проблемы химической связи».
Традиционно диборан часто описывался как электронодефицитный , потому что 12 валентных электронов могут образовывать только 6 обычных 2-центровых 2-электронных связей, которых недостаточно для соединения всех 8 атомов. Однако более правильное описание с использованием трехцентровых связей показывает, что диборан действительно электронно точен, поскольку валентных электронов достаточно, чтобы заполнить 6 связывающих молекулярных орбиталей . Тем не менее, в некоторых ведущих учебниках до сих пор используется термин «электронодефицитный».
Другое использование
Из-за экзотермичности его реакции с кислородом диборан был испытан в качестве ракетного топлива . Полное сгорание является сильно экзотермическим. Однако сгорание в ракетном двигателе не завершается, так как образуется некоторое количество окиси бора B 2 O. Это преобразование отражает неполное сгорание углеводородов с образованием окиси углерода (CO). Диборан также оказался трудным в обращении.
Диборан был исследован как предшественник пленок боридов металлов и для p-легирования кремниевых полупроводников.
Безопасность
Диборан - пирофорный газ. Вместо этого обычно используются коммерчески доступные аддукты, по крайней мере, для приложений в органической химии. Эти аддукты включают боран-тетрагидрофуран (боран-ТГФ) и боран-диметилсульфид . Токсические эффекты диборана смягчаются, поскольку это соединение нестабильно на воздухе. Токсичность по отношению к лабораторным крысам была исследована.
использованная литература
Цитированные источники
- Хейнс, Уильям М., изд. (2011). CRC Справочник по химии и физике (92-е изд.). CRC Press . ISBN 978-1439855119.
- Yerazunis, S., et al. «Растворимость диборана в диметиловом эфире и диэтиленгликоле, в смесях боргидрида натрия и диметилового эфира диэтиленгликоля, а также в диметиловом бутилсульфиде». Журнал химических и технических данных , вып. 7, вып. 3, июль 1962 г., стр. 337–39, DOI: 10.1021 / je60014a004.

