Нитрат рубидия - Rubidium nitrate

|
|
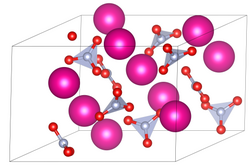 Элементарная ячейка нитрата рубидия
|
|
| Имена | |
|---|---|
|
Название ИЮПАК
Нитрат рубидия
|
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.032.767 |
| Номер ЕС | |
|
PubChem CID
|
|
| Номер RTECS | |
|
Панель управления CompTox ( EPA )
|
|
|
|
|
|
| Характеристики | |
| RbNO 3 | |
| Молярная масса | 147,473 г / моль |
| Появление | Белое гигроскопичное твердое вещество |
| Плотность | 3,11 г / см 3 |
| Температура плавления | 310 ° С (590 ° F, 583 К) разлагается |
| Точка кипения | 578 ° С (1072 ° F, 851 К) |
| 44,28 г / 100 мл (16 ° C) 65,0 г / 100 мл (25 ° C) |
|
| −41,0 · 10 −6 см 3 / моль | |
|
Показатель преломления ( n D )
|
1,524 |
| Состав | |
| тригональный | |
| P3 1 | |
|
а = 10,474 Å, с = 7,443 Å
|
|
|
Объем решетки ( В )
|
707,2 Å 3 |
| Опасности | |
| Основные опасности | Окислитель |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | Не воспламеняется |
| Смертельная доза или концентрация (LD, LC): | |
|
LD 50 ( средняя доза )
|
4625 мг / кг (крыса, перорально) |
| Родственные соединения | |
|
Другие анионы
|
Сульфат рубидия Хлорид рубидия |
|
Другие катионы
|
Нитрат лития Нитрат натрия Нитрат калия Нитрат цезия |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
Нитрат рубидия - неорганическое соединение с формулой Rb NO 3 . Эта соль нитрата щелочного металла имеет белый цвет и хорошо растворяется в воде.
Характеристики
Нитрат рубидия представляет собой белый кристаллический порошок, который хорошо растворяется в воде и очень слабо растворяется в ацетоне . При испытании пламенем RbNO 3 дает розовато-лиловый / светло-фиолетовый цвет.
Использует
Соединения рубидия имеют очень мало применений. Подобно нитрату цезия , он используется в оптике инфракрасного излучения, в пиротехнических композициях в качестве пиротехнического красителя и в качестве окислителя , например, в ловушках и осветительных ракетах, хотя он редко используется в фейерверках для получения красно-фиолетового цвета. Он также используется в качестве сырья для получения других соединений рубидия и металлического рубидия, для производства катализаторов и в сцинтилляционных счетчиках .
Производство
RbNO 3 можно получить растворением металлического рубидия, его гидроксида или карбоната в азотной кислоте.
- RbOH + HNO 3 → RbNO 3 + H 2 O
- 2 Rb + 2 HNO 3 → 2 RbNO 3 + H 2
Рекомендации
- ^ a b В. Ленк, Х. Принц, А. Стейнмец, «Рубидий и рубидиевые соединения» в Энциклопедии промышленной химии Ульмана, 2010 г. Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim. DOI : 10.1002 / 14356007.a23_473.pub2
- ^ Ютта Pohl, Dieter Pohl, Gunadi Adiwidjaja (1992). «Фазовый переход в нитрате рубидия при 346 К и структура при 296, 372, 413 и 437 К» . Acta Crystallographica Раздел B . B48 : 160–166. DOI : 10.1107 / S0108768191013459 .CS1 maint: несколько имен: список авторов ( ссылка )


