Нитрат фтора - Fluorine nitrate

|
|
|
|
| Идентификаторы | |
|---|---|
|
3D модель ( JSmol )
|
|
| ChemSpider | |
|
PubChem CID
|
|
| UNII | |
|
Панель управления CompTox ( EPA )
|
|
|
|
|
|
| Свойства | |
| F N O 3 | |
| Молярная масса | 81,002 г · моль -1 |
| Плотность | 2,217 г / л |
| Температура плавления | -175 ° С (-283,0 ° F, 98,1 К) |
| Точка кипения | -46 ° С (-51 ° F, 227 К) |
| Термохимия | |
|
Std энтальпия
формации (Δ F H ⦵ 298 ) |
+10,46 кДж / моль |
| Опасности | |
| Основные опасности | Взрывоопасный газ |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
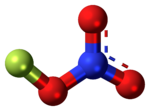
Нитрат фтора - нестабильное производное азотной кислоты с формулой FNO.
3. Он чувствителен к ударам. Из-за его нестабильности при необходимости его часто производят из нитрата хлора .
Синтез и свойства
Нитрат фтора образуется, когда газообразный фтор барботируют через азотную кислоту или реагируют с твердым нитратом калия :
- F
2 + HNO
3 → FNO
3 + ВЧ
- F
2 + KNO
3 → FNO
3 + KF
Он разлагается в воде с образованием кислорода газа, дифторидом кислорода , фтористоводородной кислотой и азотной кислотой.
Ссылки
- Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8.
Соли и ковалентные производные нитрат- иона
| Этот товар, связанный с неорганическими соединениями, является незавершенным . Вы можете помочь Википедии, расширив ее . |
