Хром (II) хлорид - Chromium(II) chloride

|
|

|
|
| Имена | |
|---|---|
|
Название ИЮПАК
Хром (II) хлорид
|
|
| Другие имена
Хромовый хлорид
|
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.030.136 |
| Номер ЕС | |
|
PubChem CID
|
|
| Номер RTECS | |
| UNII | |
| Номер ООН | 3077 |
|
Панель управления CompTox ( EPA )
|
|
|
|
|
|
| Характеристики | |
| Cl 2 Cr | |
| Молярная масса | 122,90 г · моль -1 |
| Внешность | Порошок от белого до серого / зеленого цвета (безводный), очень гигроскопичный |
| Запах | Без запаха |
| Плотность | 2,88 г / см 3 (24 ° C) |
| Температура плавления | 824 ° C (1515 ° F, 1097 K) безводный 51 ° C (124 ° F, 324 K) тетрагидрат, разлагается |
| Точка кипения | 1302 ° C (2376 ° F, 1575 K) безводный |
| Растворимый | |
| Растворимость | Не растворим в спирте , эфире |
| Кислотность (p K a ) | 2 |
| + 7230 · 10 −6 см 3 / моль | |
| Структура | |
|
Орторомбический (деформированный рутил , безводный), oP6 Моноклинный (тетрагидрат) |
|
| Pnnm, № 58 (безводный) P2 1 / c, № 14 (тетрагидрат) |
|
| 2 / м 2 / м 2 / м (безводный) 2 / м (тетрагидрат) |
|
|
a = 6,64 Å, b = 5,98 Å, c = 3,48 Å (безводный)
α = 90 °, β = 90 °, γ = 90 °
|
|
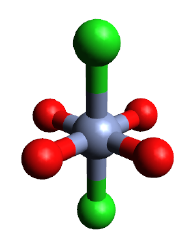
| Октаэдрический (Cr 2+ , безводный) | |
| Термохимия | |
|
Теплоемкость ( C )
|
71,2 Дж / моль · К |
|
Стандартная мольная
энтропия ( S |
115,3 Дж / моль · К |
|
Std энтальпия
формации (Δ F H ⦵ 298 ) |
-395,4 кДж / моль |
|
Свободная энергия Гиббса (Δ f G ˚)
|
−356 кДж / моль |
| Опасности | |
| Паспорт безопасности | Оксфордский паспорт безопасности материалов |
| Пиктограммы GHS |

|
| Сигнальное слово GHS | Предупреждение |
| H302 , H315 , H319 , H335 | |
| P261 , P305 + 351 + 338 | |
| NFPA 704 (огненный алмаз) | |
| Смертельная доза или концентрация (LD, LC): | |
|
LD 50 ( средняя доза )
|
1870 мг / кг (крысы, перорально) |
| Родственные соединения | |
|
Другие анионы
|
Фторид хрома (II) Бромид хрома (II) Иодид хрома (II) |
|
Другие катионы
|
Хлорид хрома (III) Хлорид хрома (IV) Хлорид молибдена (II) Хлорид вольфрама (II) |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
Хром (II) хлорид описывает неорганические соединения с формулой Cr Cl 2 (H 2 O) n . Безводное твердое вещество в чистом виде имеет белый цвет, однако коммерческие образцы часто имеют серый или зеленый цвет; он гигроскопичен и легко растворяется в воде с образованием ярко-голубых чувствительных к воздуху растворов тетрагидрата Cr (H 2 O) 4 Cl 2 . Хлорид хрома (II) не имеет коммерческого использования, но используется в лабораторных условиях для синтеза других комплексов хрома.
Синтез
Циклический 2 получают восстановление хрома (III) , хлорид либо с водородом при 500 ° C:
- 2 CrCl 3 + H 2 → 2 CrCl 2 + 2 HCl
или электролизом.
Небольшие препараты могут использовать LiAlH 4 , цинк или родственные реагенты для восстановления CrCl 3.
- 4 CrCl 3 + LiAlH 4 → 4 CrCl 2 + LiCl + AlCl 3 + 2 H 2
- 2 CrCl 3 + Zn → 2 CrCl 2 + ZnCl 2
CrCl 2 можно также получить обработкой раствора ацетата хрома (II) хлористым водородом.
- Cr 2 (OAc) 4 + 4 HCl → 2 CrCl 2 + 4 AcOH
Структура и свойства
Безводный CrCl 2 имеет белый цвет, однако коммерческие образцы часто имеют серый или зеленый цвет. Он кристаллизуется в пространственной группе Pnnm , которая представляет собой орторомбически искаженный вариант структуры рутила ; делая его изоструктурным хлориду кальция . Центры Cr октаэдрические , искаженные эффектом Яна-Теллера .
Гидратированное производное CrCl 2 (H 2 O) 4 образует моноклинные кристаллы с пространственной группой P2 1 / c . Геометрия молекулы приблизительно октаэдрическая, состоящая из четырех коротких связей Cr-O (2,078 Å), расположенных в плоской квадратной конфигурации, и двух более длинных связей Cr-Cl (2,758 Å) в транс-конфигурации.
Реакции
Восстановительный потенциал для Cr 3+ + е - ⇄ Cr 2+ составляет -0,41. Поскольку потенциал восстановления H + до H 2 в кислых условиях равен +0,00, ион хрома имеет достаточный потенциал для восстановления кислот до водорода, хотя эта реакция не происходит без катализатора.
Органическая химия
Хлорид хрома (II) используется в качестве предшественника других неорганических и металлоорганических комплексов хрома. Алкилгалогениды и нитроароматические соединения восстанавливаются CrCl 2 . Умеренная электроотрицательность хрома и диапазон субстратов, которые может принимать CrCl 2, делают хроморганические реагенты очень универсальными с точки зрения синтеза. Это реагент в реакции Нодзаки-Хияма-Киши , полезном методе получения колец среднего размера. Он также используется при олефинизации Такаи для образования винилиодидов из альдегидов в присутствии йодоформа .