Активин и ингибин - Activin and inhibin
| ингибин, альфа | |||||||
|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||
| Символ | INHA | ||||||
| Ген NCBI | 3623 | ||||||
| HGNC | 6065 | ||||||
| OMIM | 147380 | ||||||
| RefSeq | NM_002191 | ||||||
| UniProt | P05111 | ||||||
| Прочие данные | |||||||
| Locus | Chr. 2 кв. 33 кв. | ||||||
| |||||||
| ингибин, бета А | |||||||
|---|---|---|---|---|---|---|---|
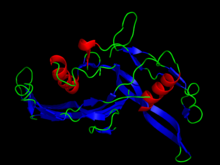 Димер активина, из 2ARV.pdb
| |||||||
| Идентификаторы | |||||||
| Символ | INHBA | ||||||
| Альт. символы | активин А | ||||||
| Ген NCBI | 3624 | ||||||
| HGNC | 6066 | ||||||
| OMIM | 147290 | ||||||
| RefSeq | NM_002192 | ||||||
| UniProt | P08476 | ||||||
| Прочие данные | |||||||
| Locus | Chr. 7 стр. 15–13 | ||||||
| |||||||
| ингибин, бета B | |||||||
|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||
| Символ | INHBB | ||||||
| Альт. символы | активин B | ||||||
| Ген NCBI | 3625 | ||||||
| HGNC | 6067 | ||||||
| OMIM | 147390 | ||||||
| RefSeq | NM_002193 | ||||||
| UniProt | P09529 | ||||||
| Прочие данные | |||||||
| Locus | Chr. 2 цен-q13 | ||||||
| |||||||
| ингибин, бета C | |||||||
|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||
| Символ | INHBC | ||||||
| Альт. символы | активин С | ||||||
| Ген NCBI | 3626 | ||||||
| HGNC | 6068 | ||||||
| OMIM | 601233 | ||||||
| RefSeq | NM_005538 | ||||||
| UniProt | P55103 | ||||||
| Прочие данные | |||||||
| Locus | Chr. 12 q13 | ||||||
| |||||||
| ингибин, бета E | |||||||
|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||
| Символ | INHBE | ||||||
| Альт. символы | активин E | ||||||
| Ген NCBI | 83729 | ||||||
| HGNC | 24029 | ||||||
| OMIM | 612031 | ||||||
| RefSeq | NM_031479 | ||||||
| UniProt | P58166 | ||||||
| Прочие данные | |||||||
| Locus | Chr. 12 q13.2 | ||||||
| |||||||
Активин и ингибин - два тесно связанных белковых комплекса, которые обладают почти прямо противоположными биологическими эффектами. Выявленные в 1986 году, активин совершенствует FSH биосинтез и секрецию , участвует в регуляции менструального цикла . Было обнаружено, что активин выполняет многие другие функции, включая роль в пролиферации, дифференцировке , апоптозе , метаболизме , гомеостазе , иммунном ответе , заживлении ран и эндокринной функции. И наоборот, ингибин подавляет синтез ФСГ и подавляет секрецию ФСГ. Предположение о существовании ингибина было выдвинуто еще в 1916 году; однако, его существование не было продемонстрировано до работы Нины Шварц и Корнелии Ченнинг в середине 1970-х годов, после чего оба белка были молекулярно охарактеризованы десятью годами позже.
Активин представляет собой димер, состоящий из двух идентичных или очень похожих бета-субъединиц. Ингибин также представляет собой димер, в котором первый компонент представляет собой бета-субъединицу, аналогичную или идентичную бета-субъединице в активине. Однако, в отличие от активина, второй компонент димера ингибина является более отдаленно связанной альфа-субъединицей. Активин, ингибин и ряд других структурно родственных белков, таких как антимюллеров гормон , костный морфогенетический белок и фактор дифференцировки роста, принадлежат к суперсемейству белков TGF-β .
Состав
Активин и ингибин белковых комплексов являются димерным в структуре, и в каждом комплексе, два мономер соединен друг с другом посредством одной дисульфидной связи . Кроме того, оба комплекса происходят из одного и того же семейства родственных генов и белков, но различаются по своему субъединичному составу. Ниже приведен список наиболее распространенных комплексов ингибина и активина и их субъединичный состав:
|
|
|||||||||||||||||||||||||||
Альфа- и бета-субъединицы имеют примерно 25% сходства последовательностей , тогда как сходство между бета-субъединицами составляет примерно 65%.
У млекопитающих четыре бета - субъединицы, были описаны, называемый активин & beta ; A , & beta ; активин B , активин β С и активин β Е . Активин β A и β B идентичны двум бета-субъединицам ингибина. Пятая субъединица, активин β D , была описана у Xenopus laevis . Две субъединицы активина β A дают начало активину A, одна субъединица β A , а одна субъединица β B дает активин AB и так далее. Описаны различные, но не все теоретически возможные гетеродимеры. Субъединицы связаны одной ковалентной дисульфидной связью.
Β С субъединица может образовывать активин гетеродимеров с & beta ; A или & beta ; B субъединиц , но не может димеризации с ингибин а.
Функция
Активин
Активин вырабатывается гонадами , гипофизом , плацентой и другими органами:
- В фолликуле яичника активин увеличивает связывание ФСГ и вызванную ФСГ ароматизацию . Он участвует в синтезе андрогенов, усиливая действие ЛГ в яичниках и семенниках . У мужчин активин усиливает сперматогенез .
- Активин сильно выражен в раненой коже , а избыточная экспрессия активина в эпидермисе от трансгенного мышея улучшает заживление ран и улучшает рубцовое образование. Его действие в заживлении ран и морфогенезе кожи осуществляется через дозозависимую стимуляцию кератиноцитов и стромальных клеток .
- Активин также регулирует морфогенез ветвящихся органов, таких как простата , легкие и особенно почки . Активин А увеличивал уровень экспрессии коллагена типа I, предполагая, что активин А действует как мощный активатор фибробластов .
- Недостаток активина во время развития приводит к дефектам нервного развития.
- Повышающая регуляция Activin A заставляет плюрипотентные стволовые клетки участвовать в мезоэндодермальной судьбе и, таким образом, обеспечивает полезный инструмент для дифференцировки стволовых клеток и образования органоидов .
Ингибин
И у женщин, и у мужчин ингибин подавляет выработку ФСГ . Ингибин не подавляет секрецию гонадолиберина в гипоталамусе. Однако общий механизм различается между полами:
У женщин
Ингибин вырабатывается гонадами , гипофизом , плацентой , желтым телом и другими органами.
ФСГ стимулирует секрецию ингибина гранулезными клетками фолликулов яичников в яичниках . В свою очередь, ингибин подавляет ФСГ.
- Ингибин B достигает пика в ранней и средней фолликулярной фазе и второго пика при овуляции .
- Ингибин А достигает своего пика в средней лютеиновой фазе .
Секреция ингибина снижается GnRH и усиливается инсулиноподобным фактором роста -1 (IGF-1).
У мужчин
Он секретируется клетками Сертоли , расположенными в семенных канальцах внутри семенников . Андрогены стимулируют выработку ингибина; этот белок также может помочь локально регулировать сперматогенез .
Механизм действия
Активин
Как и другие члены суперсемейства, активины взаимодействуют с двумя типами трансмембранных рецепторов клеточной поверхности (типы I и II), которые обладают внутренней серин / треонинкиназной активностью в своих цитоплазматических доменах:
Активин связывается с рецептором типа II и инициирует каскадную реакцию, которая приводит к привлечению, фосфорилированию и активации рецептора активина типа I. Затем он взаимодействует и затем фосфорилирует SMAD2 и SMAD3 , два цитоплазматических белка SMAD .
Затем Smad3 перемещается в ядро и взаимодействует с SMAD4 посредством мультимеризации, в результате чего они модулируются как комплексы факторов транскрипции, ответственные за экспрессию большого разнообразия генов.
Ингибин
В отличие от активина, о механизме действия ингибина известно гораздо меньше, но он может включать конкуренцию с активином за связывание с рецепторами активина и / или связывание с рецепторами, специфичными для ингибина.
Клиническое значение
Активин
Активина А больше в жировой ткани у людей с ожирением, чем у худощавых людей. Активин А способствует пролиферации клеток-предшественников адипоцитов , подавляя их дифференцировку в адипоциты. Активин А также увеличивает воспалительные цитокины в макрофагах .
Мутации в гене рецептор активина ACVR1 приводит к фибродисплазии , смертельное заболевание , которое вызывает мышцы и мягкие ткани постепенно заменяются костной тканью. Это состояние характеризуется образованием лишнего скелета, который вызывает иммобилизацию и, в конечном итоге, смерть от удушья. Мутация в ACVR1 приводит к тому, что активин А, который обычно действует как антагонист рецептора и блокирует остеогенез (рост кости), ведет себя как агонист рецептора и вызывает гиперактивный рост кости. 2 сентября 2015 года Regeneron Pharmaceuticals объявила, что они разработали антитело к активину А, которое эффективно лечит болезнь на животной модели этого состояния.
Мутации в гене ACVR1 также связаны с раком, особенно с диффузной внутренней глиомой моста (DIPG).
Повышенный уровни активина B с нормальным уровнем активина А при условии возможного биомаркера для миальгического энцефаломиелита / синдрома хронической усталости .
Активин А сверхэкспрессируется при многих формах рака . Было показано, что он способствует онкогенезу , препятствуя адаптивному противоопухолевому иммунному ответу при меланоме .
Ингибин
Количественное определение ингибина А является частью пренатального квадрокоптера, который можно проводить во время беременности в гестационном возрасте 16–18 недель. Повышенный уровень ингибина А (наряду с повышенным уровнем бета-ХГЧ , пониженным уровнем АФП и пониженным содержанием эстриола ) свидетельствует о наличии у плода синдрома Дауна . В качестве скринингового теста результаты аномального квадрокоптера необходимо дополнить более точными тестами.
Он также использовался в качестве маркера рака яичников .
Ингибин B может использоваться как маркер функции сперматогенеза и мужского бесплодия . Средний уровень сывороточного ингибина B значительно выше у фертильных мужчин (примерно 140 пг / мл), чем у бесплодных мужчин (примерно 80 пг / мл). У мужчин с азооспермией положительный тест на ингибин B немного повышает шансы на успешное наступление беременности посредством экстракции сперматозоидов из яичек (TESE), хотя связь не очень существенна и имеет чувствительность 0,65 (95% доверительный интервал [ДИ]: 0,56 –0,74) и специфичность 0,83 (ДИ: 0,64–0,93) для прогнозирования наличия сперматозоидов в семенниках при необструктивной азооспермии.
Рекомендации
Внешние ссылки
- Активин в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH)
- Inhibin в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH)
- Грущ М., Крейдл Э. (1 августа 2008 г.). «Активин и фоллистатин в биологии печени и гепатоцеллюлярной карциноме» . SciTopics . Эльзевир. Архивировано 9 декабря 2008 года . Источник +24 Декабрь 2008 .

