Циклопропан - Cyclopropane

|
|||
|
|
|||
|
|
|||
| Имена | |||
|---|---|---|---|
|
Предпочтительное название IUPAC
Циклопропан |
|||
| Идентификаторы | |||
|
3D модель ( JSmol )
|
|||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard |
100.000.771 |
||
| КЕГГ | |||
|
PubChem CID
|
|||
| UNII | |||
|
Панель управления CompTox ( EPA )
|
|||
|
|||
|
|||
| Характеристики | |||
| С 3 Н 6 | |||
| Молярная масса | 42,08 г / моль | ||
| Появление | Бесцветный газ | ||
| Запах | Сладко пахнущий | ||
| Плотность | 1,879 г / л (1 атм, 0 ° С) | ||
| Температура плавления | -128 ° С (-198 ° F, 145 К) | ||
| Точка кипения | -33 ° С (-27 ° F, 240 К) | ||
| Кислотность (p K a ) | ~ 46 | ||
| -39,9 · 10 −6 см 3 / моль | |||
| Опасности | |||
| Основные опасности | Легковоспламеняющееся удушающее средство |
||
| Паспорт безопасности | Внешний паспорт безопасности материала | ||
| NFPA 704 (огненный алмаз) | |||
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|||
|
|
|||
| Ссылки на инфобоксы | |||
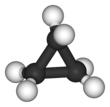
Циклопропан - это циклоалкан с молекулярной формулой (CH 2 ) 3 , состоящий из трех метиленовых групп (CH 2 ), связанных друг с другом с образованием кольца. Небольшой размер кольца создает значительную кольцевую деформацию в конструкции. Сам по себе циклопропан представляет в основном теоретический интерес, но многие его производные имеют коммерческое или биологическое значение.
История
Циклопропан был открыт в 1881 году Августом Фройндом , который также предложил правильную структуру вещества в своей первой статье. Фрейнда обрабатывают 1,3-дибромпропан с натрием , в результате чего внутримолекулярную реакции Вюрца , ведущую непосредственно к циклопропану. Выход реакции был улучшен Густавсоном в 1887 году с использованием цинка вместо натрия. Циклопропан не имел коммерческого применения, пока Хендерсон и Лукас не обнаружили его анестезирующие свойства в 1929 году; промышленное производство началось к 1936 году. В современной анестезиологической практике его вытеснили другие агенты.
Анестезия
Циклопропан был введен в клиническое использование американским анестезиологом Ральфом Уотерсом, который использовал закрытую систему с абсорбцией углекислого газа для сохранения этого дорогостоящего агента. Циклопропан является относительно сильнодействующим, не раздражающим и пахнущим агентом с минимальной альвеолярной концентрацией 17,5% и коэффициентом распределения кровь / газ 0,55. Это означало, что введение анестезии путем вдыхания циклопропана и кислорода было быстрым и приятным. Однако по завершении длительной анестезии у пациентов может наблюдаться внезапное снижение артериального давления, что может привести к сердечной аритмии : реакции, известной как «циклопропановый шок». По этой причине, а также из-за его высокой стоимости и взрывоопасности, в последнее время он использовался только для индукции анестезии и не был доступен для клинического использования с середины 1980-х годов. Цилиндры и расходомеры окрашены в оранжевый цвет.
Фармакология
Циклопропан неактивен в отношении рецепторов ГАМК А и глицина и вместо этого действует как антагонист рецептора NMDA . Он также ингибирует рецептор AMPA и никотиновые рецепторы ацетилхолина и активирует определенные каналы K 2P .
Структура и склеивание
Треугольная структура циклопропана требует, чтобы валентные углы между углерод-углеродными ковалентными связями составляли 60 °. Молекула имеет симметрию молекулы D 3h . Помимо кольцевой деформации, молекула также имеет скручивающую деформацию из-за затменной конформации ее атомов водорода. Таким образом, связи между атомами углерода значительно слабее, чем в типичном алкане , что приводит к гораздо более высокой реакционной способности.
Связь между углеродными центрами обычно описывается в терминах изогнутых связей . В этой модели углерод-углеродные связи изогнуты наружу, так что межорбитальный угол составляет 104 °. Одно необычное последствие изогнутой связи состоит в том, что, хотя связи CC в циклопропане слабее, чем обычно, атомы углерода также расположены ближе друг к другу, чем в обычной алкановой связи: 151 пм против 153 пм (средняя алкеновая связь: 146 пм).
Делокализация шести электронов трех CC σ-связей циклопропана была дана как объяснение лишь немного большей деформации циклопропана («всего» 27,6 ккал / моль) по сравнению с циклобутаном (26,2 ккал / моль) с циклогексаном в качестве ссылки на E str. = 0 ккал / моль. Эта стабилизация называется σ-ароматичностью, в отличие от обычной π-ароматичности, которая, например, оказывает сильное стабилизирующее действие на бензол . Другие исследования не подтверждают роль σ-ароматичности в циклопропане и существование индуцированного кольцевого тока; такие исследования обеспечивают альтернативное объяснение энергетической стабилизации и аномального магнитного поведения циклопропана.
Синтез
Циклопропан сначала был получен посредством сочетания Вюрца , при котором 1,3-дибромпропан подвергался циклизации с использованием натрия . Выход этой реакции может быть улучшен за счет использования цинка в качестве дегалогенирующего агента и йодида натрия в качестве катализатора.
- BrCH 2 CH 2 CH 2 Br + 2 Na → (CH 2 ) 3 + 2 NaBr
Получение циклопропановых колец называется циклопропанированием .
Циклопропаны
 1-Аминоциклопропан-1-карбоновая кислота играет важную роль в биосинтезе растительного гормона этилена .
1-Аминоциклопропан-1-карбоновая кислота играет важную роль в биосинтезе растительного гормона этилена .
Производные циклопропана многочисленны. Многие биомолекулы и фармацевтические препараты имеют циклопропановое кольцо. Известным примером является аминоциклопропанкарбоновая кислота , которая является предшественником этилена , растительного гормона. В пиретроидах являются основой многих инсектицидов. Известно несколько циклопропановых жирных кислот .
Реакции
Из-за повышенного π-характера своих связей CC циклопропан в некоторых случаях может реагировать как алкен. Например , он подвергается hydrohalogenation с минеральными кислотами с получением линейный алкил галогениды. Замещенные циклопропаны также реагируют по правилу Марковникова . Замещенные циклопропаны могут окислительно присоединяться к переходным металлам в процессе, называемом C – C активацией .
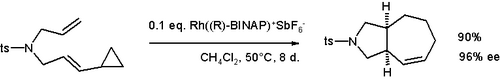
Циклопропильные группы, соседние с винильными группами, могут вступать в реакции расширения кольца . Примеры включают vinylcyclopropane перегруппировку и divinylcyclopropane-циклогептадиен перегруппировку . Эти реакционная способность может быть использовано , чтобы генерировать необычные циклические соединения, такие как циклобутеноны или бициклических виды , такие как циклогептно показано ниже.
Безопасность
Циклопропан легко воспламеняется. Однако, несмотря на свою энергию деформации, он не более взрывоопасен, чем другие алканы .
Смотрите также
- Тетраэдран содержит четыре конденсированных циклопропановых кольца, которые образуют грани тетраэдра.
- Пропеллан содержит три циклопропановых кольца, которые имеют одну центральную углерод-углеродную связь.
- Циклопропен
- Метиленциклопропан