Процесс Wacker - Wacker process
Процесс Wacker или процесс Hoechst-Wacker (названный в честь одноименных химических компаний) относится к окислению этилена до ацетальдегида в присутствии хлорида палладия (II) в качестве катализатора . Эта химическая реакция была одним из первых способов гомогенного катализа с применением палладиеорганической химии в промышленных масштабах.
История
Впервые о реакции Вакера сообщили Smidt et al.
Разработка химического процесса, ныне известного как процесс Wacker, началась в 1956 году в компании Wacker Chemie . В то время многие промышленные соединения производились из ацетилена , полученного из карбида кальция , - дорогостоящей и экологически вредной технологии. Строительство нового нефтеперерабатывающего завода в Кельне компанией Esso рядом с производственной площадкой Wacker в сочетании с осознанием того, что этилен будет более дешевым сырьем, побудило Wacker изучить возможности его использования. В рамках последовавших исследований реакция этилена и кислорода над палладием на угле в поисках оксида этилена неожиданно дала доказательства образования ацетальдегида (просто по запаху). Дальнейшие исследования превращения этилена в ацетальдегид привели к патенту 1957 года, описывающему газофазную реакцию с использованием гетерогенного катализатора. Тем временем Hoechst AG присоединилась к гонке и после подачи заявки на патент вынудила Wacker вступить в партнерство под названием Aldehyd GmbH . Гетерогенный процесс в конечном итоге потерпел неудачу из-за инактивации катализатора и был заменен гомогенной системой на водной основе, для которой пилотная установка была запущена в 1958 году. Проблемы с агрессивным раствором катализатора были решены путем принятия титана (недавно доступного для промышленного использования) в качестве конструкционного материала. для реакторов и насосов. Производственные предприятия вступили в строй в 1960 году.
Механизм реакции
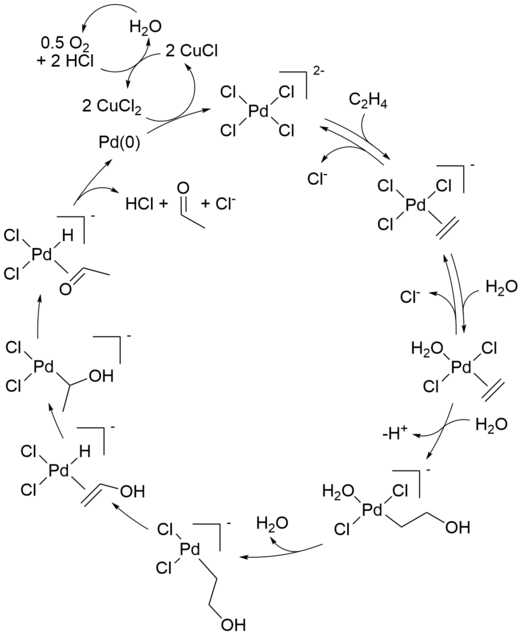
Механизм реакции промышленного процесса Ваккера (окисление олефинов через хлорид палладия (II)) привлекал большое внимание в течение нескольких десятилетий. Аспекты механизма все еще обсуждаются. Современная формулировка описана ниже:
Первоначальная стехиометрическая реакция была впервые описана Филлипсом. Чистую реакцию также можно описать следующим образом:
- [PdCl 4 ] 2 - + C 2 H 4 + H 2 O → CH 3 CHO + Pd + 2 HCl + 2 Cl -
За этой конверсией следуют реакции, в которых регенерируется катализатор Pd (II):
- Pd + 2 CuCl 2 + 2 Cl - → [PdCl 4 ] 2- + 2 CuCl
- 2 CuCl + 1/2O 2 + 2 HCl → 2 CuCl 2 + H 2 O
Расходуются только алкен и кислород. Без хлорида меди (II) в качестве окислителя металл Pd (0) (возникающий в результате отщепления бета-гидридом Pd (II) на последней стадии) выпадал бы в осадок, останавливая реакцию после одного цикла. Эта стехиометрическая реакция была открыта в 1894 году. Воздух, чистый кислород или ряд других реагентов могут затем окислить полученную смесь CuCl- хлорид обратно до CuCl 2 , позволяя циклу продолжаться.
Историко-механистические исследования
Ранние механистические исследования 1960-х гг. Выявили несколько ключевых моментов:
- В этой реакции не наблюдается эффектов обмена H / D. Эксперименты с использованием C 2 D 4 в воде генерируют CD 3 CDO, а эксперименты с C 2 H 4 в D 2 O генерируют CH 3 CHO. Таким образом, таутомеризация кето-енолов не является возможной механической стадией.
- Незначительный кинетический изотопный эффект с полностью дейтерированными реагентами (к H/k D= 1,07). Следовательно, предполагается, что перенос гидрида не является определяющим .
- Значительный конкурентный изотопный эффект с C 2 H 2 D 2 , (к H/k D= ~ 1,9), предполагает, что стадия определения скорости должна предшествовать образованию ацетальдегида.
- Высокие концентрации хлорида и хлорида меди (II) способствуют образованию нового продукта - хлоргидрина .
Многие механистические исследования процесса Ваккера были сосредоточены на пути образования связи CO, стадии гидроксипалладирования . Генри пришел к выводу, что скоординированный гидроксид атакует этиленовый лиганд по внутреннему (син-) пути. Позже стереохимические исследования Стилла с соавторами подтверждают наличие пути против присоединения, в соответствии с которым свободный гидроксид атакует этиленовый лиганд. Условия для экспериментов Стилле существенно отличаются от условий промышленного процесса. Другие исследования с использованием нормальных промышленных условий Ваккера (за исключением высоких концентраций хлорида и высоких концентраций хлорида меди) также дали продукты, которые предполагали, что нуклеофильная атака является реакцией против присоединения.
Кинетические исследования были проведены на изотопно замещенных аллиловых спиртах в стандартных промышленных условиях (с низкими концентрациями хлоридов) для изучения механизмов реакции. Эти результаты показали, что нуклеофильная атака - медленный процесс, в то время как предложенные механизмы, объясняющие более ранние стереохимические исследования, предполагали, что нуклеофильная атака - быстрый процесс.
Последующие стереохимические исследования показали, что оба пути возникают и зависят от концентраций хлоридов. Однако эти исследования также оспариваются, поскольку аллиловые спирты могут быть чувствительны к реакциям изомеризации, и различные стереоизомеры могут быть образованы из этих реакций, а не из стандартного процесса Ваккера.
Таким образом, экспериментальные данные, по-видимому, подтверждают, что син-присоединение происходит при низких реакционных концентрациях хлорида (<1 моль / л , в условиях промышленного процесса), в то время как анти-присоединение происходит при высоких реакционных концентрациях хлорида (> 3 моль / л), вероятно, из-за того, что ионы хлора насыщают катализатор и ингибируют механизм внутренней сферы. Однако точный путь и причина этого переключения путей до сих пор неизвестны.
Еще больше усложняют механизм процесса Ваккера вопросы о роли хлорида меди. Большинство теорий предполагало, что медь не играет роли в механизмах окисления олефинов. Тем не менее, эксперименты Штангла и Джира показали, что образование хлоргидрина зависит от концентрации хлорида меди. Работа Хосокавы и его коллег позволила получить кристаллизованный продукт, содержащий хлорид меди, что указывает на то, что он может играть небезопасную роль в окислении олефинов. И, наконец, исследование, проведенное с первых шагов Comas-Vives и соавт. с участием медного сокатализатора не обнаружено, что антидобавление является предпочтительным путем. Этот путь позже был подтвержден экспериментами Андерсона и Сигмана без содержания меди. Другой закон кинетической скорости без протонной зависимости был обнаружен в условиях отсутствия меди, что указывает на возможность того, что даже небольшие количества медных сокатализаторов могут играть небезопасную роль в этой химии. Хотя эти работы усложняют картину механизма процесса Ваккера, следует, вероятно, сделать вывод, что этот и связанный с ним химический состав могут быть чувствительны к условиям реакции, и могут быть задействованы несколько различных путей реакции.
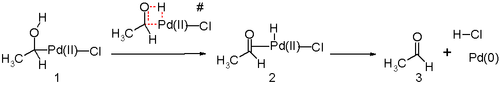
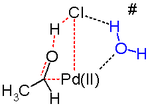
Другой ключевой шаг в процессе Wacker - это миграция водорода из кислорода в хлорид и образование двойной связи CO. Обычно считается, что на этом этапе происходит так называемое отщепление β-гидрида с циклическим четырехчленным переходным состоянием :
Исследования in silico доказывают, что переходное состояние для этой стадии реакции является неблагоприятным, и действует альтернативный механизм реакции восстановительного элиминирования . Предложенным стадиям реакции, вероятно, способствует молекула воды в растворе, действующая как катализатор.
Промышленный процесс
Для производства ацетальдегида используются два способа производства: одностадийный и двухстадийный.
Одноэтапный процесс
Этен и кислород одновременно пропускаются в реакционной башне при температуре около 130 ° C и 400 кПа. Катализатор представляет собой водный раствор PdCl 2 и CuCl 2 . Ацетальдегид очищают экстрактивной перегонкой с последующей фракционной перегонкой . Экстракционная дистилляция с водой удаляет легкие фракции, имеющие более низкие температуры кипения, чем у ацетальдегида ( хлорметан , хлорэтан и диоксид углерода ) в верхней части, в то время как вода и побочные продукты с более высокой температурой кипения, такие как уксусная кислота , кротоновый альдегид или хлорированные ацетальдегиды, удаляются вместе с ацетальдегидом. внизу. Из-за коррозионной природы катализатора реактор облицован кислотостойким керамическим материалом, а трубки изготовлены из титана .
Двухэтапный процесс
В двухстадийном процессе реакция и окисление осуществляются отдельно в трубчатых реакторах. В отличие от одностадийного процесса, вместо кислорода можно использовать воздух. Этилен пропускают через реактор вместе с катализатором при 105–110 ° C и 900–1000 кПа. Раствор катализатора, содержащий ацетальдегид, отделяют быстрой перегонкой . Катализатор окисляют в реакторе окисления при 1000 кПа с использованием воздуха в качестве окислительной среды. Окисленный раствор катализатора отделяют и отправляют обратно в реактор. Кислород из воздуха полностью расходуется, а отработанный воздух циркулирует как инертный газ. Смесь ацетальдегид - водяной пар предварительно концентрируется до 60–90% ацетальдегида за счет использования тепла реакции, а сброшенная вода возвращается в испарительную колонну для поддержания концентрации катализатора. Далее следует двухступенчатая перегонка сырого ацетальдегида. На первом этапе отделяются низкокипящие вещества, такие как хлорметан , хлорэтан и диоксид углерода . На второй стадии удаляются вода и высококипящие побочные продукты, такие как хлорированные ацетальдегиды и уксусная кислота , и ацетальдегид получается в чистом виде с головного погона. Из-за коррозионной природы катализатора оборудование, контактирующее с ним, покрыто титаном .
Как в одно-, так и в двухстадийных процессах выход ацетальдегида составляет около 95%, а производственные затраты практически одинаковы. Преимущество использования разбавленных газов в двухступенчатом методе уравновешивается более высокими инвестиционными затратами. Оба метода дают хлорированные углеводороды, хлорированные ацетальдегиды и уксусную кислоту в качестве побочных продуктов. Как правило, выбор метода зависит от сырьевых материалов и энергии, а также от доступности кислорода по разумной цене. В общем, 100 частей этена дают:
- 95 частей ацетальдегида
- 1,9 части хлорированных альдегидов
- 1,1 части непревращенного этена
- 0,8 части диоксида углерода
- 0,7 части уксусной кислоты
- 0,1 части хлорметана
- 0,1 части этилхлорида
- 0,3 части этана, метана, кротонового альдегида
и другие второстепенные побочные продукты
Окисление Цудзи-Ваккера
Появление Wacker Process стимулировало многие исследования полезности и применимости реакций к более сложным терминальным олефинам. Окисления Тсуджи-Wacker представляет собой палладий (II) , -catalyzed превращение таких олефинов в карбонильные соединения. Клемент и Селвиц были первыми, кто обнаружил, что использование водного ДМФА в качестве растворителя позволяет окислять 1-додецен до 2-додеканона, что решает проблему нерастворимости олефинов более высокого порядка в воде. Фэи отметил, что использование 3-метилсульфолана вместо ДМФА в качестве растворителя увеличивает выход окисления 3,3-диметилбут-1-ена. Два года спустя Цуджи применил условия Зельвица для селективного окисления концевых олефинов с множеством функциональных групп и продемонстрировал их полезность в синтезе сложных субстратов. Дальнейшее развитие реакции привело к появлению различных каталитических систем, направленных на селективность реакции, а также к внедрению межмолекулярного и внутримолекулярного окисления с нуклеофилами, не являющимися водными.
Региоселективность
Марковникова сложение
Окисление Цуджи-Ваккера окисляет концевой олефин до соответствующего метилкетона в условиях процесса Ваккера. Практически идентичный процессу Wacker Process, предлагаемый каталитический цикл (рис.1) начинается с комплексообразования PdCl 2 и двух хлорид-анионов с PdCl 4 , который затем подвергается последующей лигандной замене двух хлоридных лигандов на воду и алкен с образованием Pd (Cl 2 ) (H 2 O) (алкен) комплекс. Затем молекула воды региоселективно атакует олефин через механизм внешней сферы по марковниковской манере с образованием более термодинамически стабильного комплекса Pd (Cl 2 ) (OH) ( -CH 2 -CHOH-R). Диссоциация хлоридного лиганда до трехкоординатного палладиевого комплекса способствует удалению β-гидрида, затем последующая мигрирующая вставка 1,2-гидрида генерирует комплекс Pd (Cl 2 ) (OH) (-CHOHR-CH 3 ). При этом происходит отщепление β-гидрида с высвобождением кетона, а последующее восстановительное отщепление дает HCl, воду и палладий (0). Наконец, палладий (0) повторно окисляется до PdCl 2 двумя эквивалентами Cu (II) Cl 2 , который, в свою очередь, может повторно окисляться O 2 .
Окисление концевых олефинов обычно дает кетонный продукт Марковникова, однако в случаях, когда субстрат отдает предпочтение альдегиду (обсуждается ниже), для усиления региоселективности Марковникова можно использовать различные лиганды. Использование спартеина в качестве лиганда (рис. 2, А) способствует нуклеопалладации на концевом атоме углерода, чтобы минимизировать стерическое взаимодействие между комплексом палладия и субстратом. Хинокс-лигированный палладиевый катализатор используется для содействия образованию кетона, когда субстрат содержит направляющую группу (рис. 2, B). Когда такой субстрат связывается с Pd (Quinox) (OOtBu), этот комплекс координационно насыщается, что предотвращает связывание направляющей группы и приводит к образованию продукта Марковникова. Эффективность этого лиганда также объясняется его электронным свойством, когда анионный TBHP предпочитает связывать транс с оксазолином, а олефин координирует транс с хинолином.
Антимарковниковское дополнение
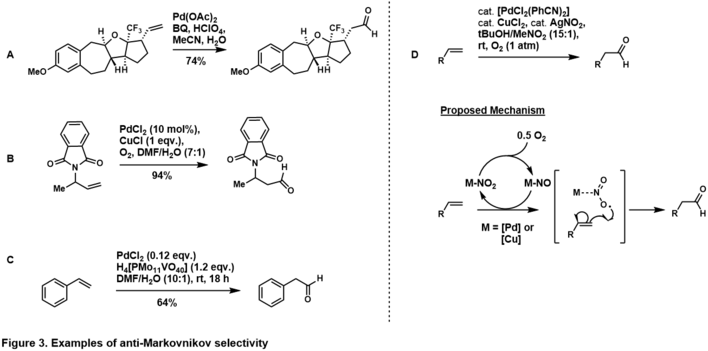
Селективность добавления антимарковникова к альдегиду может быть достигнута за счет использования встроенной стереоэлектроники подложки. Размещение направляющей группы в гомоаллильном (т.е. фиг. 3, A) и аллильном положении (т.е. фиг. 3, B) к концевому олефину способствует образованию антимарковниковского альдегидного продукта, что предполагает, что в каталитическом цикле направляющая группа хелатирует с комплекс палладия, такой, что вода атакует антимарковниковский углерод с образованием более термодинамически стабильного палладоцикла. Антимарковниковская селективность также наблюдается в стиренильных субстратах (т.е. рис. 3, C), предположительно через η 4 -палладий-стирольный комплекс после того, как вода атакует антимарковниковые. Дополнительные примеры контролируемого субстратом, анти-марковниковского окисления олефинов Цуджи-Ваккера приведены в обзорах Namboothiri, Feringa и Muzart.
Граббс и его сотрудники проложили путь к антимарковскому окислению стереоэлектронно несмещенных концевых олефинов с использованием системы палладий-нитрит (рис. 2, D). В его системе концевой олефин окислился до альдегида с высокой селективностью через путь контроля катализатора. Этот механизм изучается, однако данные свидетельствуют о том, что он проходит через нитритный радикал, добавляется к концевому углероду, чтобы произвести более термодинамически стабильный вторичный радикал. Граббс расширил эту методологию на более сложные, беспристрастные олефины.
Сфера
Нуклеофилы кислорода
Межмолекулярное окисление олефинов спиртами в качестве нуклеофилов обычно приводит к образованию кеталей , тогда как катализируемое палладием окисление олефинов карбоновыми кислотами в качестве нуклеофилов образует виниловые или аллильные карбоксилаты . В случае диолов в их реакциях с алкенами обычно образуются кетали, тогда как реакции олефинов, содержащих электроноакцепторные группы, имеют тенденцию к образованию ацеталей .
Катализируемое палладием межмолекулярное окисление диенов с карбоновыми кислотами и спиртами в качестве доноров дает продукты 1,4-присоединения . В случае циклогексадиена (рис. 4, А) Бэквалл обнаружил, что стереохимический исход продукта зависит от концентрации LiCl. Эта реакция протекает сначала путем образования комплекса Pd (OAc) (бензохинон) (аллил) путем антинуклеопалладирования диена с ацетатом в качестве нуклеофила. Отсутствие LiCl вызывает восстановительное отщепление внутренней сферы, что приводит к стереохимии транс-ацетата с образованием транс-1,4-аддукта. Присутствие LiCl замещает ацетат хлоридом из-за его более высокой аффинности связывания, что заставляет внешнюю сферу ацетат атаковать палладий и обеспечивает цис-ацетатную стереохимию с образованием цис-1,4-аддукта. Внутримолекулярная окислительная циклизация: 2- (2-циклогексенил) фенол циклизуется до соответствующего дигидробензофурана (рис. 4, B); 1-циклогексадиен-уксусная кислота в присутствии уксусной кислоты циклизуется с образованием соответствующего аддукта лактонацетат 1,4 (рис. 4, C) с цис- и транс- селективностью, контролируемой присутствием LiCl.
Нуклеофилы азота
Окислительное аминирование олефинов обычно проводят с амидами или имидами ; Считается, что амины протонируются кислой средой или связывают металлический центр слишком сильно, чтобы позволить каталитическому химическому процессу протекать. Было обнаружено, что эти нуклеофилы азота компетентны как в межмолекулярных, так и в внутримолекулярных реакциях, показаны некоторые примеры (Рисунок 5, A, B).