Пентацен - Pentacene
|
|
|
|
|
| Имена | |
|---|---|
|
Предпочтительное название IUPAC
Пентацен |
|
| Другие имена
2,3: 6,7-Дибензантрацен
Бензо [b] нафтацен Дибенз [b, i] антрацен NSC 90784 лин-Дибензантрацен лин-Нафтоантрацен |
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| 1912418 | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard |
100,004,722 |
| Номер ЕС | |
| 733903 | |
|
PubChem CID
|
|
| UNII | |
|
Панель управления CompTox ( EPA )
|
|
|
|
|
|
| Характеристики | |
| C 22 H 14 | |
| Молярная масса | 278,354 г · моль -1 |
| Появление | Темно-синий порошок |
| Плотность | 1,3 г см −3 |
| Температура плавления | > 300 ° C (572 ° F, 573 K) сублимируется при 372 ° C |
| Точка кипения | 40–43 ° C (104–109 ° F, 313–316 К) при 0,15 торр |
| -205,4 × 10 −6 см 3 моль −1 | |
| Состав | |
| Триклиник | |
| П-1 | |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
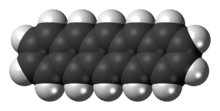
Пентацен представляет собой полициклический ароматический углеводород, состоящий из пяти линейно конденсированных бензольных колец. Это сильно сопряженное соединение представляет собой органический полупроводник . Соединение генерирует экситоны при поглощении ультрафиолетового ( УФ ) или видимого света ; это делает его очень чувствительным к окислению. По этой причине это соединение, представляющее собой порошок пурпурного цвета, медленно разлагается под воздействием воздуха и света.
Структурно пентацен представляет собой один из линейных аценов , предыдущий - тетрацен (четыре конденсированных бензольных кольца), а следующий - гексацен (шесть конденсированных бензольных колец). В августе 2009 года группа исследователей из IBM опубликовала экспериментальные результаты визуализации одиночной молекулы пентацена с помощью атомно-силового микроскопа . В июле 2011 года они использовали модификацию сканирующей туннельной микроскопии для экспериментального определения формы самых высоких и самых низких незанятых молекулярных орбиталей .
В 2012 г. п- терфенил, активированный пентаценом, показал свою эффективность в качестве усилительной среды для мазера при комнатной температуре .
Синтез
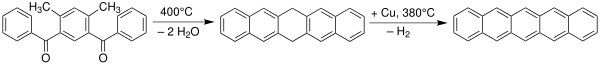
Пентацен был впервые синтезирован в 1912 году британскими химиками Уильямом Хобсоном Миллсом и Милдред Мэй Гостлинг . Классический метод синтеза пентацена - реакция Эльбса .
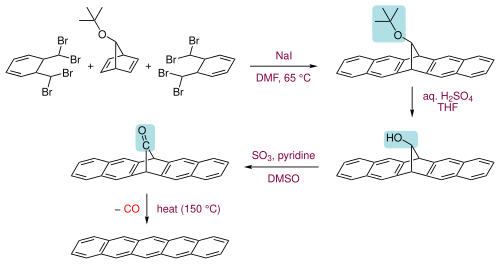
Пентацены можно также получить экструзией небольшого летучего компонента ( монооксида углерода ) из подходящего предшественника при 150 ° C.
Сам предшественник получают в три этапа из двух молекул α, α, α ', α'-тетрабром- о- ксилола с 7- трет- бутоксибицикло [2.2.1] гепта-2,5-диеном при первом нагревании с иодид натрия в диметилформамиде для прохождения серии реакций отщепления и реакций Дильса-Альдера с образованием кольцевой системы, затем гидролиз трет- бутоксигруппы до спирта с последующим ее окислением до кетона .
Сообщается, что продукт имеет некоторую растворимость в хлороформе и поэтому его можно наносить методом центрифугирования . Пентацен растворим в горячих хлорированных бензолах, таких как 1,2,4-трихлорбензол , из которых его можно перекристаллизовать с образованием тромбоцитов.
Производные пентацена
Мономерные производные пентацена
6,13-Замещенные пентацены доступны через пентаценхинон путем реакции с арильным или алкинилнуклеофилом (например, реагентами Гриньяра или литийорганическими реагентами) с последующей восстановительной ароматизацией. Другой метод основан на гомологизации диинов переходными металлами (через цирконциклопентадиены). Функционализация пентацена позволила контролировать твердотельную упаковку этого хромофора. Выбор заместителей (как размер, так и расположение замещения в пентацене) влияет на твердотельную упаковку и может использоваться для контроля того, принимает ли соединение 1-мерный или 2-мерный кофациальный пи-стэкинг в твердом состоянии, так как в отличие от набивки «в елочку», наблюдаемой для пентацена.
Хотя структура пентацена напоминает структуру других ароматических соединений, таких как антрацен , его ароматические свойства плохо определены; как таковой пентацен и его производные являются предметом многочисленных исследований.
Таутомерное химическое равновесие существует между 6-метиленом-6,13-dihydropentacene и 6-methylpentacene.
Это равновесие полностью в пользу метиленового соединения. Только при нагревании раствора соединения до 200 ° C образуется небольшое количество пентацена, о чем свидетельствует появление красно-фиолетовой окраски. Согласно одному исследованию, механизм реакции для этого равновесия основан не на внутримолекулярном 1,5-гидридном сдвиге , а на бимолекулярной свободнорадикальной миграции водорода. Напротив, изотолуолы с таким же центральным химическим мотивом легко ароматизируются.
Пентацен реагирует с элементарной серой в 1,2,4-трихлорбензоле с образованием соединения гексатиапентацена . Рентгеновская кристаллография показывает, что все длины связей углерод-сера примерно равны (170 мкм ); из этого следует, что резонансные структуры B и C с полным разделением зарядов более значимы, чем структура A.
В кристаллической фазе молекулы демонстрируют ароматические стэкинг-взаимодействия , в результате чего расстояние между некоторыми атомами серы на соседних молекулах может стать меньше (337 пм), чем сумма двух радиусов Ван-дер-Ваальса (180 пм).
Как и родственный тетратиафульвален , это соединение изучается в области органических полупроводников .
Ацены могут выглядеть как плоские и жесткие молекулы, но на самом деле они могут быть очень искажены. Пентацен, изображенный ниже:
имеет скрутку от конца до конца 144 ° и стерически стабилизирован шестью фенильными группами. Соединение может быть разделено на два его энантиомера с необычно высоким сообщенным оптическим вращением 7400 °, хотя рацемизация происходит с химическим периодом полураспада 9 часов.
Олигомеры и полимеры пентацена
Олигомеры и полимеры на основе пентацена были исследованы как синтетически, так и в настройках приложений устройства. Полимерные светоизлучающие диоды ( PLED ) были сконструированы с использованием сопряженных сополимеров ( 1a – b ), содержащих флуорен и пентацен. Несколько других сопряженных полимеров пентацена ( 2a-b и 3 ) были реализованы на основе реакций сочетания Соногашира и Сузуки мономера дибромпентацена. Несопряженные полимеры на основе пентацена были синтезированы путем этерификации мономера пентацендиола с бис-хлорангидридами с образованием полимеров 4a – b .

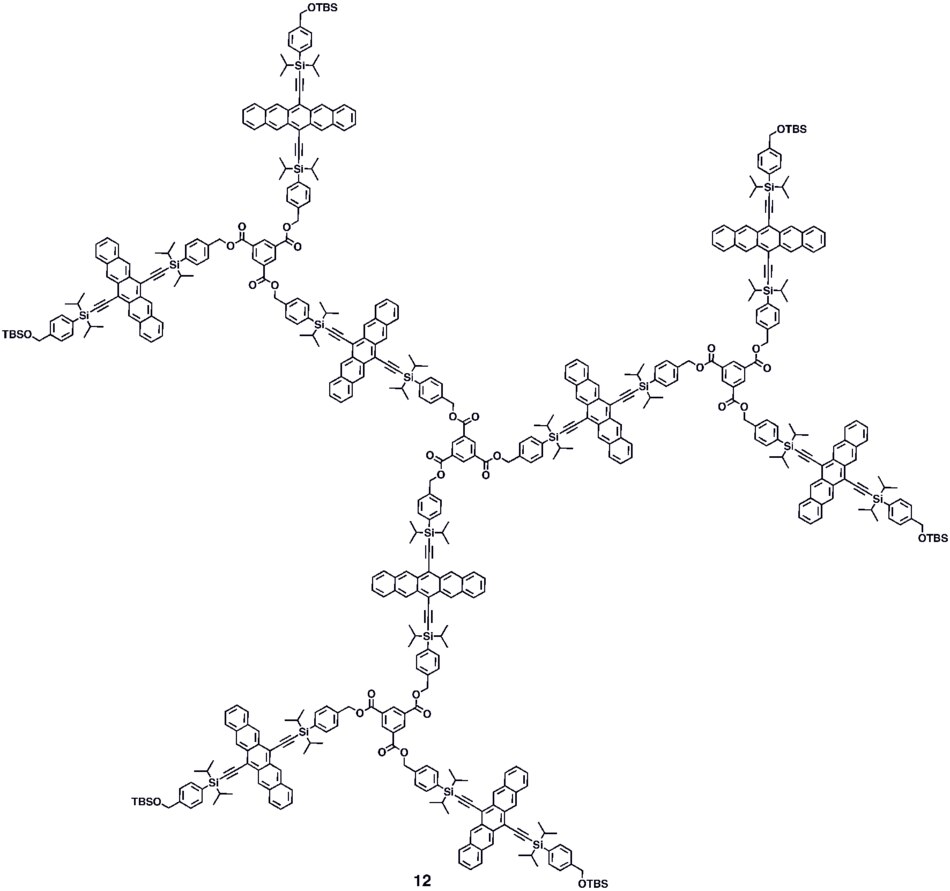
Для образования конъюгированных олигомеров пентацена 5a-c использовались различные синтетические стратегии, включая процедуру образования связи «один горшок-четыре», которая обеспечила перерабатываемый в растворе сопряженный димер пентацена ( 5c ), который показал усиление фотопроводимости> 10, что помещает его характеристики в пределах того же порядка величины, что и термически напыленные пленки нефункционализированного пентацена, которые показали коэффициент фотопроводимости> 16 при использовании аналогичных методов измерения. Сообщается о модульном методе синтеза конъюгированных ди-, три- и тетрамеров пентацена ( 6-8 ), который основан на реакциях гомо- и кросс-сочетания устойчивых промежуточных продуктов дегидропентацена. Были синтезированы неконъюгированные олигомеры 9–10 на основе пентацена, включая дендримеры 9–10, содержащие до 9 фрагментов пентацена на молекулу с молярной поглощающей способностью для наиболее интенсивного поглощения> 2 000 000 М -1 • см -1 . Было показано, что дендримеры 11–12 обладают улучшенными характеристиками в устройствах по сравнению с аналогичными полимерами на основе пентацена 4a – b в контексте фотодетекторов.
Материаловедение
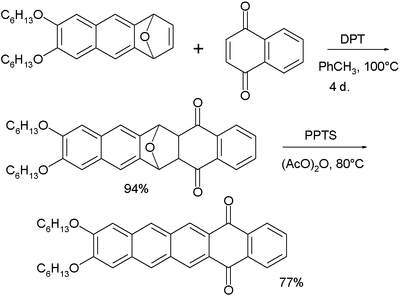
Пентацены были исследованы как потенциальные дихроичные красители . Показанный ниже пентаценохинон является флуоресцентным, и при смешивании со смесью жидких кристаллов E7 достигается дихроичное соотношение 8. Более длинные ацены лучше выравниваются в нематической жидкокристаллической фазе.
В сочетании с бакминстерфуллереном пентацен используется при разработке прототипов органических фотоэлектрических элементов. Органические фотоэлектрические элементы дешевле и гибче, чем традиционные неорганические элементы, которые потенциально могут открыть двери для солнечных элементов на новые рынки.
Пентацен - популярный выбор для исследований органических тонкопленочных транзисторов и OFET , поскольку он является одной из наиболее тщательно изученных сопряженных органических молекул с высоким потенциалом применения благодаря подвижности дырок в OFET до 5,5 см 2 / (В · с). , что превосходит аморфный кремний.
Пентацен, как и другие органические проводники, подвержен быстрому окислению на воздухе, что исключает коммерческое использование. Если пентацен предварительно окислен, пентацен-хинон является потенциальным изолятором затвора, тогда подвижность может приблизиться к подвижности рубрена - наиболее подвижного органического полупроводника, а именно 40 см 2 / (В · с). Этот метод окисления пентацена сродни окислению кремния, используемому в кремниевой электронике.
Смотрите также
использованная литература
внешние ссылки
- факты о пентацене , полученные 17 апреля 2006 г.
- Органические транзисторы улучшаются с возрастом , New Scientist, 2 декабря 2007 г.
- Pentacene Imaged , изображения IBM Pentacene, первая молекула, детально отображенная 29 августа 2009 г.