Нитрозилхлорид - Nitrosyl chloride
|
|

|
|
| Имена | |
|---|---|
|
Название ИЮПАК
Нитрозилхлорид
|
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.018.430 |
| Номер ЕС | |
| Номер E | E919 (глазури, ...) |
| MeSH | нитрозил + хлорид |
|
PubChem CID
|
|
| Номер RTECS | |
| UNII | |
| Номер ООН | 1069 |
|
Панель управления CompTox ( EPA )
|
|
|
|
|
|
| Характеристики | |
| NOCl | |
| Молярная масса | 65,459 г моль -1 |
| Появление | Желтый газ |
| Плотность | 2,872 мг мл -1 |
| Температура плавления | -59,4 ° С (-74,9 ° F, 213,8 К) |
| Точка кипения | -5,55 ° С (22,01 ° F, 267,60 К) |
| Реагирует | |
| Состав | |
| Двугранный, двугранный | |
| Гибридизация | sp 2 at N |
| 1,90 Д | |
| Термохимия | |
|
Стандартная мольная
энтропия ( S |
261,68 Дж -1 моль -1 |
|
Std энтальпия
формации (Δ F H ⦵ 298 ) |
51,71 кДж моль -1 |
| Опасности | |
| Паспорт безопасности | inchem.org |
| NFPA 704 (огненный алмаз) | |
| Родственные соединения | |
|
Родственные соединения
|
|
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
Нитрозилхлорид - это химическое соединение с формулой NOCl. Это желтый газ, который обычно встречается в составе царской водки , смеси 3 частей концентрированной соляной кислоты и 1 части концентрированной азотной кислоты . Это сильный электрофил и окислитель . Иногда его называют реактивом Тильдена.
Структура и синтез
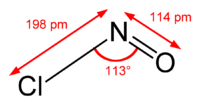
Молекула изогнута. Двойная связь существует между N и O (расстояние = 1,16 Å) и одинарной связью между N и Cl (расстояние = 1,96 Å). Угол O = N – Cl равен 113 °.
Производство
Нитрозилхлорид можно производить разными способами.
- Соединение нитрозилсерной кислоты и HCl дает соединение. Этот метод используется в промышленных масштабах.
- HCl + NOHSO 4 → H 2 SO 4 + NOCl
- Более удобный лабораторный метод включает (обратимое) обезвоживание азотистой кислоты HCl.
- HNO 2 + HCl → H 2 O + NOCl
- Путем прямого сочетания хлора и оксида азота ; Эта реакция меняется на противоположную при температуре выше 100 ° C.
- Cl 2 + 2 NO → 2 NOCl
- При восстановлении диоксида азота хлористым водородом:
- 2NO 2 + 4 HCl → 2NOCl + 2H 2 O + Cl 2
Встречаемость в царской водке
NOCl также образуется в результате комбинации соляной и азотной кислот в соответствии со следующей реакцией:
- HNO 3 + 3 HCl → 2 [Cl] + 2 H 2 O + NOCl
В азотной кислоте NOCl легко окисляется до диоксида азота . Присутствие NOCl в царской водке было описано Эдмундом Дэви в 1831 году.
Реакции
NOCl в большинстве своих реакций ведет себя как электрофил и окислитель. С галогенидными акцепторами, например пентахлоридом сурьмы , превращается в соли нитрозония :
- NOCl + SbCl 5 → [NO] + [SbCl 6 ] -
В родственной реакции серная кислота дает нитрозилсерную кислоту , смешанный ангидрид азотистой и серной кислоты:
- ClNO + H 2 SO 4 → ONHSO 4 + HCl
NOCl реагирует с тиоцианатом серебра с образованием хлорида серебра и псевдогалогеннитрозилтиоцианата :
- ClNO + AgSCN → AgCl + ONSCN
Точно так же он реагирует с цианидом серебра с образованием цианида нитрозила .
Нитрозилхлорид используется для получения нитрозильных комплексов металлов . С гексакарбонилом молибдена NOCl дает динитрозилдихлоридный комплекс:
- Mo (CO) 6 + 2 NOCl → MoCl 2 (NO) 2 + 6 CO
Растворяет платину:
- Pt + 6 NOCl → (NO + ) 2 [PtCl 6 ] 2- + 4 NO
Приложения в органическом синтезе
Помимо своей роли в производстве капролактама, NOCl находит и другие применения в органическом синтезе . Он добавляется к алкенам с образованием α- хлороксимов . Добавление NOCl следует правилу Марковникова . Кетены также добавляют NOCl, давая нитрозильные производные:
- H 2 C = C = O + NOCl → ONCH 2 C (O) Cl
Эпоксиды реагируют с NOCl с образованием α-хлорнитритоалкильных производных. В случае пропиленоксида добавление протекает с высокой региохимией:
Он превращает амиды в N -нитрозопроизводные. NOCl превращает некоторые циклические амины в алкены. Например, азиридин реагирует с NOCl с образованием этена , закиси азота и хлористого водорода .
Промышленное применение
NOCl и циклогексан фотохимически реагируют с образованием гидрохлорида циклогексаноноксима . Этот процесс использует тенденцию NOCl подвергаться фотодиссоциации на радикалы NO и Cl. Оксид превращается в капролактам , предшественник нейлона-6 .
Безопасность
Нитрозилхлорид очень токсичен и раздражает легкие, глаза и кожу.
использованная литература
внешние ссылки
-
 СМИ, связанные с нитрозилхлоридом на Викискладе?
СМИ, связанные с нитрозилхлоридом на Викискладе?


