Нирапариб - Niraparib
 | |
| Клинические данные | |
|---|---|
| Произношение |
/ П ɪ г æ р ə г ɪ б / nih- РАП -uh-ребро |
| Торговые наименования | Zejula |
| Другие имена | МК-4827 |
| AHFS / Drugs.com | Монография |
| MedlinePlus | a617007 |
| Данные лицензии | |
Категория беременности |
|
| Пути администрирования |
Устно |
| Код УВД | |
| Легальное положение | |
| Легальное положение | |
| Фармакокинетические данные | |
| Биодоступность | 73% |
| Связывание с белками | 83% |
| Метаболизм | Карбоксилэстеразы |
| Метаболиты | M1 ( карбоновая кислота ) |
| Ликвидация Период полураспада | 36 часов |
| Экскреция | 48% мочи, 29% фекалий |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| Панель управления CompTox ( EPA ) | |
| ECHA InfoCard |
100.210.548 |
| Химические и физические данные | |
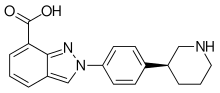
| Формула | C 19 H 20 N 4 O |
| Молярная масса | 320,396 г · моль -1 |
| 3D модель ( JSmol ) | |
| Растворимость в воде | 0,7–1,1 |
| |
| |
Нирапариб , продаваемый под торговой маркой Zejula , представляет собой противораковое лекарство, используемое для лечения эпителиального рака яичников, маточных труб или первичного рака брюшины. Принимается внутрь .
Наиболее частые побочные эффекты включают тошноту (плохое самочувствие), тромбоцитопению (низкий уровень тромбоцитов), усталость и слабость, анемию (низкий уровень эритроцитов), запор , рвоту , боль в животе, нейтропению (низкий уровень нейтрофилов, тип лейкоцитов), бессонница ( нарушение сна), головная боль, отсутствие аппетита, диарея , одышка (затрудненное дыхание), гипертония (высокое кровяное давление), боль в спине, головокружение, кашель, боль в суставах, приливы и снижение белые кровяные клетки.
Нирапариб был одобрен для медицинского применения в США и Европейском союзе в 2017 году.
Медицинское использование
Нирапариб показан для поддерживающего лечения взрослых с рецидивирующим эпителиальным раком яичников , маточной трубы или первичным раком брюшины, которые находятся в полном или частичном ответе на химиотерапию на основе платины .
В октябре 2019 года показания к применению нирапариба были расширены, чтобы включить людей с распространенным раком яичников, маточной трубы или первичным раком брюшины, получавших три или более предыдущих схем химиотерапии, и чей рак связан с положительным статусом на основе гомологичной рекомбинации (HRD). HRD определяется либо вредоносной, либо предполагаемой вредной мутацией BRCA, либо геномной нестабильностью у пациентов с прогрессированием заболевания более шести месяцев после ответа на последнюю химиотерапию на основе платины.
В апреле 2020 года показания для нирапариба были расширены и теперь включают поддерживающее лечение взрослых с запущенным эпителиальным раком яичников, маточной трубы или первичным раком брюшины, которые находятся в полном или частичном ответе на химиотерапию на основе платины первой линии.
В Европейском союзе нирапариб показан: в качестве монотерапии для поддерживающего лечения взрослых с развитым эпителиальным (стадия III и IV по FIGO) высокой степенью злокачественности яичников, маточной трубы или первичным раком брюшины, у которых наблюдается ответ (полный или частичный) после завершения лечения. химиотерапия на основе платины первой линии; и в качестве монотерапии для поддерживающего лечения взрослых с чувствительным к платине рецидивом тяжелого серозного эпителия яичника, маточной трубы или первичным раком брюшины, которые находятся в ответе (полном или частичном) на химиотерапию на основе платины.
Противопоказания.
В информации о назначении противопоказаний нет.
Побочные эффекты
Наиболее частыми побочными эффектами в исследованиях были низкое количество клеток крови, а именно тромбоцитопения (у 61% пациентов, тяжелая у 29%), анемия (у 50%, тяжелая у 25%) и нейтропения (у 30%, тяжелая у 20%). ). Другие побочные эффекты, в основном от легких до умеренных, включали тошноту , усталость и запор . В исследовании, продолжавшемся более 250 дней (в среднем ), 15% пациентов были вынуждены навсегда прекратить прием нирапариба из-за побочных эффектов.
Взаимодействия
Исследования клинического взаимодействия не проводились. Потенциал взаимодействия с другими лекарственными средствами невелик, поскольку нирапариб и его основной метаболит M1 не взаимодействуют в значительной степени с какими-либо важными ферментами печени цитохрома P450 in vitro . Нирапариб, но не M1, транспортируется с помощью P-гликопротеина и BCRP , но существенно не ингибирует их. Ни нирапариб, ни M1 существенно не взаимодействуют с какими-либо другими важными белками-переносчиками.
Фармакология
Механизм действия
Нирапариб является ингибитором ферментов PARP1 и PARP2 .
Фармакокинетика.
73% принятого внутрь нирапариба всасывается в кишечнике и достигает максимальной концентрации в плазме крови примерно через три часа, независимо от приема пищи. В кровотоке 83% вещества связывается с белками плазмы . Он инактивируется карбоксилэстеразами до основного метаболита M1, производного карбоновой кислоты , который впоследствии глюкуронидируется .
Средний период полувыведения составляет 36 часов. 47,5% вещества обнаруживается в моче и 38,8% в кале. Неметаболизированный нирапариб составляет 11% в моче и 19% в кале.
Химия
Препарат используется в форме моногидрата тозилата нирапариба , который представляет собой негигроскопичные кристаллы от белого до желтовато -белого цвета.
Исследования
Исследование 2012 года на клеточной линии показало, что ингибиторы PARP проявляют цитотоксические эффекты, основанные не только на их ферментативном ингибировании PARP, но и на их захвате PARP на поврежденной ДНК, и сила этой улавливающей активности была упорядочена: нирапариб >> олапариб >> велипариб .
История
Niraparib получил быстрое обозначение следа в США пищевых продуктов и медикаментов (FDA), и Tesaro представила новое применение препарата в 2016 году был утвержден 27 марта 2017 года в США, а также одобрен в Европейском Союзе 16 ноября 2017 года.
В исследовании с участием 553 пациентов выживаемость без прогрессирования (ВБП) для пациентов с вредной или предполагаемой вредной мутацией BRCA в зародышевой линии составила 21,0 месяца при терапии нирапарибом по сравнению с 5,5 месяцами в группе плацебо . Пациенты без такой мутации имели ВБП 9,3 месяца в группе нирапариба по сравнению с 3,9 месяца в группе плацебо.
США пищевых продуктов и медикаментов (FDA) удовлетворил заявки на niraparib кратчайшем пути , приоритетного рассмотрения , прорыв терапии и бесхозных наркотиков обозначения.
использованная литература
внешние ссылки
- «Нирапариб» . Информационный портал о наркотиках . Национальная медицинская библиотека США.
- «Тозилат нирапариба» . Информационный портал о наркотиках . Национальная медицинская библиотека США.
- «Моногидрат тозилата нирапариба» . Словарь лекарств NCI . Национальный институт рака.
- «Моногидрат тозилата нирапариба» . Национальный институт рака . 14 апреля 2017.
