MECP2 - MECP2
MECP2 ( метил-CpG-связывающий белок 2 ) представляет собой ген , кодирующий белок MECP2. MECP2, по-видимому, необходим для нормальной функции нервных клеток . Этот белок особенно важен для зрелых нервных клеток, где он присутствует в больших количествах. Белок MECP2, вероятно, участвует в выключении («подавлении» или « подавлении ») нескольких других генов. Это препятствует тому, чтобы гены вырабатывали белки, когда они не нужны. Недавние исследования показали, что MECP2 может также активировать другие гены. Ген MECP2 расположен на длинном (q) плече Х-хромосомы в полосе 28 («Xq28»), от пары оснований 152 808 110 до пары оснований 152 878 611.
MECP2 - важный считыватель метилирования ДНК. Его метил-CpG-связывающий домен (MBD) распознает и связывает области 5-мС . MECP2 является X-связанным и подвергается X-инактивации . Мутации гена MECP2 являются причиной большинства случаев синдрома Ретта , прогрессирующего неврологического расстройства развития и одной из наиболее частых причин когнитивной инвалидности у женщин.
Функция
Белок MECP2 обнаружен во всех клетках организма, включая мозг , и действует как репрессор и активатор транскрипции, в зависимости от контекста. Однако идея о том, что MECP2 действует как активатор, относительно нова и остается спорной. В головном мозге он обнаруживается в высоких концентрациях в нейронах и связан с созреванием центральной нервной системы (ЦНС) и формированием синаптических контактов .
Механизм действия
Белок связывает MeCP2 к формам ДНК , которые были метилированными . Затем белок MeCP2 взаимодействует с другими белками, образуя комплекс, который выключает ген. MeCP2 предпочитает связываться с сайтами генома с химическим изменением цитозина (C), когда он встречается в определенной последовательности ДНК, « CpG ». Это форма метилирования ДНК . Многие гены имеют CpG-островки , которые часто встречаются в начале гена. MECP2 не связывается с этими островками в большинстве случаев, поскольку они не метилированы. Выражение нескольких генов может регулироваться путем метилирования их островов CpG и MECP2 может играть определенную роль в подгруппе из них. Исследователи еще не определили, какие гены нацелены на белок MeCP2, но такие гены, вероятно, важны для нормальной функции центральной нервной системы. Однако первое крупномасштабное картирование сайтов связывания MECP2 в нейронах показало, что только 6% сайтов связывания находятся в островках CpG, и что 63% промоторов, связанных с MECP2, активно экспрессируются и только 6% сильно метилированы, что указывает на то, что Основная функция MECP2 - это нечто иное, чем подавление метилированных промоторов.
После связывания MeCP2 будет конденсировать структуру хроматина , образовывать комплекс с гистоновыми деацетилазами (HDAC) или напрямую блокировать факторы транскрипции . Более поздние исследования продемонстрировали, что MeCP2 может также функционировать как активатор транскрипции, рекрутируя фактор транскрипции CREB1 . Это было неожиданным открытием, которое предполагает, что MeCP2 является ключевым регулятором транскрипции с потенциально двойной ролью в экспрессии генов. Фактически, большинство генов, которые регулируются MeCP2, по-видимому, активируются, а не подавляются. Однако остается спорным, регулирует ли MeCP2 эти гены напрямую или эти изменения имеют вторичный характер. Дальнейшие исследования показали, что в некоторых случаях MeCP2 может напрямую связываться с неметилированной ДНК. MeCP2 участвует в регуляции импринтированных генов и локусов, которые включают UBE3A и DLX5 .
Сниженная экспрессия MECP2 в Mecp2 +/- нейральных стволовых клетках вызывает усиление старения , нарушение пролиферативной способности и накопление неисправленных повреждений ДНК . После обработки клеток Mecp2 +/- любым из трех различных агентов, повреждающих ДНК, клетки накапливали больше повреждений ДНК и были более склонны к гибели клеток, чем контрольные клетки. Был сделан вывод, что снижение экспрессии MECP2 вызывает снижение способности репарации ДНК, и это, вероятно, способствует неврологическому спаду.
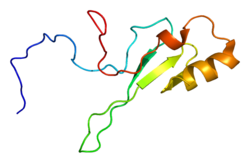
Состав
MECP2 является частью семейства белков метил-CpG-связывающих доменов (MBD), но обладает собственными уникальными различиями, которые помогают выделить его из группы. Он имеет два функциональных домена:
- метил- цитозин -связывающий домен (ММД) , состоящий из 85 аминокислот ; а также
- домен репрессии транскрипции (TRD), состоящий из 104 аминокислот
Домен MBD образует клин и прикрепляется к метилированным сайтам CpG на цепях ДНК. Затем область TRD реагирует с SIN3A, рекрутируя гистоновые деацетилазы (HDAC). Есть также необычные повторяющиеся последовательности, обнаруженные на карбоксильном конце. Эта область тесно связана с семейством головок вилки на аминокислотном уровне.
Роль в болезни
Роль MECP2 в заболевании в первую очередь связана либо с потерей функции (недостаточной экспрессией) гена MECP2, как при синдроме Ретта, либо с усилением функции (сверхэкспрессией), как при синдроме дупликации MECP2 . Многие мутации были связаны с потерей экспрессии гена MECP2 и были идентифицированы у пациентов с синдромом Ретта. Эти мутации включают изменения одиночных пар оснований ДНК ( SNP ), вставки или делеции ДНК в гене MECP2 , а также изменения, влияющие на то, как информация гена преобразуется в белок ( сплайсинг РНК ). Мутации в гене изменяют структуру белка MeCP2 или приводят к уменьшению количества белка. В результате белок не может связываться с ДНК или включать или выключать другие гены. Гены, которые обычно репрессируются MeCP2, остаются активными, когда их продукты не нужны. Другие гены, которые обычно активируются MeCP2, остаются неактивными, что приводит к недостатку генного продукта. Этот дефект, вероятно, нарушает нормальное функционирование нервных клеток, что приводит к появлению признаков и симптомов синдрома Ретта.
Синдром Ретта в основном встречается у девочек с распространенностью примерно у 1 из 10 000. Пациенты рождаются с очень трудно обнаруживаемыми признаками расстройства, но примерно через шесть месяцев или полтора года речевые и двигательные функции начинают снижаться. Далее следуют судороги , задержка роста, когнитивные и двигательные нарушения. Локус MECP2 сцеплен с Х-хромосомой, и аллели, вызывающие заболевание, являются доминирующими . Из-за того, что он распространен у женщин, он был связан с мужской летальностью или с преимущественной передачей через отцовскую Х-хромосому; тем не менее, в редких случаях некоторые мужчины также могут быть поражены синдромом Ретта. Мужчины с дупликациями генов MECP-2 в локусе Xq28 также подвержены риску рецидивов инфекций и менингита в младенчестве.
Мутации в гене MECP2 также были идентифицированы у людей с несколькими другими заболеваниями, влияющими на центральную нервную систему. Например, мутации MECP2 связаны с некоторыми случаями от умеренной до тяжелой Х-связанной умственной отсталости. Мутации в гене также были обнаружены у мужчин с тяжелой дисфункцией головного мозга ( неонатальная энцефалопатия ), которые доживают до раннего детства. Кроме того, у нескольких людей с признаками как синдрома Ретта, так и синдрома Ангельмана (состояние, характеризующееся умственной отсталостью, проблемами с движением и неуместным смехом и возбудимостью) есть мутации в гене MECP2. Наконец, мутации MECP2 или изменения активности гена были зарегистрированы в некоторых случаях аутизма (нарушение развития, которое влияет на общение и социальное взаимодействие).
В более поздних исследованиях сообщается о генетическом полиморфизме генов MeCP2 у пациентов с системной красной волчанкой (СКВ). СКВ - системное аутоиммунное заболевание, которое может поражать несколько органов. О полиморфизме MeCP2 до сих пор сообщалось у пациентов с волчанкой европейского происхождения и азиатской волчанки.
Генетическая потеря MECP2 была идентифицирована как изменение свойств клеток в locus ceruleus - исключительном источнике норадренергической иннервации коры головного мозга и гиппокампа .
Исследователи пришли к выводу, что «поскольку эти нейроны являются основным источником норадреналина в стволе и переднем мозге и участвуют в регуляции различных функций, нарушенных при синдроме Ретта, таких как дыхание и познание, мы предполагаем, что голубое пятно является критическим местом в потеря MECP2 приводит к дисфункции ЦНС ».
Интерактивная карта проезда
Нажмите на гены, белки и метаболиты ниже, чтобы просмотреть статьи по теме.
Взаимодействия
Было показано, что MECP2 взаимодействует с белком SKI и корепрессором 1 ядерного рецептора . Считается, что в нейрональных клетках мРНК MECP2 взаимодействует с miR-132 , что подавляет экспрессию белка. Это является частью гомеостатического механизма, который может регулировать уровни MECP2 в головном мозге.
MeCP2 и гормоны
MeCP2 в развивающемся мозге крысы регулирует важное социальное развитие сексуально диморфным образом. Уровни MeCP2 различаются между самцами и самками в развивающемся головном мозге крысы через 24 часа после рождения в пределах миндалины и гипоталамуса , но эта разница больше не наблюдается через 10 дней после рождения. В частности, самцы экспрессируют меньше MeCP2, чем самки, и это согласуется с чувствительным к стероидам периодом времени мозга новорожденных крыс. Снижение уровня MeCP2 с помощью малой интерферирующей РНК (миРНК) в течение первых нескольких дней жизни снижает уровень социального игрового поведения подростков до типичных для женщин уровней, но не влияет на игровое поведение девочек-подростков.
MeCP2 важен для организации гормонально-зависимого поведения и половых различий в развивающейся миндалине крысы. MeCP2, по-видимому, регулирует продукцию аргининвазопрессина (AVP) и рецепторов андрогенов (AR) у самцов крыс, но не у самок. Известно, что вазопрессин регулирует многие виды социального поведения, включая создание пар и социальное признание. В то время как самцы крыс обычно имеют более высокий уровень вазопрессина в миндалевидном теле, снижение MeCP2 в течение первых 3 дней жизни вызывает стойкое снижение уровня вазопрессина до типичных для самок уровней в этой области мозга, которое сохраняется в течение всего взрослого возраста. Самцы крыс со сниженным уровнем MeCP2 также демонстрируют значительное снижение AR через две недели после инфузии, но этот эффект исчезает к взрослому состоянию.
Стресс в молодости
MeCP2 отслеживает реакцию на стресс в раннем возрасте. Стресс в раннем возрасте коррелирует с гиперфосфорилированием белка MeCP2 в паравентрикулярном ядре гипоталамуса. Таким образом, это приводит к снижению занятости MeCP2 в промоторной области гена AVP и, следовательно, к повышению уровней AVP. Вазопрессин - это первичный гормон, участвующий в оси гипотальм-гипофиз-надпочечники, связности мозга, которая регулирует обработку стресса и реакцию на него. Таким образом, сниженное функционирование белка MeCP2 усиливает стрессовую реакцию нейронов.
использованная литература
дальнейшее чтение
- Chahrour M, Zoghbi HY (2007). «История синдрома Ретта: от клиники к нейробиологии» . Нейрон . 56 (3): 422–37. DOI : 10.1016 / j.neuron.2007.10.001 . PMID 17988628 . S2CID 16266882 .
- Карни Р.М., Вольперт С.М., Раван С.А., Шахбазиан М., Эшли-Кох А., Куккаро М.Л., Вэнс Дж. М., Перикак-Ванс М.А. (2003). «Идентификация мутаций MeCP2 в серии женщин с аутичным расстройством». Pediatr Neurol . 28 (3): 205–11. DOI : 10.1016 / S0887-8994 (02) 00624-0 . PMID 12770674 .
- Керр AM, Овраг D (2003). «Обзорная статья: новые пути с синдромом Ретта» . J Интеллект Disabil Res . 47 (Pt 8): 580–7. DOI : 10.1046 / j.1365-2788.2003.00506.x . PMID 14641805 .
- Neul JL, Zoghbi HY (2004). «Синдром Ретта: прототипное расстройство психического развития». Невролог . 10 (2): 118–28. DOI : 10.1177 / 1073858403260995 . PMID 15070486 . S2CID 9617631 .
- Шанен С., Хаувинк Э. Дж., Доррани Н., Лейн Дж., Эверетт Р., Фенг А., Кантор Р. М., Перси А. (2004). «Фенотипические проявления мутации MECP2 при классическом и атипичном синдроме Ретта». Am J Med Жене . 126 (2): 129–40. DOI : 10.1002 / ajmg.a.20571 . PMID 15057977 . S2CID 32897044 .
- Ван ден Вейвер И.Б., Zoghbi HY (2001). «Мутации в гене, кодирующем метил-CpG-связывающий белок 2, вызывают синдром Ретта». Brain Dev . 23 (Дополнение 1): S147–51. DOI : 10.1016 / S0387-7604 (01) 00376-X . PMID 11738862 . S2CID 26138178 .
- Уэбб Т., Латиф Ф (2001). «Синдром Ретта и ген MECP2» . J Med Genet . 38 (4): 217–23. DOI : 10.1136 / jmg.38.4.217 . PMC 1734858 . PMID 11283201 .
- Шахбазян MD, Zoghbi HY (2003). «Синдром Ретта и MeCP2: связь эпигенетики и нейрональной функции» . Являюсь. J. Hum. Genet . 71 (6): 1259–72. DOI : 10.1086 / 345360 . PMC 378559 . PMID 12442230 .
- Moog U, Smeets EE, van Roozendaal KE и др. (2003). «Расстройства нервного развития у мужчин, связанные с геном, вызывающим синдром Ретта у женщин (MECP2)». Евро. J. Paediatr. Neurol . 7 (1): 5–12. DOI : 10.1016 / S1090-3798 (02) 00134-4 . PMID 12615169 .
- Мильтенбергер-Милтеньи G, Laccone F (2004). «Мутации и полиморфизмы в человеческом метил-CpG-связывающем белке MECP2». Гм. Мутат . 22 (2): 107–15. DOI : 10.1002 / humu.10243 . PMID 12872250 . S2CID 42516576 .
- Weaving LS, Ellaway CJ, Gécz J, Christodoulou J (2006). «Синдром Ретта: клинический обзор и генетическое обновление» . J. Med. Genet . 42 (1): 1–7. DOI : 10.1136 / jmg.2004.027730 . PMC 1735910 . PMID 15635068 .
- Бапат С., Галанде С. (2005). «Ассоциация по вине: идентификация DLX5 как мишени для MeCP2 обеспечивает молекулярную связь между геномным импринтингом и синдромом Ретта». BioEssays . 27 (7): 676–80. DOI : 10.1002 / bies.20266 . PMID 15954098 .
- Златанова Ж (2005). «MeCP2: хроматиновые связи и не только». Biochem. Cell Biol . 83 (3): 251–62. DOI : 10.1139 / o05-048 . PMID 15959553 .
- Кауфманн В.Е., Джонстон М.В., Blue ME (2006). «Экспрессия и функция MeCP2 во время развития мозга: последствия для патогенеза и клинической эволюции синдрома Ретта». Brain Dev . 27 (Дополнение 1): S77 – S87. DOI : 10.1016 / j.braindev.2004.10.008 . PMID 16182491 . S2CID 702975 .
- Армстронг Д.Д. (2006). «Можем ли мы связать дефицит MeCP2 со структурными и химическими аномалиями в мозге Ретта?». Brain Dev . 27 (Дополнение 1): S72 – S76. DOI : 10.1016 / j.braindev.2004.10.009 . PMID 16182497 . S2CID 45587850 .
- Сантос М., Коэльо PA, Maciel P (2006). «Ремоделирование хроматина и нейрональная функция: интересные ссылки» . Гены, мозг и поведение . 5 (Дополнение 2): 80–91. DOI : 10.1111 / j.1601-183X.2006.00227.x . PMID 16681803 .
- Бьенвеню Т., Челли Дж. (2006). «Молекулярная генетика синдрома Ретта: когда метилирование ДНК остается нераспознанным». Природа Обзоры Генетики . 7 (6): 415–26. DOI : 10.1038 / nrg1878 . PMID 16708070 . S2CID 28215286 .
- Франк У (2007). «Механизмы заболевания: нейрогенетика дефицита MeCP2». Природа Клиническая Практика Неврологии . 2 (4): 212–21. DOI : 10.1038 / ncpneuro0148 . PMID 16932552 . S2CID 22710951 .
внешние ссылки
- Международный фонд синдрома Ретта
- Rett UK Support and Research Charity
- Фонд исследований синдрома Ретта
- Ensembl Gene réf Protein исх
- GeneCard
- RettBASE: База данных вариаций IRSA MECP2
- Запись GeneReview / NIH / UW о заболеваниях, связанных с MECP2
- GeneReviews / NCBI / NIH / UW запись о синдроме дупликации MECP2
- Британский сайт для семей, пострадавших от MECP2.
- Сайт для семей, пострадавших от MECP2.
- Французский официальный сайт по дублированию MeCP2