Глиоксаль - Glyoxal
|
|
|||
| Имена | |||
|---|---|---|---|
|
Имена ИЮПАК
Оксальдегид
|
|||
|
Предпочтительное название IUPAC
Ethanedial |
|||
| Другие имена
Глиоксаля
Glyoxaldehyde Oxalaldehyde Ethanedialdehyde |
|||
| Идентификаторы | |||
|
3D модель ( JSmol )
|
|||
| ЧЭБИ | |||
| ChemSpider | |||
| ECHA InfoCard |
100.003.160 |
||
| КЕГГ | |||
|
PubChem CID
|
|||
| UNII | |||
|
Панель управления CompTox ( EPA )
|
|||
|
|||
|
|||
| Характеристики | |||
| С 2 Н 2 О 2 | |||
| Молярная масса | 58,036 г · моль -1 | ||
| Плотность | 1,27 г / см 3 | ||
| Температура плавления | 15 ° С (59 ° F, 288 К) | ||
| Точка кипения | 51 ° С (124 ° F, 324 К) | ||
| Термохимия | |||
|
Теплоемкость ( C )
|
1,044 Дж / (К · г) | ||
| Опасности | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | -4 ° С (25 ° F, 269 К) | ||
| 285 ° С (545 ° F, 558 К) | |||
| Родственные соединения | |||
|
Родственные альдегиды
|
ацетальдегид гликолевый альдегид пропандиальный метилглиоксаль |
||
|
Родственные соединения
|
глиоксиловая кислота и гликолевая кислота , щавелевая кислота , пировиноградная кислота , диацетил ацетилацетон |
||
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|||
|
|
|||
| Ссылки на инфобоксы | |||
Глиоксаль - это органическое соединение с химической формулой OCHCHO. Это наименьший диальдегид (соединение с двумя альдегидными группами). Это кристаллическое твердое вещество, белое при низких температурах и желтое при температуре плавления (15 ° C). Жидкость желтого цвета, а пары зеленого цвета.
Чистый глиоксаль обычно не встречается, поскольку он образует гидраты , которые олигомеризуются . Для многих целей эти гидратированные олигомеры ведут себя аналогично глиоксалю. Он производится в промышленных масштабах как предшественник многих продуктов.
Производство
Глиоксаль был впервые получен и назван немецко-британским химиком Генрихом Дебусом (1824–1915) путем взаимодействия этанола с азотной кислотой .
Коммерческий глиоксаль получают либо путем газофазного окисления из этиленгликоля в присутствии серебра или меди катализатора (процесс Лапорта) или путем жидкофазного окисления ацетальдегида с азотной кислотой .
Первый коммерческий источник глиоксаля был в Ламотте , Франция, начат в 1960 году. Единственным крупнейшим коммерческим источником является BASF в Людвигсхафене , Германия , с производительностью около 60 000 тонн в год. Другие производственные площадки существуют также в США и Китае. Коммерческий глиоксаль в нерасфасованном виде производится и представляет собой 40% -ный раствор в воде по весу (молярное отношение глиоксаля к воде приблизительно 1: 5).
Лабораторные методы
Глиоксальте может быть синтезированы в лаборатории путем окисления ацетальдегида с селенистой кислотой .
Безводный глиоксаль получают путем нагревания твердого гидрата (ов) глиоксаля с пятиокисью фосфора и конденсации паров в холодной ловушке .
Характеристики
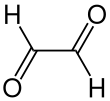
Экспериментально определенная константа закона Генри для глиоксаля равна:
Биохимия

Конечные продукты улучшенного гликирования (AGE) - это белки или липиды, которые становятся гликированными в результате диеты с высоким содержанием сахара. Они представляют собой биомаркеры, влияющие на старение и развитие или ухудшение многих дегенеративных заболеваний , таких как диабет , атеросклероз , хроническое заболевание почек и болезнь Альцгеймера .
Приложения
В мелованной бумаге и текстильных материалах используется большое количество глиоксаля в качестве сшивающего агента для составов на основе крахмала . Он конденсируется с мочевиной с образованием 4,5-дигидрокси-2-имидазолидинона, который далее реагирует с формальдегидом, давая бис (гидроксиметил) производное диметилолэтиленмочевины , которое используется для химической обработки одежды, устойчивой к появлению морщин, то есть постоянной печати.
Глиоксаль используется как солюбилизатор и сшивающий агент в химии полимеров .
Глиоксаль является ценным строительным блоком в органическом синтезе , особенно в синтезе гетероциклов, таких как имидазолы . Удобной формой реагента для использования в лаборатории является его бис (полуацеталь) с этиленгликолем , 1,4-диоксан-2,3-диол. Это соединение коммерчески доступно.
Растворы глиоксаля также можно использовать в качестве фиксатора для гистологии , то есть как метод сохранения клеток для исследования их под микроскопом.
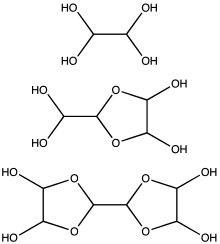
Видообразование в растворе
Глиоксаль обычно поставляется в виде 40% -ного водного раствора. Как и другие небольшие альдегиды , глиоксаль образует гидраты. Кроме того, гидраты конденсируются с образованием ряда олигомеров, структура некоторых из которых остается неопределенной. Для большинства приложений точная природа частиц в растворе не имеет значения. По крайней мере, один гидрат глиоксаля продается на рынке, дигидрат тримера глиоксаля: [(CHO) 2 ] 3 (H 2 O) 2 (CAS 4405-13-4). Доступны и другие эквиваленты глиоксаля, такие как полуацеталь этиленгликоля 1,4-диоксан- транс -2,3 -диол ( CAS 4845-50-5, температура плавления 91-95 ° C).
Подсчитано, что при концентрациях менее 1 М глиоксаль существует преимущественно в виде мономера или его гидратов, т.е. ОСННО, ОСНСН (ОН) 2 или (НО) 2 СНСН (ОН) 2 . При концентрациях выше 1 М преобладают димеры. Эти димеры, вероятно, являются диоксоланами с формулой [(HO) CH] 2 O 2 CHCHO. Димеры и тримеры осаждаются в виде твердых веществ из холодных растворов.
Другие случаи
Глиоксаль был обнаружен как следовой газ в атмосфере, например как продукт окисления углеводородов. Тропосферные концентрации 0-200 п.п. по объему сообщалось, в загрязненных районах до 1 частей на миллиард по объему.
Безопасность
ЛД50 (перорально, крысы) 3300 мг / кг, при ЛД50 поваренной соли составляет 3000 мг / кг.
использованная литература
- ^ pubchem.ncbi.nlm.nih.gov/compound/Glyoxal#section=IUPAC-Name&fullscreen=true
- Перейти ↑ O'Neil, MJ (2001): The Merck Index , 13th Edition, page 803.
- ^ a b c d e f Маттиода, Жорж; Блан, Ален. «Глиоксаль». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a12_491.pub2 .
-
^ См .:
- Х. Дебус (1857) «О действии азотной кислоты на спирт при обычных температурах», Philosophical Magazine , 4-я серия, 13 : 39–49. С п. 40: «Этот остаток почти полностью состоял из альдегида глиоксиловой кислоты; я предложил назвать его глиоксалем , C 2 H 4 O 3 ».
- Х. Дебус (1857) «О глиоксале», Philosophical Magazine , 4-я серия, 13 : 66.
- ^ Генри Энфилд Роско и Карл Шорлеммер, Трактат по химии , том. 3 (Нью-Йорк, Нью-Йорк: Д. Эпплтон и Ко, 1890), стр. 101-102.
- ^ Ронцио, АР; Во, Т. Д. (1944). «Глиоксаль бисульфит». Органический синтез . 24 : 61. DOI : 10,15227 / orgsyn.024.0061 .
-
^ Harries, C .; Темме, Ф. (1907). "Über monomolekulares und trimolekulares Glyoxal" [О мономолекулярном и тримоэкулярном глиоксале]. Берихте . 40 (1): 165–172. DOI : 10.1002 / cber.19070400124 .
Man erhitzt nun das Glyoxal-Phosphorpentoxyd-Gemisch mit freier Flamme und beobachtet bald, dass sich unter Schwarzfärbung des Kolbeninhalte ein flüchtiges grünes Gas bildet, welches sich in der gekühltenöövöröööös. [Смесь (сырого) глиоксаля и P 4 O 10 нагревают открытым пламенем и вскоре после почернения содержимого обнаруживают подвижный зеленый газ, который конденсируется в охлажденной колбе в виде красивых желтых кристаллов.]
- ^ Ip, HS; Хуанг, XH; Ю., JZ (2009). «Эффективные константы закона Генри глиоксаля, глиоксиловой кислоты и гликолевой кислоты» (PDF) . Geophys. Res. Lett . 36 (1): L01802. Bibcode : 2009GeoRL..36.1802I . DOI : 10.1029 / 2008GL036212 .
- ^ Голдин, Элисон; Бекман, Джошуа А .; Шмидт, Энн Мари; Крегер, Марк А. (2006). «Американская кардиологическая ассоциация» . Тираж . 114 (6): 597–605. DOI : 10.1161 / CIRCULATIONAHA.106.621854 . PMID 16894049 .
- ^ Вистоли, G; Де Маддис, доктор философии; Ципак, А; Жаркович, Н; Карини, М; Aldini, G (август 2013 г.). «Конечные продукты продвинутого гликоксидации и липоксидации (AGE и ALE): обзор механизмов их образования» (PDF) . Свободный Радич. Res . 47 : Suppl 1: 3–27. DOI : 10.3109 / 10715762.2013.815348 . PMID 23767955 . S2CID 207517855 .
- ^ Снайдер, HR; Хэндрик, Р.Г.; Брукс, Л.А. (1942). «Имидазол» . Органический синтез . 22 : 65.; Сборник , 3 , с. 471
- Перейти ↑ Whipple, EB (1970). «Структура глиоксаля в воде». Варенье. Chem. Soc. 92 (24): 7183–7186. DOI : 10.1021 / ja00727a027 .
- ^ Vrekoussis, M .; Wittrock, F .; Richter, A .; Берроуз, JP (2009). «Временная и пространственная изменчивость глиоксаля из космоса» . Атмос. Chem. Phys . 9 (13): 4485–4504. DOI : 10,5194 / ACP-9-4485-2009 .
- ^ Volkamer, Райнер; и другие. (2007). «Недостающий сток для газофазного глиоксаля в Мехико: образование вторичного органического аэрозоля». Geophys. Res. Lett . 34 (19): 19. Bibcode : 2007GeoRL..3419807V . DOI : 10.1029 / 2007gl030752 .
- ^ «Данные по безопасности (MSDS) для хлорида натрия» . ox.ac.uk . Архивировано из оригинала на 2011-06-07.



![{\ displaystyle K _ {\ text {H}} = 4,19 \ times 10 ^ {5} \ times \ exp \ left [{\ frac {6.22 \ times 10 ^ {4} \, {\ text {kJ}} \, {\ text {mol}} ^ {- 1}} {R}} \ times \ left ({\ frac {1} {T}} - {\ frac {1} {298 \, {\ text {K}}) }} \ right) \ right] \, {\ text {M}} \, {\ text {atm}} ^ {- 1}.}](https://wikimedia.org/api/rest_v1/media/math/render/svg/889cc6b8a3cb98f718253ccab840f434f2809fd5)