Эзопиклон - Eszopiclone
 | |
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Lunesta, Eszop, другие |
| AHFS / Drugs.com | Монография |
| MedlinePlus | a605009 |
| Данные лицензии | |
| Пути администрирования |
Внутрь ( таблетки ) |
| Код УВД | |
| Правовой статус | |
| Правовой статус | |
| Фармакокинетические данные | |
| Связывание с белками | 52–59% |
| Метаболизм | Окисление и деметилирование печени ( опосредованное CYP3A4 и CYP2E1 ) |
| Ликвидация Период полураспада | 6 часов |
| Экскреция | Почка |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| Панель управления CompTox ( EPA ) | |
| ECHA InfoCard |
100.149.304 |
| Химические и физические данные | |
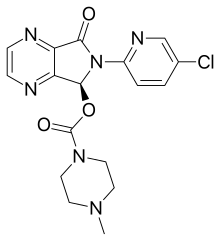
| Формула | C 17 H 17 Cl N 6 O 3 |
| Молярная масса | 388,81 г · моль -1 |
| 3D модель ( JSmol ) | |
| |
| |
| (проверять) | |
Эсзопиклон , продаваемый, среди прочего, под торговой маркой Lunesta , является лекарством, используемым для лечения бессонницы . Доказательства подтверждают пользу от легкой до умеренной на срок до шести месяцев. Принимается внутрь.
Общие побочные эффекты включают головную боль, сухость во рту , тошноту и головокружение. Серьезные побочные эффекты могут включать суицидальные мысли , нездоровое немедицинское употребление, галлюцинации и ангионевротический отек . Более тщательный уход рекомендуется людям с проблемами печени и пожилым людям. Быстрое снижение дозы может привести к отмене. Эзопиклон классифицируется как небензодиазепиновый седативный снотворный и циклопирролон . Это S - стереоизомеры из зопиклона . Он работает, взаимодействуя с рецепторами ГАМК .
Эзопиклон, одобренный для медицинского применения в США в 2004 году, доступен как генерический препарат . В 2017 году это было 214-е место среди наиболее часто назначаемых лекарств в Соединенных Штатах: было выписано более двух миллионов рецептов. Эсзопиклон не продается в Европейском Союзе , поскольку в 2009 году EMA постановило, что он слишком похож на зопиклон, чтобы считаться новым патентоспособным продуктом.
Медицинское использование
Кокрановский обзор 2018 года показал, что он дает умеренное улучшение наступления и поддержания сна. Авторы предполагают, что там, где предпочтительные немедикаментозные стратегии лечения исчерпаны, эзопиклон обеспечивает эффективное лечение бессонницы. В 2014 году USFDA попросило снизить начальную дозу с 2 миллиграммов до 1 миллиграмма после того, как в исследовании было обнаружено, что даже через 8 часов после приема препарата в ночное время некоторые люди не могли справляться со своими повседневными делами, такими как вождение и другие действия, требующие полной бдительности.
Эзопиклон немного эффективен при лечении бессонницы, когда проблема с засыпанием является основной жалобой. Кирш и др. обнаружили, что преимущество перед плацебо имеет сомнительную клиническую значимость. Хотя эффект препарата и ответ на плацебо были довольно незначительными и сомнительной клинической значимостью, они вместе дают достаточно большой клинический ответ. Не рекомендуется для хронического употребления пожилыми людьми.
Пожилые люди
Седативные снотворные препараты, включая эзопиклон, чаще назначают пожилым людям, чем более молодым пациентам, несмотря на то, что их преимущества обычно не вызывают впечатления. Следует проявлять осторожность при выборе подходящего снотворного, и если лекарственная терапия начата, ее следует начинать с минимально возможной дозы, чтобы минимизировать побочные эффекты.
В 2015 году Американское гериатрическое общество рассмотрело информацию о безопасности эзопиклона и аналогичных препаратов и пришло к выводу, что «небензодиазепиновых, агонистических средств бензодиазепиновых рецепторов (эзопиклон, залеплон , золпидем ) следует избегать без учета продолжительности использования из-за их связи с вредом. сбалансированы с их минимальной эффективностью при лечении бессонницы ».
В обзоре было сделано это заключение как из-за относительно большой опасности золпидема и других «z-препаратов» для пожилых людей, так и из-за того факта, что эти препараты обладают «минимальной эффективностью при лечении бессонницы». Это было изменение по сравнению с рекомендацией AGS 2012 года, в которой предлагалось ограничить использование до 90 дней или меньше. В обзоре говорилось: «предостережение относительно 90-дневного использования [было] снято с небензодиазепиновых снотворных, агонистов бензодиазепиновых рецепторов, что привело к недвусмысленному заявлению« избегать »(без оговорок) из-за увеличения доказательств вреда в этой области с тех пор, как Обновление 2012 г. "
Обширный обзор медицинской литературы, посвященной лечению бессонницы и пожилых людей, показал, что существуют значительные доказательства эффективности и долговечности немедикаментозных методов лечения бессонницы у взрослых всех возрастов и что эти вмешательства используются недостаточно. По сравнению с бензодиазепинами небензодиазепиновые седативно-снотворные средства, в том числе эзопиклон, по-видимому, не имели значительных клинических преимуществ по эффективности или переносимости у пожилых людей, если таковые были. Было обнаружено, что новые агенты с новыми механизмами действия и улучшенными профилями безопасности, такие как агонисты рецепторов мелатонина , перспективны для лечения хронической бессонницы у пожилых людей. Долгосрочное использование седативно-снотворных средств при бессоннице не имеет доказательной базы и традиционно не рекомендуется по причинам, которые включают опасения по поводу таких потенциальных побочных эффектов лекарств, как когнитивные нарушения ( антероградная амнезия ), дневная седация, нарушение координации движений и повышенный риск движения автотранспорта. аварии и падения. Кроме того, еще предстоит определить эффективность и безопасность длительного использования этих агентов. Был сделан вывод о том, что необходимы дополнительные исследования для оценки долгосрочных эффектов лечения и наиболее подходящей стратегии ведения пожилых людей с хронической бессонницей.
Мета-анализ 2009 года выявил более высокий уровень инфицирования .
Побочные эффекты
Снотворные, в том числе эзопиклон, связаны с повышенным риском смерти.
Повышенная чувствительность к эзопиклону является противопоказанием к его применению. Некоторые побочные эффекты встречаются чаще, чем другие. Рекомендации по использованию эзопиклона могут быть изменены другими состояниями здоровья. Эти условия или обстоятельства могут возникать у людей с пониженным метаболизмом и другими состояниями. При определении частоты и дозировки можно учитывать наличие нарушения функции печени, лактации и деятельности, требующей умственной активности (например, вождение).
- неприятный вкус
- Головная боль
- периферический отек
- грудная боль
- ненормальное мышление
- изменение поведения
- депрессия
- галлюцинации
- вождение во сне и лунатизм
- сухость во рту
- сыпь
- измененный режим сна
- нарушение координации
- головокружение
- дневная сонливость
- зуд
- болезненное или частое мочеиспускание
- боль в спине
- агрессивное поведение
- путаница
- волнение
- суицидальные мысли
- обезличивание
- амнезия
Метаанализ 2009 года показал , что у людей, принимающих эзопиклон или другие снотворные средства, на 44% выше частота легких инфекций , таких как фарингит или синусит , по сравнению с теми, кто принимает плацебо.
Зависимость
В Соединенных Штатах эзопиклон является контролируемым веществом из Списка IV в соответствии с Законом о контролируемых веществах . Использование эзопиклона может привести к физической и психологической зависимости. Риск немедицинского употребления и зависимости возрастает с увеличением дозы и продолжительности употребления и одновременного употребления других психоактивных веществ. Риск также выше у пациентов с расстройствами, связанными с употреблением алкоголя, или другими расстройствами, связанными с употреблением психоактивных веществ, или с психическими расстройствами в анамнезе. Переносимость может развиться после многократного приема бензодиазепинов и бензодиазепиноподобных препаратов в течение нескольких недель.
Исследование, финансируемое и проведенное компанией Sepracor , производителем эзопиклона, не обнаружило признаков толерантности или зависимости в группе пациентов, наблюдаемых в течение шести месяцев.
Немедицинское использование
Исследование возможностей немедицинского использования эзопиклона показало, что у лиц , ранее использовавших бензодиазепины в немедицинских целях, эзопиклон в дозах 6 и 12 мг производил эффекты, аналогичные эффектам 20 мг диазепама . Исследование показало, что при этих дозах, которые в два или более раз превышают максимальные рекомендуемые дозы, как для эзопиклона (Lunesta), так и для диазепама ( Валиум ).
Передозировка
Согласно информации о назначении в США, сообщалось о передозировках эзопиклона, в 90 раз превышающих рекомендованную дозу, при которых пациент полностью выздоравливал. Согласно выпуску официальной информации о назначении лекарств США за май 2014 г. , смертельные случаи были зарегистрированы только в тех случаях, когда эзопиклон сочетался с другими наркотиками или алкоголем.
Центры по борьбе с отравлениями сообщили, что в период с 2005 по 2006 год в штате Техас было зарегистрировано 525 случаев полной передозировки эзопиклона , большинство из которых были преднамеренными попытками самоубийства .
При употреблении в течение последнего часа передозировку эзопиклона можно лечить приемом активированного угля или промыванием желудка .
Взаимодействия
При приеме эзопиклона вместе с другими депрессантами ЦНС, включая антипсихотики , седативные снотворные (например, барбитураты или бензодиазепины), антигистаминные препараты , опиоиды , фенотиазины и некоторые антидепрессанты, повышается риск депрессии центральной нервной системы . Также повышается риск угнетения центральной нервной системы при приеме других лекарств, которые подавляют метаболическую активность ферментной системы CYP3A4 в печени . Лекарства, которые ингибируют эту ферментную систему, включают нелфинавир , ритонавир , кетоконазол , итраконазол и кларитромицин . Алкоголь также оказывает аддитивный эффект при одновременном применении с эзопиклоном. Эзопиклон наиболее эффективен, если его не принимать после обильной еды с высоким содержанием жира.
Фармакология
Эзопиклон действует на сайт связывания бензодиазепина, расположенный на нейронах ГАМК А, как положительный аллостерический модулятор . Эзопиклон быстро всасывается после перорального приема с пиком в сыворотке крови между 0,45 и 1,3 часа. Период полувыведения эзопиклона составляет примерно 6 часов, и он интенсивно метаболизируется путем окисления и деметилирования. Приблизительно от 52% до 59% дозы слабо связывается с белками плазмы. Изоферменты цитохрома P450 (CYP) CYP3A4 и CYP2E1 участвуют в биотрансформации эзопиклона; таким образом, препараты, которые индуцируют или ингибируют эти изоферменты CYP, могут влиять на метаболизм эзопиклона. Менее 10% принятой перорально дозы выводится с мочой в виде рацемического зопиклона. С точки зрения связывания бензодиазепинового рецептора и соответствующей активности 3 мг эзопиклона эквивалентны 10 мг диазепама .
История
В противоречивой статье 2009 года в Медицинском журнале Новой Англии «Потерянная передача - информация FDA о лекарствах, которая никогда не доходит до клиницистов», сообщалось, что в самом крупном из трех исследований Lunesta было обнаружено, что по сравнению с плацебо Lunesta «превосходит плацебо», в то время как это только сократило начальное время засыпания в среднем на 15 минут. «Клиницисты, интересующиеся эффективностью препарата, не могут найти информацию об эффективности на этикетке: там указано только, что Lunesta превосходит плацебо. Медицинский обзор FDA предоставляет данные об эффективности, хотя и не раньше, чем на странице 306 403-страничного документа. В крупнейшем испытании фазы 3 пациенты из группы Lunesta засыпали в среднем на 15 минут быстрее и спали в среднем на 37 минут дольше, чем в группе плацебо. Однако в среднем пациенты Lunesta по-прежнему соответствовали критериям бессонницы и не сообщили клинически значимое улучшение активности или функционирования на следующий день ».
Доступность в Европе
11 сентября 2007 года Sepracor подписала маркетинговое соглашение с британской фармацевтической компанией GlaxoSmithKline на право продажи эзопиклона (под названием Lunivia, а не Lunesta) в Европе . Ожидалось, что Sepracor получит около 155 миллионов долларов, если сделка состоится. В 2008 году Sepracor подал заявку в EMA ( эквивалент Европейского союза FDA США ) для получения разрешения на продажу препарата в ЕС и сначала получил положительный ответ. Однако Sepracor отозвала свою заявку на разрешение в 2009 году после того, как EMA заявило, что не будет предоставлять эзопиклону статус «нового активного вещества», поскольку он по сути фармакологически и терапевтически слишком похож на зопиклон, чтобы считаться новым патентоспособным продуктом. Поскольку срок действия патента на зопиклон истек, это постановление позволило бы конкурирующим компаниям также законно производить более дешевые генерические версии эзопиклона для европейского рынка. По состоянию на ноябрь 2012 года Sepracor не подавал повторную заявку на авторизацию, и эзопиклон недоступен в Европе. Сделка с GSK сорвалась, и вместо этого GSK заключила сделку на 3,3 миллиарда долларов по продаже снотворного препарата Actelion almorexant , который вошел в фазу 3 медицинских испытаний, прежде чем разработка была прекращена из-за побочных эффектов.
использованная литература
внешние ссылки
- «Эзопиклон» . Информационный портал о наркотиках . Национальная медицинская библиотека США.
