Тропинон - Tropinone

|
|

|
|
| Имена | |
|---|---|
|
Название ИЮПАК
8-Метил-8-азабицикло [3.2.1] октан-3-он
|
|
| Другие имена
3-тропинон
|
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| ЧЭБИ | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard |
100.007.756 |
|
PubChem CID
|
|
| UNII | |
|
Панель управления CompTox ( EPA )
|
|
|
|
|
|
| Характеристики | |
| C 8 H 13 НЕТ | |
| Молярная масса | 139,195 г / моль |
| Появление | Коричневое твердое вещество |
| Температура плавления | 42,5 ° С (108,5 ° F, 315,6 К) |
| Точка кипения | (разлагается) |
| Опасности | |
| NFPA 704 (огненный алмаз) | |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
Тропинон - это алкалоид , синтезированный в 1917 году Робертом Робинсоном в качестве синтетического предшественника атропина , дефицитного товара во время Первой мировой войны . Тропинона и алкалоиды кокаин и атропин все одни и те же тропан структура ядра. Соответствующая им конъюгированная кислота при pH 7,3 основных разновидностей известна как тропиниумон .
Синтез
Первый синтез тропинона был осуществлен Ричардом Вильштеттером в 1901 году. Он начался с, казалось бы, родственного циклогептанона , но потребовал многих шагов для введения азотного мостика; общий выход для пути синтеза составляет всего 0,75%. Вильштеттер ранее синтезировал кокаин из тропинона, что явилось первым синтезом и выяснением структуры кокаина.
«Двойная реакция Манниха» Робинсона
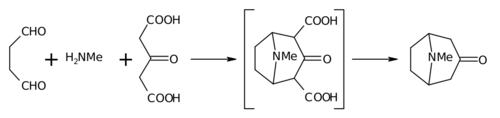
Синтез 1917 года Робинсона считается классическим в общем синтезе из-за его простоты и биомиметического подхода. Тропинон представляет собой бициклическую молекулу , но реагенты, используемые при его получении, довольно просты: янтарный альдегид , метиламин и ацетонедикарбоновая кислота (или даже ацетон ). Синтез является хорошим примером биомиметической реакции или синтеза биогенетического типа, поскольку в биосинтезе используются одни и те же строительные блоки. Он также демонстрирует тандемную реакцию в однореакторном синтезе . Кроме того, выход синтеза составил 17%, а с последующими улучшениями превысил 90%.
Эта реакция описывается как внутримолекулярная «двойная реакция Манниха » по понятным причинам. В этом отношении он не уникален, поскольку другие также пытались использовать его в синтезе пиперидина.
Вместо ацетона ацетонедикарбоновая кислота известна как « синтетический эквивалент ». Группы 1,3-дикарбоновой кислоты представляют собой так называемые « активирующие группы » для облегчения реакций образования кольца. Соль кальция используется в качестве « буфера », поскольку утверждается, что более высокие выходы возможны, если реакция проводится при « физиологическом pH ».
Механизм реакции
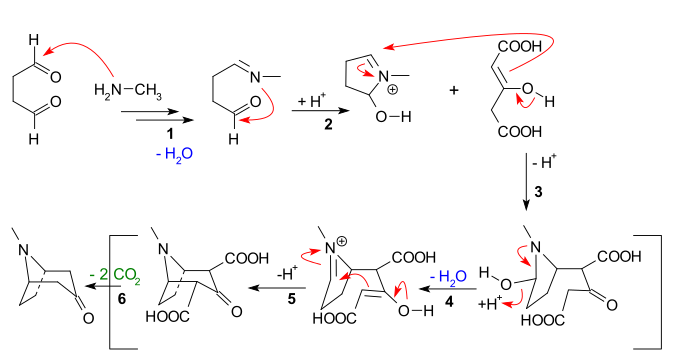
Основные особенности, очевидные из приведенной ниже последовательности реакций:
- Нуклеофильное присоединение из метиламина в янтарный , а затем потере воды , чтобы создать имин
- Внутримолекулярное добавление имина ко второму альдегидному звену и замыкание первого кольца
- Межмолекулярная Манниха реакция на еноляте ацетон дикарбоксилата
- Образование нового енолята и образование нового имина с потерей воды на
- Вторая внутримолекулярная реакция Манниха и замыкание второго кольца
- Потеря 2 карбоксильных групп до тропинона
Некоторые авторы действительно пытались сохранить одну из групп CO 2 H.
CO 2 R-тропинон имеет 4 стереоизомера, хотя соответствующий алкиловый эфир экгонидина имеет только пару энантиомеров.
Из циклогептанона
IBX- дегидрирование (окисление) циклогептанона (суберона) до 2,6-циклогептадиенона [1192-93-4] с последующей реакцией с амином является универсальным способом образования тропинонов. Вызванный механизм четко обозначен как двойная реакция Михаэля (т.е. добавление конъюгата).
Биохимический метод
Снижение тропинона
Снижение уровня тропинона опосредуется НАДФН- зависимыми ферментами редуктазы, которые были охарактеризованы у многих видов растений. Все эти виды растений содержат два типа ферментов редуктазы, тропинонредуктазу I и тропинонредуктазу II. TRI производит тропин, а TRII производит псевдотропин. Из-за различных кинетических характеристик и характеристик pH / активности ферментов, а также из-за того, что активность TRI в 25 раз выше, чем у TRII, большая часть восстановления тропинона происходит за счет TRI с образованием тропина.
Смотрите также
- Бензтропин
- Дурман
- 2-Карбометокситропинон (2-CMT) промежуточный продукт в создании аналогов кокаина экгонина
- Экгонидин