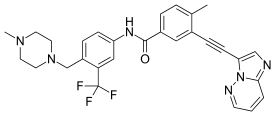
Понатиниб - Ponatinib
 | |
 | |
| Клинические данные | |
|---|---|
| Произношение | / Р oʊ п æ т ɪ п ɪ б / poh- НАТ -i-Перо |
| Торговые наименования | Iclusig |
| Другие имена | AP24534 |
| AHFS / Drugs.com | Монография |
| MedlinePlus | a613029 |
| Данные лицензии | |
Категория беременности |
|
| Пути администрирования |
Внутрь ( таблетки ) |
| Код УВД | |
| Правовой статус | |
| Правовой статус | |
| Фармакокинетические данные | |
| Биодоступность | Неизвестный |
| Связывание с белками | > 99% ( in vitro ) |
| Метаболизм | Печень ( CYP3A4 , 2C8 , 2D6 , 3A5 ) |
| Ликвидация Период полураспада | 12–66 часов |
| Экскреция | Кал (87%), моча (5%) |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| Панель управления CompTox ( EPA ) | |
| Химические и физические данные | |
| Формула | C 29 H 27 F 3 N 6 O |
| Молярная масса | 532,571 г · моль -1 |
| 3D модель ( JSmol ) | |
| |
| |
Ponatinib (торговое название Iclusig / aɪ к л ¯u с ɪ ɡ / глаз- Клу -sig , ранее AP24534 ) является устным препарат , разработанным ARIAD Pharmaceuticals для лечения хронического миелолейкоза (ХМЛ) и Филадельфию хромосомы -положительной (Ph +) , острый лимфобластный лейкоз (ОЛЛ). Это многоцелевой ингибитор тирозинкиназы . Некоторые формы ХМЛ, имеющие мутацию T315I, устойчивы к современным методам лечения, таким как иматиниб . Понатиниб был разработан, чтобы быть эффективным против этих типов опухолей.
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США одобрило этот препарат в качестве кандидата в декабре 2012 года, но 31 октября 2013 года временно приостановило продажи из-за «риска образования опасных для жизни тромбов и сильного сужения кровеносных сосудов». Эта приостановка была частично отменена 20 декабря 2013 года, когда для понатиниба была выпущена пересмотренная информация о назначении понатиниба, введены новые «Предупреждение о черном ящике» и «Стратегия оценки и смягчения рисков» для более точной оценки рисков и преимуществ использования препарата.
В США это может стоить 138 000 долларов в год, что подвергается критике.
Допуски и показания
Понатиниб был одобрен FDA США 14 декабря 2012 г. для пациентов с резистентным или непереносимым ХМЛ и Ph + ALL на основании результатов исследования фазы II PACE, опубликованных днями ранее на ежегодном заседании ASH . Поскольку одобрение было получено в рамках программы ускоренного одобрения FDA, от заявителя требовалось провести дополнительные исследования. На основании этих дополнительных исследований FDA предоставило в 2016 году полное одобрение и обновило этикетку, включив в него пациентов с хронической фазой, ускоренной фазой или бластной фазой хронического миелоидного лейкоза и острым лимфобластным лейкозом с положительной филадельфийской хромосомой, для которых не применяется никакая другая терапия ингибиторами тирозинкиназы. указано. Одобрение было также получено для лечения острого лимфобластного лейкоза, положительного по филадельфийской хромосоме, с положительным T315I и положительным T315I.
Побочные эффекты
9 октября 2013 г. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США частично приостановило участие в новых испытаниях понатиниба из-за увеличения количества тромбов, наблюдаемых у пациентов, принимающих препарат. Позднее, 18 октября, исследование EPIC было отменено. Последующие исследования 449 пациентов, получавших в течение 4 лет понатиниб по поводу хронической фазы хронического миелогенного лейкоза, обнаружили следующие побочные реакции. У 150 пациентов наблюдались сердечно-сосудистые (21% пациентов), периферические (12%) и цереброваскулярные (9%) артериальные окклюзионные события. Венозные тромбоэмболические осложнения наблюдались у 6% пациентов. Наиболее частыми нежелательными явлениями разной степени были гипертония (69%), сыпь (63%), боль в животе (48%), усталость (47%), головная боль (43%), артериальная ишемия (42%), сухость кожи ( 42%), запор (41%), артралгия (32%), тошнота (28%), гипертермия (26%), периферическая невропатия (24%), миалгия (24%), боль в конечностях (23%), спине боль (21%) и диарея (20%). Кроме того, были зарегистрированы случаи синдрома задней обратимой энцефалопатии .
Клинические испытания
В 2010 году ARIAD объявил о результатах Фазы I исследования понатиниба у пациентов с резистентным и рефрактерным хроническим миелоидным лейкозом (ХМЛ) и филадельфийским острым лимфобластным лейкозом (Ph + ALL). Исследование показало, что у пациентов с хронической фазой ХМЛ, получавших понатиниб, 66 процентов пациентов в исследовании достигли значительного цитогенетического ответа, включая 100 процентов пациентов, у которых также была мутация T315I.
В основное исследование фазы II PACE (Ponatinib Ph + ALL and CML Evaluation) начали регистрировать пациентов в сентябре 2010 г., и оно предназначено для предоставления окончательных клинических данных для утверждения регулирующими органами в этих условиях. Хорошие результаты были получены в декабре 2012 года.
Исследование фазы III EPIC (оценка эффективности понатиниба и иматиниба при ХМЛ) началось в июне 2012 г. и было остановлено 18 октября 2013 г.
Механизм действия
Первичной мишенью для понатиниба является BCR-ABL , аномальная тирозинкиназа, которая является отличительной чертой CML и Ph + ALL. ХМЛ характеризуется чрезмерным и нерегулируемым образованием лейкоцитов костным мозгом из-за генетической аномалии, которая продуцирует белок BCR-ABL. После хронической фазы производства слишком большого количества лейкоцитов ХМЛ обычно переходит в более агрессивные фазы, такие как ускоренный или взрывной кризис. Ph + ALL - это подтип острого лимфобластного лейкоза, который несет хромосому Ph +, которая продуцирует BCR-ABL. Он протекает более агрессивно, чем ХМЛ, и его часто лечат комбинацией химиотерапии и ингибиторов тирозинкиназы. Поскольку оба этих заболевания экспрессируют белок BCR-ABL, это может сделать их потенциально восприимчивыми к лечению понатинибом. BCR-ABL выявляется у 95% пациентов с ХМЛ.
Пациенты с ХМЛ в настоящее время получают терапию первой линии - нилотиниб и / или дазатиниб, хотя 22-33% пациентов прекращают терапию через два года из-за побочных эффектов, неудач лечения и других причин.
Открытие и происхождение
Понатиниб был разработан с использованием вычислительной и структурной платформы разработки лекарств ARIAD для подавления ферментативной активности BCR-ABL с очень высокой эффективностью и широкой специфичностью. Понатиниб был предназначен для воздействия не только на нативный BCR-ABL, но и на его изоформы, несущие мутации, которые придают устойчивость к лечению существующими ингибиторами тирозинкиназы, включая особенно мутацию T315I, для которой не существует эффективной терапии.
Путь к открытиям связан с AP23464, одним из первых конкурентных двойных ингибиторов Src / Abl АТФ компании Ariad. AP23464 был идентифицирован с использованием дизайна лекарственного средства на основе структуры и целевых синтетических библиотек тризамещенных аналогов пурина . Вещество эффективно ингибирует киназы Src и Bcr-Abl, включая многие распространенные мутации Bcr-Abl, устойчивые к иматинибу. Однако AP23464 не ингибирует мутацию T315I, в то время как понатиниб подавляет.
Стоимость, покрытие и доступность
[США] Онкологи жаловались, что многие пациенты не могут позволить себе «астрономическую» стоимость 138 000 долларов в год, что делает его одним из самых дорогих лекарств в медицине, и [по их мнению] намного более дорогим, чем то, что необходимо для оплаты разработки. расходы.
В 2015 году понатиниб доступен в Англии для лечения ХМЛ (хроническая фаза, ускоренная фаза или бластная фаза) и Ph + ALL у пациентов с задокументированной мутацией T315I в рамках Фонда противораковых препаратов и не был оценен Национальным институтом здравоохранения и ухода. Excellence (NICE), отметившую малочисленность ожидаемой популяции пациентов. По оценкам NICE, понатиниб будет стоить приблизительно 61 000 фунтов стерлингов в год, но цена, уплачиваемая Фондом противораковых препаратов, является конфиденциальной и может отличаться.
Смотрите также
использованная литература
внешние ссылки
- «Понатиниб» . Информационный портал о наркотиках . Национальная медицинская библиотека США.
