Этонитазен - Etonitazene
 | |
 | |
| Клинические данные | |
|---|---|
| Код УВД | |
| Правовой статус | |
| Правовой статус | |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| ЧЭМБЛ | |
| Панель управления CompTox ( EPA ) | |
| ECHA InfoCard |
100.011.827 |
| Химические и физические данные | |
| Формула | C 22 H 28 N 4 O 3 |
| Молярная масса | 396,491 г · моль -1 |
| 3D модель ( JSmol ) | |
| |
| |
|
| |
Etonitazene является обезболивающим лекарственным средством, впервые сообщались в 1957 году, что было показано, что примерно тысяча на тысячу пятьсот раз потенции от морфина у животных
Поскольку он характеризуется сильным потенциалом зависимости и склонностью вызывать глубокое угнетение дыхания , он не используется у людей. Однако он полезен на животных моделях для исследований зависимости , особенно тех, которые требуют от животных пить или проглатывать агент, поскольку он не такой горький, как соли опиатов, такие как сульфат морфина .
Незаконное производство
Незаконное производство и продажа этонитазена ограничены. Выявленный на московском нелегальном рынке наркотиков в 1998 году, его в основном курили в сигаретах со шнурками. Химик из Morton Thiokol произвел соединение и поместил его в носовой ингалятор. Препарат производился в России в 1996 году и продавался как «Китайский карлик». Препарат привел к неподтвержденному количеству смертей из-за его неопределенной силы действия. Похоже, что у него крутая кривая доза-ответ и непредсказуемая фармакокинетика, особенно при инъекции, аналогично некоторым другим сильнодействующим опиоидам, таким как декстроморамид , что может сделать этонитазен особенно опасным по сравнению с опиоидами аналогичной активности, такими как фентанил .
Аналоги
Известен ряд аналогов, и единственным другим хорошо известным соединением, вышедшим из первоначальных исследований 1950-х годов, является клонитазен , который намного слабее этонитазена (примерно в 3 раза больше морфина). Совсем недавно, примерно с конца 2018 года, на незаконных рынках по всему миру начал появляться ряд дизайнерских аналогов, наиболее известными из которых являются метонитазен , изотонитазен и этазен , хотя другие продолжают появляться.
Из этих аналогов только этонитазен и клонитазен прямо перечислены в конвенциях ООН и поэтому контролируются во всем мире. Остальное будет незаконным только в таких странах, как США, Австралия и Новая Зеландия, где действуют законы, эквивалентные Федеральному закону об аналогах . В Соединенных Штатах это контролируемое наркотическое вещество из Списка I с DEA ACSCN 9624 и нулевой годовой квотой на производство по состоянию на 2013 год.
Синтез
Этонитазен и родственные ему опиоидные агонисты бензимидазолы были открыты в конце 1950-х годов группой швейцарских исследователей, работающих в фармацевтической фирме CIBA (ныне Novartis ). Одним из первых соединений, исследованных швейцарской командой, был 1- (β-диэтиламиноэтил) -2-бензилбензимидазол, который, как было обнаружено, обладает 10% анальгетической активности морфина при испытаниях в биотестах на грызунах. Это открытие побудило группу начать всестороннее систематическое исследование 2-бензилбензимидазолов и установить взаимосвязь структура-активность этого нового семейства анальгетиков. Для получения этих соединений были разработаны два общих синтетических метода.
Первый метод включал конденсацию о-фенилендиамина с фенилацетонитрилом с образованием 2-бензилбензимидазола. Затем бензимидазол алкилируют желаемым 1-хлор-2-диалкиламиноэтаном с образованием конечного продукта. Эта конкретная процедура была наиболее полезной для получения бензимидазолов, у которых отсутствовали заместители в бензольных кольцах. Схема этого метода представлена ниже.
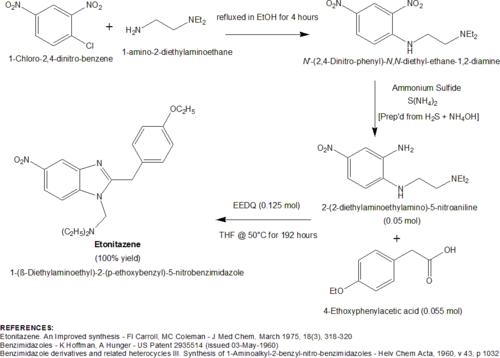
Наиболее универсальный синтез , разработанный швейцарской команды первого участие алкилирования из 2,4-динитрохлорбензола с 1-амино-2-diethylaminoethane с образованием N- (β-диэтиламиноэтил) -2,4-динитроанилин [иначе: N '- (2, 4-Динитрофенил) -N, N-диэтилэтан-1,2-диамин]. Затем 2-нитрозаместитель в соединении 2,4-динитроанилина селективно восстанавливается до соответствующего первичного амина с использованием сульфида аммония в качестве восстанавливающего агента . Сульфид аммония может быть образован in situ путем добавления концентрированного водного гидроксида аммония с последующим насыщением раствора газообразным сероводородом . Промежуточный продукт, образованный селективным восстановлением 2-нитрозаместителя, 2- (β-диэтиламиноэтиламино) -5- нитроанилина , затем реагирует с гидрохлоридной солью иминоэтилового эфира 4- этоксифенилацетонитрила (также известного как п-этоксибензилцианид ). Иминоэфир, гидрохлорид этилового эфира 2- (4-этоксифенил) ацетимидной кислоты , получают растворением 4-замещенного бензилцианида в смеси безводного этанола и хлороформа и затем насыщением этого раствора сухим газообразным хлористым водородом . Реакция между 2- (β-диалкиламиноалкиламином) -5-нитроанилином и HCl-солью иминоэтилового эфира приводит к образованию этонитазена. Эта процедура особенно полезна при получении 4-, 5-, 6- и 7-нитробензимидазолов. Варьируя выбор иминоэфира замещенной фенилуксусной кислоты, получают соединения с разнообразием заместителей в бензольном кольце в положении 2. Схема этого конкретного синтеза применительно к получению этонитазена показана ниже.
Особенно новый высокоэффективный синтез этонитазена был разработан Ф.И. Кэрроллом и М.К. Колеманом в середине 1970-х годов. Авторам было поручено получить большие количества этонитазена, но они обнаружили, что обычный синтез неадекватен. Проблема с обычным синтезом заключалась в лабильности реагента иминоэфира, этилового эфира 2- (4-этоксифенил) ацетимидиновой кислоты (полученного взаимодействием 4-этоксифенилацетонитрила с этанольным HCl). Иминоэфир требовал использования безводных условий реакции, и его было неудобно получать в больших количествах. Это побудило авторов экспериментировать с использованием реагента сочетания, EEDQ (N-этоксикарбонил-2-этокси-1,2-дигидрохинолин), чтобы способствовать конденсации 2- (2-диэтиламиноэтиламино) -5-нитроанилина с 4-этоксифенилуксусная кислота. Невероятно, но авторы обнаружили, что, когда эта конденсация проводилась в присутствии 2 или более молярных эквивалентов EEDQ (добавленных порциями в 3 этапа) в ТГФ при 50 ° C в течение 192 часов (8 дней), почти количественный выход (100% ) этонитазена. В дополнение к впечатляющему увеличению выхода по сравнению с традиционной процедурой, процедура обработки была значительно упрощена, поскольку хинолин , диоксид углерода и этанол были единственными образующимися побочными продуктами. Схема этой процедуры показана ниже.
В публикации 2011 г. [J. Орг. Chem., 2011, 76 (23), 9577-9583] из южнокорейской группы в общих чертах описал новый однореакторный синтез замещенных и незамещенных 2-бензилбензимидазолов, который можно легко адаптировать для получения этонитазола. Трехкомпонентный синтез прямого предшественника этонитазена, 2- (4-этоксибензил) -5-нитро-1H-бензоимидазола, состоит из 2-бром- или 2-йод-5-нитрофениламина (1,0 молярный эквивалент), 4-замещенный бензальдегид (1,2 эквив.) И азид натрия (2 эквив.). 2-Гало-5-нитрофениламин требует наличия бром- или йодной группы для оптимальной активности. 2-Хлорфениламины полностью инертны. В дополнение к этим трем компонентам реакцию оптимизировали в присутствии 0,05 молярных эквивалентов (5 мол.%) Катализатора, хлорида меди (I) и 5 мол.% Лиганда, TMEDA ( тетраметилэтилендиамин ). После нагревания этих компонентов при 120 ° C в течение 12 часов в ДМСО прямой предшественник этонитазена, 2- (4-этоксибензил) -5-нитро-1H-бензоимидазол, образовывался с выходом примерно 80-90%. Вторичный амин азот 2- (4-этоксибензил) -5-нитро-1Н-бензоимидазол затем алкилирует (2-хлорэтил) диэтиламин в виде etonitazene. Схема этого синтеза показана ниже.
Смотрите также
- Этазен (деснитроэтонитазен)