Пиксантрон - Pixantrone
|
|
| Имена | |
|---|---|
|
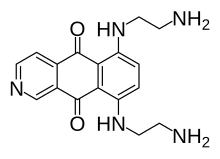
Предпочтительное название IUPAC
6,9-Бис [(2-аминоэтил) амино] бензо [ g ] изохинолин-5,10-дион |
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| DrugBank | |
| КЕГГ | |
|
PubChem CID
|
|
| UNII | |
|
Панель управления CompTox ( EPA )
|
|
|
|
|
|
| Характеристики | |
| C 17 H 19 N 5 O 2 | |
| Молярная масса | 325,365 г / моль |
| Появление | Синее твердое вещество |
| Фармакология | |
| L01DB11 ( ВОЗ ) | |
| Данные лицензии | |
| Внутривенно | |
| Фармакокинетика : | |
| 9,5–17,5 часов | |
| Фекальный (основной путь экскреции) и почечный (4–9%) | |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
Pixantrone ( Rinn ; торговое название Pixuvri ) является экспериментальным противоопухолевым (противораковым) лекарственным средством, аналог по митоксантрону с меньшим количеством токсичных эффектами на сердечной ткани. Он действует как яд топоизомеразы II и интеркалирующий агент . Кодовое название BBR 2778 относится к пиксантрону дималеату , действительному веществу, обычно используемому в клинических испытаниях.
История
Антрациклины - важные химиотерапевтические агенты. Однако их использование связано с необратимыми и кумулятивными повреждениями сердца . Исследователи попытались создать родственные лекарства, которые сохраняют биологическую активность, но не обладают кардиотоксичностью антрациклинов. Пиксантрон был разработан для уменьшения повреждения сердца, связанного с лечением, при сохранении эффективности.
Случайный скрининг в Национальном институте рака США огромного количества соединений, предоставленных Allied Chemical Company, привел к открытию аметантрона, обладающего значительной противоопухолевой активностью. Дальнейшие исследования относительно рациональной разработки аналогов аметантрона привели к синтезу митоксантрона , который также проявлял заметную противоопухолевую активность. Митоксантрон рассматривался как аналог доксорубицина с меньшей структурной сложностью, но с аналогичным механизмом действия. В клинических исследованиях было показано, что митоксантрон эффективен против множества типов опухолей с менее токсичными побочными эффектами, чем те, которые возникают в результате терапии доксорубицином. Однако митоксантрон не был полностью свободен от кардиотоксичности. Был синтезирован ряд структурно модифицированных аналогов митоксантрона и проведены исследования взаимосвязи структура-активность. BBR 2778 первоначально был синтезирован Университета Вермонта исследователи Miles П. Хакер и Пола А. Krapcho и первоначально характеризуется в пробирке для опухолевых клеток цитотоксичности и механизм действия исследований в научно - исследовательском центре Boehringer Mannheim Italia, Монце и Университет штата Вермонт , Burlington . Другие исследования были завершены в Университете Техаса MD Anderson Cancer Center , Хьюстон , в Istituto Nazionale Tumori , Милан , и Падуанского университета . В поисках новых гетероаналогов антрацендионов он был выбран как наиболее многообещающее соединение. Токсикологические исследования показали, что BBR 2778 не является кардиотоксичным, а патенты США принадлежат Университету Вермонта. Дополнительная заявка на патент США была подана в июне 1995 г. компанией Boehringer Mannheim, Италия.
Итальянская компания Novuspharma была основана в 1998 году в результате слияния Boehringer Mannheim и Hoffmann-La Roche , а BBR 2778 был разработан как ведущий противораковый препарат Novuspharma - пиксантрон. Заявка на патент на инъекционный препарат была подана в мае 2003 года.
В 2003 году биотехнологическая компания из Сиэтла Cell Therapeutics приобрела пиксантрон в результате слияния с Novuspharma.
Клинические испытания
Пиксантрон - это вещество, которое изучается для лечения рака. Он принадлежит к семейству препаратов, называемых противоопухолевыми антибиотиками. III фаза клинических испытаний пиксантрона завершена. Пиксантрон изучается как противоопухолевое средство при различных видах рака , включая солидные опухоли и гематологические злокачественные новообразования, такие как неходжкинские лимфомы .
Исследования на животных показали, что пиксантрон не усугубляет ранее существовавшее повреждение сердечной мышцы, предполагая, что пиксантрон может быть полезен для пациентов, предварительно получавших антрациклины. В то время как у мышей, получавших повторные циклы пиксантрона, наблюдаются лишь минимальные сердечные изменения, 2 цикла традиционных антрациклинов, доксорубицина или митоксантрона, приводят к выраженной или тяжелой дегенерации сердечной мышцы.
Клинические испытания замены пиксантрона на доксорубицин в стандартной терапии первой линии пациентов с агрессивной неходжкинской лимфомой показали снижение тяжелых побочных эффектов по сравнению с пациентами, получавшими стандартную терапию на основе доксорубицина. Несмотря на то, что пациенты с пиксантроном получали больше циклов лечения, наблюдалось трехкратное снижение частоты серьезных повреждений сердца, а также клинически значимое снижение инфекций и тромбоцитопении, а также значительное снижение фебрильной нейтропении. Эти результаты могут иметь большое значение для лечения пациентов с раком груди, лимфомой и лейкемией, где можно предотвратить изнурительное повреждение сердца от доксорубицина. Предыдущие варианты лечения многократно рецидивирующей агрессивной неходжкинской лимфомы имели неутешительные результаты.
В завершенном исследовании фазы II RAPID сравнивали схему CHOP-R циклофосфамида, доксорубицина, винкристина, преднизона и ритуксимаба с той же схемой, но с заменой доксорубицина на пиксантрон. Цель заключалась в том, чтобы показать, что Пиксантрон не уступает доксорубицину и менее токсичен для сердца.
Было показано, что пиксантрон потенциально снижает кардиотоксичность и продемонстрировал многообещающую клиническую активность в этих исследованиях фазы II у пациентов с неходжкинской лимфомой, подвергавшихся тщательному предварительному лечению .
Основное рандомизированное клиническое исследование фазы III EXTEND (PIX301) изучало пиксантрон, чтобы увидеть, насколько хорошо он работает по сравнению с другими химиотерапевтическими препаратами при лечении пациентов с рецидивирующей неходжкинской лимфомой. Частота полного ответа у пациентов, получавших пиксантрон, была значительно выше, чем у пациентов, получавших другие химиотерапевтические агенты для лечения рецидивирующей / рефрактерной агрессивной неходжкинской лимфомы .
Администрация
Его можно вводить через периферическую вену, а не через центральный имплантированный катетер, как это требуется для других подобных препаратов.
Нормативное одобрение
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США
FDA предоставило ускоренное назначение пиксантрона пациентам, которые ранее лечились два или более раза по поводу рецидивной или рефрактерной агрессивной НХЛ. Спонсор исследования компания Cell Therapeutics объявила, что Pixantrone достиг основной конечной точки эффективности. Протокол заседания Консультативного комитета по онкологическим препаратам от 22 марта 2010 г. показывает, что на самом деле это не было достигнуто со статистической значимостью, и это в сочетании с серьезными проблемами безопасности привело к выводу, что исследования было недостаточно для поддержки утверждения. В апреле 2010 года FDA запросило дополнительное исследование.
Европейское агентство по лекарственным средствам
5 мая 2009 года Pixantrone стал доступен в Европе для именных пациентов. Программа поименного пациента - это программа обеспечения лекарствами из сострадания, в рамках которой врачи могут на законных основаниях поставлять исследуемые лекарства подходящим пациентам. В рамках программы с указанием имен пациентов исследуемые препараты могут вводиться пациентам, страдающим серьезными заболеваниями, до того, как препарат будет одобрен Европейским агентством по оценке лекарственных средств. Распространение «именованный пациент» относится к распределению или продаже продукта конкретному специалисту в области здравоохранения для лечения отдельного пациента. В Европе в рамках программы поименованных пациентов лекарство чаще всего закупается через национальную систему здравоохранения. В 2012 году пиксантрон получил условное разрешение на продажу в Европейском союзе в качестве монотерапии для лечения взрослых пациентов с множественными рецидивирующими или рефрактерными агрессивными неходжкинскими В-клеточными лимфомами.
Исследовать
Пиксантрон так же эффективен, как митоксантрон в моделях рассеянного склероза на животных . Пиксантрон имеет такой же механизм действия, как митоксантрон, на эффекторную функцию лимфомоноцитов B и T при экспериментальном аллергическом энцефаломиелите, но с меньшей кардиотоксичностью. Пиксантрон подавляет антиген-специфическую и митоген-индуцированную пролиферацию лимфомононуклеарных клеток, а также продукцию IFN-гамма. Клинические испытания в настоящее время продолжаются в Европе.
Пиксантрон также снижает тяжесть экспериментальной аутоиммунной миастении у крыс Льюиса, а эксперименты по жизнеспособности клеток in vitro показали, что Пиксантрон значительно снижает нейротоксичность бета-амилоида (A бета (1-42)), механизма, причастного к болезни Альцгеймера .
