Myxobolus cerebralis -Myxobolus cerebralis
| Myxobolus cerebralis | |
|---|---|
|
|
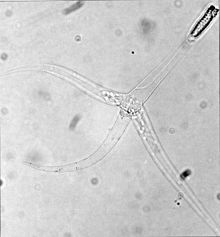
| Триактиномиксонная стадия Myxobolus cerebralis - обратите внимание на три «хвоста» | |
|
Научная классификация |
|
| Королевство: | Animalia |
| Тип: | Книдария |
| Класс: | Миксоспорея |
| Порядок: | Bivalvulida |
| Семья: | Myxobolidae |
| Род: | Миксобол |
| Разновидность: |
М. cerebralis
|
| Биномиальное имя | |
|
Myxobolus cerebralis
Хофер , 1903 год.
|
|
| Синонимы | |
|
Myxosoma cerebralis |
|
Myxobolus cerebralis является myxosporean паразит из лососевых ( лосось , форель , и их союзников)что вызывает вихревое болезнь в выращиваемых лосося и форелиа также в популяциях диких рыб . Впервые он был описан у радужной форели в Германии столетие назад, но его ареал распространился, и он появился в большинстве стран Европы (включая Россию), США, Южной Африке, Канаде и других странах. В 1980-х годахбыло обнаружено, что M. cerebralis требуется тубифицидный олигохет (разновидность сегментированного червя ) для завершения своего жизненного цикла. Паразит заражает своих хозяев своими клетками после протыкания их полярными филаментами, выброшенными изкапсул, похожих на нематоцисты .
Болезнь кружения поражает молодь рыб (мальков и мальков) и вызывает деформацию скелета и неврологические нарушения. Рыбы «кружатся» вперед неуклюжим, похожим на штопор, вместо обычного плавания, им трудно кормиться, и они более уязвимы для хищников . Смертность молоди высока, до 90% инфицированных популяций, а те, что выживают, деформируются паразитами, живущими в их хрящах и костях . Они действуют как резервуар для паразита, который попадает в воду после смерти рыбы. M. cerebralis - один из наиболее экономически важных микозоидов в рыбе, а также один из самых патогенных. Это был первый миксоспориан, патология и симптомы которого были описаны научно. Паразит не передается человеку.
Таксономия
Систематики и наименование обоих М. cerebralis , и myxozoans в целом, имеют сложную историю. Первоначально считалось, что он заражает мозг рыб (отсюда и особый эпитет cerebralis ) и нервную систему , хотя вскоре было обнаружено, что он поражает в первую очередь хрящевую и скелетную ткань . Попытки изменить название на Myxobolus chondrophagus , которое более точно описывало бы организм, не увенчались успехом из-за правил номенклатуры . Позже было обнаружено , что организмы, ранее называвшиеся Triactinomyxon dubium и T. gyrosalmo ( класс Actinosporea ), фактически являются стадиями триактиномиксона M. cerebralis , жизненный цикл которых был расширен за счет включения стадии триактиномиксона. Точно так же другие актиноспориевые были включены в жизненные циклы различных миксоспориев.
Сегодня миксозои, которые ранее считались многоклеточными простейшими , большинством ученых считаются животными , хотя их статус официально не изменился. Недавние молекулярные исследования показывают, что они связаны с Bilateria или Cnidaria , причем Cnidaria более близки морфологически, потому что обе группы имеют экструзионные волокна. Bilateria были несколько ближе в некоторых генетических исследованиях, но было обнаружено, что в них использовались образцы, загрязненные материалом из организма-хозяина, и исследование 2015 года подтверждает, что они книдарии.
Морфология
M. cerebralis имеет множество различных стадий, от единичных клеток до относительно крупных спор, не все из которых были подробно изучены.
Стадия триактиномиксона
Стадии, поражающие рыбу, называемые спорами триактиномиксона , состоят из одного типа, длина которого составляет около 150 микрометров (мкм), и трех отростков, или «хвостов», каждый длиной около 200 микрометров. Пакет спороплазмы в конце стиля содержит 64 половых клетки, окруженные клеточной оболочкой. Также имеются три полярные капсулы , каждая из которых содержит свернутую в спираль полярную нить длиной от 170 до 180 мкм. Полярные нити как на этой стадии, так и на стадии миксоспор (см. Рисунок выше) быстро проникают в тело хозяина, создавая отверстие, через которое может проникнуть спороплазма.
Стадия спороплазмы
При контакте с рыбами-хозяевами и срабатывании полярных капсул спороплазма, содержащаяся в центральной части триактиномиксона, мигрирует в эпителий или слизистую оболочку кишечника. Во-первых, эта спороплазма подвергается митозу с образованием большего количества амебоидных клеток, которые мигрируют в более глубокие слои ткани, чтобы достичь церебрального хряща.
Миксоспорианская стадия
Миксоспоры, которые развиваются на стадиях спорогонных клеток внутри рыб-хозяев, имеют линзовидную форму. Они имеют диаметр около 10 микрометров и состоят из шести ячеек. Две из этих клеток образуют полярные капсулы, две сливаются, образуя двухъядерную спороплазму, а две образуют защитные клапаны. Миксоспоры являются инфекционными для олигохет и обнаруживаются среди остатков переваренного хряща рыб. Их часто трудно отличить от родственных видов из-за морфологического сходства между родами . Хотя M. cerebralis является единственным миксоспорином, когда-либо обнаруженным в хряще лосося, другие визуально похожие виды могут присутствовать в коже, нервной системе или мышцах .
Жизненный цикл
Myxobolus cerebralis имеет жизненный цикл с двумя хозяевами, включая лососевую рыбу и тубифицид-олигохет. Пока известно, что единственным червем, подверженным инфекции M. cerebralis, является Tubifex tubifex , хотя то, что ученые в настоящее время называют T. tubifex, на самом деле может относиться к нескольким видам. Сначала миксоспоры попадают в организм тубифицидных червей. В кишечнике просвете червя, споры выталкивать их полярные капсулы и прикрепляются к кишечному эпителию на полярных филаментах . Затем створчатые клапаны открываются вдоль линии шва, и двуядерные зародышевые клетки проникают между эпителиальными клетками кишечника червя. Эта клетка размножается, производя множество амебоидных клеток в процессе бесполого деления клеток, называемого мерогонией . В результате процесса размножения может инфицироваться межклеточное пространство эпителиальных клеток более чем в 10 соседних сегментах червя.
Примерно через 60–90 дней после инфицирования стадии половых клеток паразита подвергаются спорогенезу и развиваются в панспороцисты , каждая из которых содержит восемь спор стадии триактиномиксона. Эти споры попадают из ануса олигохет в воду. Кроме того, рыба может заразиться, съев инфицированного олигохета. Зараженные тубифициды могут выделять триактиномиксоны не менее года. Споры триактиномиксона переносятся водными потоками, где они могут заразить лосося через кожу. Проникновение этих споров в рыбу занимает всего несколько секунд. В течение пяти минут мешок половых клеток, называемый спороплазмой , вошел в эпидермис рыбы , и в течение нескольких часов спороплазма распадается на отдельные клетки, которые распространяются по рыбе.
Внутри рыбы как внутриклеточная, так и внеклеточная стадия воспроизводятся в ее хряще путем бесполого эндогения , что означает рост новых клеток из старых клеток. Заключительный этап у рыб - образование миксоспор, которые образуются спорогонией . Они выбрасываются в окружающую среду, когда рыба разлагается или поедается. Некоторые недавние исследования показывают, что некоторые рыбы могут выделять жизнеспособные миксоспоры еще при жизни.
Миксоспоры чрезвычайно прочны: «было показано, что споры Myxobolus cerebralis могут выдерживать замораживание при -20 ° C в течение как минимум 3 месяцев, старение в грязи при 13 ° C в течение как минимум 5 месяцев и прохождение через кишечник северной щуки Esox lucius. или кряквы Anas platyrhynchos без потери заразности "глистам". Триактиномиксоны намного короче, выживают 34 дня или меньше, в зависимости от температуры.
Патология

Об инфекциях M. cerebralis сообщалось от широкого круга видов лососевых: восемь видов «атлантических» лососевых, Salmo ; четыре вида «тихоокеанских» лососевых - Oncorhynchus ; четыре вида голца, Salvelinus ; хариус Thymallus thymallus ; и Huchen, Таймень Таймень . M. cerebralis наносит вред своим рыбам-хозяевам за счет прикрепления спор триактиномиксона и миграции различных стадий через ткани и по нервам, а также путем переваривания хрящей. Хвост рыбы может потемнеть, но, за исключением повреждений хряща, внутренние органы в целом выглядят здоровыми. К другим симптомам относятся деформации скелета и «кружащееся» поведение (погоня за хвостом) у молоди рыбы, которое, как считалось, было вызвано потерей равновесия, но на самом деле вызвано повреждением спинного мозга и нижней части ствола мозга. Эксперименты показали, что рыба может убить миксоболуса в своей коже (возможно, с помощью антител ), но рыба не атакует паразитов, когда они мигрируют в центральную нервную систему. Эта реакция варьируется от вида к виду.
У T. tubifex высвобождение спор триактиномиксона из кишечной стенки повреждает слизистую оболочку червя ; это может происходить тысячи раз с одним червем и, как полагают, ухудшает усвоение питательных веществ. Споры выделяются из червя почти исключительно при температуре от 10 ° C до 15 ° C, поэтому рыба в более теплых или прохладных водах с меньшей вероятностью заразится, а уровень заражения меняется в зависимости от сезона.
Восприимчивость
Размер рыбы, возраст, концентрация спор триактиномиксона и температура воды - все это влияет на уровень заражения рыб, как и виды рассматриваемых рыб. Болезнь больше всего поражает рыб младше пяти месяцев, потому что их скелет не окостенел . Это делает молодь более восприимчивой к деформациям и дает M. cerebralis больше хрящей, которыми они могут питаться. В одном исследовании семи видов многих штаммов ручья и радужная форель (за исключением одного штамма) были значительно сильнее поражены M. cerebralis после двух часов воздействия, чем другие виды, в то время как форель , чавычи , кумжа и В наименьшей степени пострадали арктический хариус . Хотя кумжа может укрывать паразита, обычно она не проявляет никаких симптомов, и этот вид, возможно, был первоначальным хозяином M. cerebralis . Отсутствие симптомов у коричневой форели означало, что паразит был обнаружен только после того, как в Европе была завезена неместная радужная форель.
Диагностика
Умеренное или тяжелое клиническое заражение рыб вихревой болезнью можно предположительно диагностировать на основании изменений в поведении и внешнем виде примерно через 35-80 дней после первоначального заражения, хотя «травма или дефицит триптофана и аскорбиновой кислоты в пище может вызывать аналогичные признаки», поэтому для окончательного диагноза может потребоваться обнаружение миксоспор в хрящах рыбы. При тяжелых инфекциях может потребоваться только микроскопическое исследование хряща для обнаружения спор. При менее тяжелых инфекциях наиболее распространенный тест включает переваривание краниального хряща протеазами пепсином и трипсином (пепсин-трипсиновый перевар - PTD) перед поиском спор. Голова и другие ткани могут быть дополнительно исследованы с помощью гистопатологии, чтобы подтвердить, соответствуют ли расположение и морфология спор тому, что известно для M. cerebralis . Также возможна серологическая идентификация спор в срезах тканей с использованием антител, индуцированных против спор. Идентичность паразита также может быть подтверждена с помощью полимеразной цепной реакции для амплификации гена 18S рРНК из 415 пар оснований из M. cerebralis . Рыбу следует проверять на наиболее восприимчивой к паразитам стадии жизни, уделяя особое внимание рыбе в аквакультурных хозяйствах.
Влияние

Хотя изначально это был легкий патоген Salmo trutta в Центральной Европе и других лососевых в Северо-Восточной Азии, интродукция радужной форели ( Oncorhynchus mykiss ) значительно увеличила воздействие этого паразита. Не обладая врожденным иммунитетом к M. cerebralis , радужная форель особенно восприимчива и может выделять столько спор, что даже более устойчивые виды в том же районе, такие как S. trutta , могут быть перегружены паразитами и вызывать гибель 80–90% . Там, где M. cerebralis хорошо прижились, это привело к сокращению или даже исчезновению целых когорт рыб.
Воздействие в Европе
Влияние M. cerebralis в Европе несколько ослаблено, поскольку этот вид является эндемичным для этого региона, что дает местным рыбным запасам определенную степень иммунитета . Радужная форель, наиболее восприимчивый к этому паразиту вид, не является родным для Европы; Успешно воспроизводящиеся дикие популяции встречаются редко, поэтому немногие дикой радужной форели достаточно молоды, чтобы быть восприимчивыми к инфекции. С другой стороны, их широко разводят для пополнения запасов водоемов для спортивной рыбалки и для аквакультуры , где этот паразит оказывает наибольшее влияние. Методы вылупления и выращивания, разработанные для предотвращения заражения мальков радужной форели, оказались успешными в Европе. Эти методы включают инкубацию яиц в воде, свободной от спор, и выращивание мальков до стадии «окостенения» в резервуарах или желобах. Эти методы уделяют особое внимание качеству источников воды, чтобы предотвратить попадание спор во время водообмена. Мальков переводят в земляные пруды только после того, как они будут признаны клинически устойчивыми к паразиту, после того как произойдет окостенение скелета.
Воздействие в Новой Зеландии
M. cerebralis был впервые обнаружен в Новой Зеландии в 1971 году. Паразит был обнаружен только в реках Южного острова, вдали от наиболее важных участков аквакультуры. Кроме того, виды лососевых, выращиваемые в коммерческой аквакультуре в Новой Зеландии, имеют низкую восприимчивость к вихревой болезни, и также не было показано, что паразит влияет на местных лососевых. Важным косвенным эффектом присутствия паразитов является карантинное ограничение на экспорт продукции из лосося в Австралию.
Воздействие в США

M. cerebralis был впервые зарегистрирован в Северной Америке в 1956 году в Пенсильвании , был занесен через инфицированную форель, импортированную из Европы, и неуклонно распространился на юг и запад. До 1990-х годов водоворот считался управляемой проблемой, поражающей радужную форель в инкубаториях. Однако недавно он установился в естественных водах штатов Роки-Маунтин ( Колорадо , Вайоминг , Юта , Монтана , Айдахо , Нью-Мексико ), где он вызывает тяжелую смертность в нескольких реках для спортивной рыбалки. Некоторые ручьи на западе США потеряли 90% своей форели. Кроме того, вихревая болезнь угрожает любительскому рыболовству, которое имеет важное значение для индустрии туризма, ключевого компонента экономики некоторых западных штатов США. Например, « Целевая группа по вихревым болезням штата Монтана подсчитала, что вылов форели только в одной Монтане привел к затратам на отдых в 300 000 000 долларов США». Что еще хуже, некоторые виды рыб, зараженных M. cerebralis ( бычья форель , головорезная форель и стальная голова ), уже находятся под угрозой исчезновения , и паразит может ухудшить их и без того опасное положение. По причинам, которые плохо изучены, но, вероятно, связаны с условиями окружающей среды, наибольшее воздействие на инфицированных рыб было в Колорадо и Монтане, а меньше всего - в Калифорнии , Мичигане и Нью-Йорке.
Воздействие в Канаде
Болезнь вихря была впервые обнаружена у рыб в озере Джонсон в национальном парке Банф в мае 2016 года. Лаборатория CFIA подтвердила это в августе, а компания Parks Canada объявила о вспышке 23 августа 2016 года. Хотя впервые она была обнаружена в Банфе, не обязательно, где болезнь возникла и распространилась. Правительство Альберты в настоящее время отбирает и тестирует рыбу в 6 различных водоразделах (река Пис, Атабаска, Северный Саскачеван, Ред-Дир, Боу и Олдман), чтобы выяснить, где распространилась болезнь. Первоначальные образцы рыбы были собраны в 2016 году и в настоящее время обрабатываются в лабораториях правительства Альберты и CFIA. С начала испытаний он был обнаружен в реке Верхний Боу, а в мае 2017 года было подтверждено, что вихревая болезнь также была обнаружена в бассейне реки Олдман. Заявление не означает, что все восприимчивые популяции рыб в бассейнах рек Боу и Олдман инфицированы этой болезнью.
В результате новой декларации от CFIA потребуется разрешение на внутреннее перемещение для восприимчивых видов и конечного использования, определенных в Программе контроля внутреннего перемещения, переносчика Tubifex tubifex , возбудителя болезни Myxobolus cerebralis и / или связанных с ними вещей. зараженных и буферных зон Альберты. Для любительского и спортивного рыболовства, включая рыбалку под руководством профессионального гида, разрешение CFIA не требуется.
Профилактика и контроль
Некоторые биологи пытались обезвредить споры триактиномиксона, заставляя их загораться преждевременно. В лаборатории только чрезмерная кислотность или основность , умеренная или высокая концентрация солей или электрический ток вызывали преждевременный разряд нити накала; нейрохимические препараты, хемосенсибилизаторы книдарий и слизь форели были неэффективными, как и анестезированная или мертвая рыба. Если бы споры можно было обезвредить, они не смогли бы заразить рыбу, но необходимы дальнейшие исследования, чтобы найти эффективное лечение.
Некоторые виды рыб более устойчивы, чем другие, даже внутри вида; использование устойчивых штаммов может помочь снизить частоту и серьезность вихревой болезни в аквакультуре. Есть также некоторые косвенные доказательства того, что популяции рыб могут со временем развить устойчивость к болезни. Кроме того, аквакультуры могут избежать заражения M. cerebralis , не используя земляные пруды для выращивания молоди; это защищает их от возможно инфицированных тубифицидов и упрощает удаление спор и олигохет с помощью фильтрации, хлорирования и ультрафиолетовой бомбардировки. Чтобы свести к минимуму популяции тубифицидов, методы включают периодическую дезинфекцию инкубатория или прудов для аквакультуры, а также выращивание мелкой форели в закрытых помещениях в воде, свободной от патогенов. Гладкие бетонные или облицованные пластиком кабельные каналы, которые содержатся в чистоте и не содержат загрязненной воды, защищают объекты аквакультуры от болезней.
Наконец, было показано , что некоторые лекарства, такие как фуразолидон , фуроксон , беномил , фумагиллин , прогуанил и хламоксихин , препятствуют развитию спор, что снижает уровень инфицирования. Например, одно исследование показало, что кормление O. mykiss фумагиллином снижает количество инфицированных рыб с 73% до 100% до 10-20%. К сожалению, это лечение считается неподходящим для популяций дикой форели, и ни одно лекарственное лечение не показало свою эффективность в исследованиях, необходимых для одобрения Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США .
Рыбаки-любители и спортивные рыбаки могут помочь предотвратить распространение паразита, не перевозя рыбу из одного водоема в другой, не выбрасывая рыбьи кости или внутренности в какой-либо водоем и обеспечивая чистоту обуви перед перемещением между разными телами. воды. Следует соблюдать федеральные, государственные, провинциальные и местные правила использования наживки .
Смотрите также
- Ceratomyxa shasta - еще один патогенный миксоспориевый паразит лососевых.
- Инфекционная анемия лосося (ИЗА) - вирусная инфекция атлантического лосося.
- Тирзиты кудоа - миксоспориевые паразиты многих видов, которые вызывают разжижение тканей рыб после смерти.
- Tetracapsuloides bryosalmonae - загадочный миксоспориан, вызывающий «пролиферативное заболевание почек» у лососевых.
- Восприимчивость лососевых к вихревой болезни
Примечания
внешние ссылки
- Доклад Всемирной торговой организации об ограничениях Австралии на импорт лосося
- Инициатива по вихревой болезни
- Карты и данные по вихревой болезни
- Профиль видов - Вихревая болезнь ( Myxobolus cerebralis ) , Национальный информационный центр по инвазивным видам, Национальная сельскохозяйственная библиотека США , содержит общую информацию и ресурсы по вихревой болезни.
- Вихревая болезнь - Йеллоустонский национальный парк (Служба национальных парков США)
- Вихревая болезнь - остановите водных автостопщиков
- Болезнь Вихря - Отдел природных ресурсов штата Юта
- Парки и дикая природа Колорадо - вихревая болезнь и колорадская форель
- Что такое кружащаяся болезнь? - Северный центральный региональный центр аквакультуры - Мохамед Фейсал - Дональд Гарлинг
- Вихревая болезнь | Alberta.ca



