Гем А - Heme A
|
|
|||
| Имена | |||
|---|---|---|---|
| Другие имена
Цитопорфирин железа IX, формилпорфирин
|
|||
| Идентификаторы | |||
|
3D модель ( JSmol )
|
|||
| ChemSpider | |||
| MeSH | Heme + a | ||
|
PubChem CID
|
|||
|
Панель управления CompTox ( EPA )
|
|||
|
|||
|
|||
| Характеристики | |||
| C 49 H 56 O 6 N 4 Fe | |||
| Молярная масса | 852,837 | ||
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|||
|
|
|||
| Ссылки на инфобоксы | |||
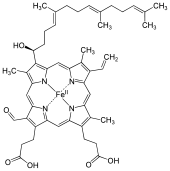
Гем А (или гем А ) представляет собой гем , координационный комплекс, состоящий из макроциклического лиганда, называемого порфирином , хелатирующего атом железа. Гем А - это биомолекула, которую в естественных условиях вырабатывают многие организмы. Гем A, который в растворе часто имеет дихроичный зеленый / красный цвет, является структурным родственником гема B , компонента гемоглобина , красного пигмента в крови.
Отношение к другим гемам
Гем А отличается от гема В тем, что метильная боковая цепь в положении 8 кольца окисляется до формильной группы, а гидроксиэтилфарнезильная группа , изопреноидная цепь, присоединена к винильной боковой цепи в положении 2 кольца гема тетрапиррола железа . Гем A подобен гему o , в том, что оба имеют это фарнезильное присоединение в положении 2, но гем O не имеет формильной группы в положении 8, все еще содержащей метильную группу. Правильная структура гема А, основанная на экспериментах ЯМР и ИК восстановленной формы гема Fe (II), была опубликована в 1975 году. Структура была подтверждена синтезом диметилового эфира в форме, не содержащей железа.
История
Гем А был впервые выделен немецким биохимиком Отто Варбургом в 1951 году и показал, что он является активным компонентом интегральной мембранной металлопротеиновой цитохром с оксидазы.
Стереохимия
Последний структурный вопрос о точной геометрической конфигурации первого атома углерода в положении 3 кольца I, углерод, связанный с гидроксильной группой, был недавно опубликован как хиральная S-конфигурация.
Подобно гему B, гем A часто присоединяется к апопротеину посредством координационной связи между железом гема и консервативной боковой цепью аминокислоты. В важной респираторной белковой цитохром с оксидазе (CCO) этот лиганд 5 для гема A в кислородном реакционном центре представляет собой гистидильную группу. Это общий лиганд для многих гемопротеинов, включая гемоглобин и миоглобин .

Гем А в цитохроме - часть циктохрома с-оксидазы, связанная двумя остатками гистидина (показаны розовым цветом ).
Примером металлопротеина, содержащего гем А, является цитохром с оксидаза. Этот очень сложный белок содержит гем А на двух разных участках, каждый из которых выполняет свою функцию. Железо гема А цитохрома а гексакоординировано, то есть связано с 6 другими атомами. Железо гема А цитохрома а3 иногда связывается с 5 другими атомами, оставляя шестой участок доступным для связывания дикислорода (молекулярного кислорода ). Кроме того, этот фермент связывает 3 меди, магний, цинк и несколько ионов калия и натрия. Считается, что две группы гема A в CCO легко обмениваются электронами между собой, ионами меди и тесно связанным белком цитохромом c.
Считается, что как формильная группа, так и изопреноидная боковая цепь играют важную роль в сохранении энергии восстановления кислорода цитохром с оксидазой . Считается, что CCO отвечает за сохранение энергии восстановления двуокиси кислорода путем перекачки протонов в межмембранное пространство митохондрий. Считается, что как формильная, так и гидроксиэтилфарнезильная группы гема А играют важную роль в этом критическом процессе, как опубликовано влиятельной группой С. Йошикавы.
Смотрите также
- Гем
- Гемопротеин
- Цитохром с оксидаза (комплекс IV клеточного дыхания )