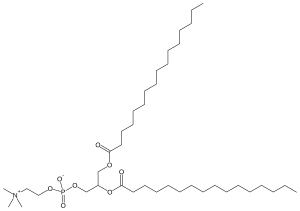
Дипальмитоилфосфатидилхолин - Dipalmitoylphosphatidylcholine
|
|
| Идентификаторы | |
|---|---|
|
3D модель ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.018.322 |
|
PubChem CID
|
|
| UNII | |
|
Панель управления CompTox ( EPA )
|
|
|
|
|
|
| Характеристики | |
| C 40 H 80 N O 8 P | |
| Молярная масса | 734,053 г · моль -1 |
| Поверхностное натяжение: | |
| 4,6 ± 0,5 х 10 -10 М | |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
Дипальмитоилфосфатидилхолин ( DPPC ) представляет собой фосфолипид (и лецитин ), состоящий из двух групп C 16 пальмитиновой кислоты, присоединенных к головной группе фосфатидилхолина .
Это основной компонент легочных сурфактантов, который снижает работу дыхания и предотвращает коллапс альвеол во время дыхания. Он также играет важную роль в изучении липосом и бислоев человека.
Сурфактант легких
Сурфактант легких (LS) - это поверхностно-активный материал, производимый большинством дышащих воздухом животных с целью снижения поверхностного натяжения слоя воды, в котором происходит газообмен в легких, учитывая, что движения при вдохе и выдохе могут вызвать повреждение. если энергии недостаточно для поддержания структурной целостности альвеол.
Монослой, образованный LS на границе раздела, состоит в основном из фосфолипидов (80%), а также белков (12%) и нейтральных липидов (8%). Среди фосфолипидов наиболее распространенным является фосфатидилхолин (PC или лецитин) (70–85%), который, в свою очередь, составляет основу пула подобных диацилфатидилхолинов, из которых 50% составляет дипальмитоилфосфатидилхолин или DPPC.
Хотя сам DPPC уже обладает способностью снижать поверхностное натяжение альвеолярной жидкости, белки и другие липиды в поверхностно-активном веществе дополнительно способствуют адсорбции кислорода на границе раздела воздух-жидкость.
DPPC представляет собой вариант фосфатидилхолина. В его структуру входят как гидрофильная «голова», так и гидрофобные «хвосты», и именно такое расположение позволяет снизить поверхностное натяжение водного слоя. Холиновый радикал составляет полярную гидрофильную головку; он ориентирован на альвеолярную жидкость и распространяется в нее. Цепи пальмитиновой кислоты (C 16 ) образуют неполярные гидрофобные хвосты; они ориентированы на внешнюю сторону.
Биосинтез
Синтез фосфолипидов, содержащихся в легочном сурфактанте, происходит в эндоплазматическом ретикулуме пневмоцитов II типа. Легочный сурфактант имеет как белковые, так и липидные компоненты. В частности, было обнаружено, что фосфатидилхолин (PC) является наиболее распространенным фосфолипидом (70–85%), и что PC в основном присутствует в виде дипальмитоилфосфатидилхолина (DPPC).
Синтез de novo фосфатидилхолина в легких происходит главным образом из цитидиндифосфат-холина (ЦДФ-холина). Превращение ЦДФ-холина в фосфатидилхолин осуществляется холинфосфатцитидилтрансферазой. При определенных условиях ферменты холинкиназа, глицерин-3-фосфатацилтрансфераза и фосфатидатфосфатаза могут играть регулирующую роль.
Из общего количества DPPC в легочном сурфактанте 45% приходится на биосинтез de novo . Остальное образуется механизмами трансацилирования, которые обменивают пальмитоильные группы на ненасыщенные ацильные цепи других родственных диацилфосфатидилхолинов. Удаление ацильных цепей из этих родственных соединений дает лизофосфатидилхолин; Реацилирование пальмитоил-КоА затем облегчается лизофосфатидилхолинацилтрансферазой с образованием DPPC.
Характеристики

Температура
Этот фосфолипид находится в твердой / гелевой фазе при 37 ° C (при эффективной температуре человеческого тела). Его температура плавления составляет около 41,3 ° C. Следовательно, когда температура выше 41 ° C, DPPC больше не находится в гелевой фазе, а в жидкой.
Было продемонстрировано, что при контакте с поверхностями диоксида кремния бислои DPPC имеют разные свойства в зависимости от температуры.
Толщина слоя остается неизменной при 25 ° C и 39 ° C. Однако при дальнейшем повышении температуры до 55 ° C двухслойная структура DPPC значительно изменяется, что вызывает уменьшение толщины слоя. Причина этой особенности заключается в том, что фактически при 55 ° C DPPC находится в неупорядоченном жидком состоянии, тогда как при более низкой температуре он находится в более упорядоченном гелевом состоянии.
Температура также влияет на шероховатость слоя, которая начинает незначительно изменяться при понижении температуры до 25 ° C.
Наконец, несущая способность бислоя выше, когда температура превышает температуру фазового перехода (из-за его повышенной текучести). Когда эта молекула находится в жидком состоянии, где текучесть намного выше, считается, что бислой также развивает способность к самовосстановлению.
Амфипатическое поведение
DPPC - это амфипатический липид. Эта характеристика обусловлена его гидрофильной головкой, состоящей из полярной фосфатидилхолиновой группы, и его гидрофобными хвостами, образованными двумя неполярными цепями пальмитиновой кислоты (C 16 ). Эта особенность позволяет DPPC легко и спонтанно образовывать мицеллы, монослои, бислои и липосомы при контакте с полярным растворителем.
Поверхностно-активное вещество
DPPC является основным фосфолипидом легочного сурфактанта, и он является поверхностно-активным из-за его амфипатического поведения и его адсорбционной способности. Однако адсорбция не является оптимальной при температуре человеческого тела только для DPPC, поскольку при 37 ° C он находится в гелеобразной фазе. Присутствие некоторых ненасыщенных фосфолипидов (таких как диолеоилфосфатидилхолин [DOPC] или фосфатидилглицерин ) и холестерина увеличивает текучесть поверхностно-активного вещества, поэтому оно может более эффективно адсорбировать кислород. Когда эта смесь контактирует с водой, например, она накапливается на границе раздела вода-воздух и образует тонкую поверхностную пленку поверхностно-активного вещества. Полярные головки молекул, составляющих поверхностно-активное вещество, притягиваются полярными молекулами жидкости (в данном случае молекулами H 2 O), вызывая значительное уменьшение поверхностного натяжения воды.
Текущее использование
Исследования используют
DPPC обычно используется для исследовательских целей, таких как создание липосом и бислоев, которые используются в более крупных исследованиях. Метод Ленгмюра-Блоджетт позволяет синтезировать липосомальные ДПФЕ бислой. В настоящее время эти липосомы используются для изучения свойств этого фосфатидилхолина и его использования в качестве механизма доставки лекарств в человеческий организм.
Кроме того, поскольку динамика слияния везикул для липидов в гелевой фазе отличается от жидкой фазы, это позволяет ученым использовать DPPC вместе с DOPC в атомно-силовой микроскопии и атомно-силовой спектроскопии.
Фармацевтическое использование
Дипальмитоилфосфатидилхолин (DPPC) обычно используется для приготовления некоторых лекарств, используемых для лечения респираторного дистресс-синдрома (RDS) у новорожденных. Современные синтетические поверхностно-активные вещества представляют собой комбинации DPPC вместе с другими фосфолипидами, нейтральными липидами и липопротеинами .
Лечение недоношенных детей с РДС с помощью сурфактантов было первоначально разработано в 1960-х годах, и недавние исследования продемонстрировали улучшение клинических исходов. Первым лечением некоторых новорожденных с РДС были поверхностно-активные фосфолипиды, в частности DPPC, с помощью аэрозоля (Robillard, 1964). Однако это лечение оказалось неэффективным, поскольку введение одного только DPPC не дало никаких положительных эффектов. Впоследствии были проведены различные исследования, чтобы попытаться найти более эффективные препараты для лечения этого заболевания.
Легочные сурфактанты можно разделить на три типа:
Безбелковые синтетические поверхностно-активные вещества первого поколения содержали только DPPC. Самый известный из них - пальмитат колфосцерил .
Второе поколение поверхностно-активных веществ было естественного (животного) происхождения и было получено из легких крупного рогатого скота или свиней. Поверхностно -активные вещества , извлеченные из бычьих легких были Infasurf и Alvofact , экстракты свиного легкого включены Curosurf , и те из модифицированных бычьих экстрактов легких , включенный Survanta или Beraksurf ( Beractant ). В отличие от новорожденных с РДС, которым вводили препараты первого поколения, тем, кого лечили этими сурфактантами второго поколения, требовалось меньше кислорода и респираторной поддержки в течение 72 часов после введения препарата.
Третье поколение поверхностно-активных веществ включает синтетические пептиды или рекомбинантные белки. В них используется смесь различных компонентов. DPPC - это агент, используемый для уменьшения поверхностного натяжения, а остальные компоненты способствуют увеличению адсорбции кислорода. Наиболее известны Venicute и Surfaxin. Эти препараты все еще находятся в стадии разработки, поэтому пока нет доказательств того, обладают ли они преимуществами по сравнению с препаратами второго поколения.
DPPC также используется для образования липосом , которые используются в качестве компонентов систем доставки лекарств .
Дисфункция сурфактанта - это заболевание, которое поражает новорожденных детей, у которых легочного сурфактанта недостаточно для адекватного дыхания, что приводит к респираторному дистресс-синдрому (RDS).
Несмотря на то, что DPPC является одним из основных компонентов сурфактанта легких, большинство генетических ошибок, связанных с нарушением дисфункции сурфактанта, не связаны с DPPC. Скорее, основными причинами этого заболевания являются различия в выработке сурфактантных белков B и C из-за генетических аномалий.
Однако существует генетическое заболевание, связанное с DPPC, которое вызывает дефицит продукции белка ABCA1 . Этот белок имеет решающее значение в транспорте фосфолипидов - и, следовательно, DPPC - к ламеллярным телам альвеолярных клеток, где DPPC взаимодействует с белками сурфактанта с образованием легочного сурфактанта.
Текущие исследования не могут найти корреляцию между процентным содержанием DPPC в легочном сурфактанте и возрастом беременности, хотя была обнаружена доказанная взаимосвязь между процентным содержанием DPPC и POPC (пальмитоил-олеоилфосфатидилхолина) у детей с респираторным дистресс-синдромом по сравнению с младенцами без это состояние. Эти связи предполагают, что конкретный состав сурфактанта приведет к респираторному дистресс-синдрому, независимо от гестационного возраста.
Корреляция между процентом DPPC и респираторным дистресс-синдромом - вот почему DPPC используется для изготовления лекарств для лечения новорожденных с этим заболеванием.
Кроме того, было показано, что DPPC связан с инфицированием поляризованных клеток специфическим видом аденовируса человека (HAdV-C2). Некоторые исследования показали, что ненасыщенный DPPC усиливает инфицирование клеток A59 HAdV-C2 (возможно, разрешая проникновение вируса через апикальную сторону поляризованных клеток).

