Аммиачный боран - Ammonia borane
|
|
| Имена | |
|---|---|
|
Название ИЮПАК
Аммониотригидроборат
|
|
| Другие имена
Боразане
|
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.170.890 |
| Номер ЕС | |
|
PubChem CID
|
|
| UNII | |
|
Панель управления CompTox ( EPA )
|
|
|
|
|
|
| Характеристики | |
|
BNH 6 |
|
| Молярная масса | 30,865 г моль -1 |
| Появление | Бесцветные кристаллы |
| Плотность | 780 мг мл -1 |
| Температура плавления | 104 ° С (219 ° F, 377 К) |
| Состав | |
| I4мм, четырехугольный | |
| Тетрагональный в B и N | |
| Тетрагидраль в B и N | |
| 5.2 D | |
| Опасности | |
| Пиктограммы GHS |
 
|
| Сигнальное слово GHS | Опасность |
| Родственные соединения | |
|
Родственные соединения
|
|
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
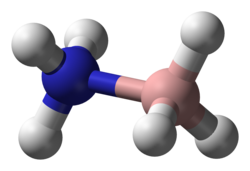
Боран аммиака (также систематически называемый амминетригидридобором ), также называемый боразаном , представляет собой химическое соединение с формулой H 3 NBH 3 . Бесцветный или твердое вещество белого цвета является наиболее простым молекулярным бором - азот - гидрид соединения. Он привлек внимание как источник водородного топлива, но в остальном представляет в первую очередь академический интерес.
Синтез
Реакция диборана с аммиаком дает в основном диаммониевую соль [H 2 B (NH 3 ) 2 ] + (BH 4 ) - . Аммиачный боран является основным продуктом, когда аддукт борана используется вместо диборана:
- BH 3 ( THF ) + NH 3 → BH 3 NH 3 + THF
Свойства и структура
Молекула принимает структуру, аналогичную структуре этана , с которой она изоэлектронна . Расстояние B-N составляет 1,58 (2) Å. Расстояния B − H и N − H составляют 1,15 и 0,96 Å соответственно. Его сходство с этаном незначительно, поскольку аммиачный боран - твердое вещество, а этан - газ: их точки плавления различаются на 284 ° C. Это различие согласуется с высокополярной природой аммиачного борана. Атомы Н, присоединенные к бору, гидридные, а атомы азота, присоединенные к азоту, несколько кислые.
Структура твердого тела указывает на тесную ассоциацию центров N H и B H. Ближайшее расстояние H − H составляет 1,990 Å, что можно сравнить с расстоянием связывания H − H 0,74 Å. Это взаимодействие называется дигидрогенной связью . Первоначальный кристаллографический анализ этого соединения изменил назначение B и N. Обновленная структура была получена с улучшенными данными с использованием метода нейтронной дифракции, который позволил атомам водорода определять местонахождение с большей точностью.
| Молекула | Аммиачно-боран | Аминоборан | Иминоборан |
|---|---|---|---|
| Формула | BNH 6 | BNH 4 | BNH 2 |
| Класс | аминоборан | аминоборан | иминоборан |
| Аналогичный углеводород | этан | этилен | ацетилен |
| Аналог углеводородного класса | алкан | алкен | алкин |
| Состав |
|
|

|
| Шариковая модель |

|

|
|
| Гибридизация бора и азота | sp 3 | sp 2 | зр |
| Длина облигации BN | 1,658 Å | 1,391 Å | 1,238 Å |
| Доля одинарной связи BN | 100% | 84% | 75% |
| Метод определения структуры | микроволновая спектроскопия | микроволновая спектроскопия | ИК-спектроскопия |
Использует
Аммиачный боран был предложен в качестве среды для хранения водорода , например, когда газ используется в качестве топлива для автомобилей. Его можно заставить выделять водород при нагревании, полимеризуясь сначала до (NH 2 BH 2 ) n , затем до (NHBH) n , который в конечном итоге разлагается до нитрида бора (BN) при температурах выше 1000 ° C. Он более плотный по водороду, чем жидкий водород, а также способен существовать при нормальных температурах и давлениях.
Боран аммиака находит применение в органическом синтезе в качестве стабильного на воздухе производного диборана.
Аналогичные аминобораны
Многие аналоги были получены из первичных, вторичных и даже третичных аминов :
- Боран трет-бутиламин ( т BuNH 2 → BH 3 )
- Боран триметиламин (Me 3 N → BH 3 )
- Боран изопропиламин ( i PrNH2 → BH 3 )
Первый аминный аддукт борана был получен из триметиламина . Боран-трет-бутиламиновый комплекс получают реакцией боргидрида натрия с трет-бутиламмонийхлоридом. Обычно аддукты более устойчивы с более основными аминами. Возможны также вариации по борному компоненту, хотя первичные и вторичные бораны встречаются реже.
Смотрите также
- Фосфин-боран (R 3 P → BH 3 )
- диметилсульфид борана (Me 2 S → BH 3 )
- боран-тетрагидрофуран (THF → BH 3 )


![Часть кристаллической структуры аммиачного борана [2]](https://upload.wikimedia.org/wikipedia/commons/thumb/9/93/Ammonia-borane-xtal-3D-balls.png/300px-Ammonia-borane-xtal-3D-balls.png)