Ванадат - Vanadate
В химии, A ванадат представляет собой анионный координационный комплекс из ванадия . Часто ванадат относится к оксоанионам ванадия , большинство из которых находится в высшей степени окисления +5. Комплексы [V (CN) 6 ] 3- и [V 2 Cl 9 ] 3- называются гексацианованадатом и нонахлордиванадатом.
Простой ион ванадата - это тетраэдрический ортованадат, VO 3-
4 анион, который присутствует, например, в ортованадате натрия и в растворах V 2 O 5 в сильном основании ( pH > 13). Обычно этот ион представлен одинарной двойной связью, однако это резонансная форма, поскольку ион представляет собой правильный тетраэдр с четырьмя эквивалентными атомами кислорода.
Кроме того, существует ряд полиоксованадат-ионов, который включает дискретные ионы и «бесконечные» полимерные ионы. Существуют также ванадаты, такие как ванадат родия, RhVO 4 , который имеет статистическую структуру рутила, в которой ионы Rh 3+ и V 5+ случайным образом занимают позиции Ti 4+ в решетке рутила, которые не содержат решетку катионов и уравновешивают ванадат-анионы, но представляют собой смешанные оксиды .
В химической номенклатуре, когда ванадат является частью названия, это указывает на то, что соединение содержит анион с центральным атомом ванадия, например гексафторванадат аммония - это общее название соединения (NH 4 ) 3 VF 6 с названием гексафторидованадата аммония ( ИЮПАК ) ( III).
Примеры оксованадат-ионов
Некоторые примеры дискретных ионов:
-
VO 3-
4 «ортованадат», четырехгранный. -
V
2 О 4-
7 «пированадат», тетраэдры VO 4 с общими углами , похожие на дихромат- ион -
V
3 О 3-
9 , циклический с общими вершинами тетраэдрами VO 4 -
V
4 О 4-
12 , циклический с общими вершинами тетраэдрами VO 4 -
V
5 О 3-
14 , угловые общие тетраэдры ВО 4 -
V
6 О 6-
18 , кольцо. -
V
10 О 6-
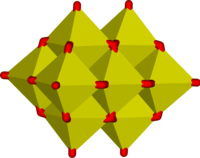
28 "декаванадат", октаэдры VO 6 с общими ребрами и углами - V
12 О 4-
32 -
V
13 О 3-
34 , склеенные октаэдры ВО 6 - V
18 О 12-
42
Некоторые примеры полимерных «бесконечных» ионов:
-
[VO
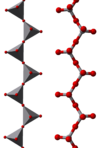
3 ] п -
п в, например, NaVO 3 , метаванадат натрия -
[V
3 О
8 ] п -
п в CaV 6 O 16
 |
 |
 |
|
|
|
В этих ионах ванадий проявляет тетраэдрическую, квадратно-пирамидальную и октаэдрическую координацию. В этом отношении ванадий имеет сходство с вольфраматом и молибдатом , тогда как хром, однако, имеет более ограниченный набор ионов.
Водные растворы
Растворение пятиокиси ванадия в сильнощелочном водном растворе дает бесцветный VO 3-
4 ион. При подкислении цвет этого раствора постепенно темнеет от оранжевого до красного примерно при pH 7. Коричневый гидратированный V 2 O 5 осаждается около pH 2, повторно растворяясь с образованием светло-желтого раствора, содержащего ион [VO 2 (H 2 O) 4 ] + . Количество и идентичность оксианионов, которые существуют между pH 13 и 2, зависят от pH, а также от концентрации. Например, протонирование ванадата инициирует серию конденсаций с образованием полиоксованадат-ионов:
- pH 9–12; HVO 2-
4 , V
2 О 4-
7 - pH 4–9; ЧАС
2 VO -
4 , V
4 О 4-
12 , HV
10 О 5-
28 - pH 2–4; H 3 VO 4 , H
2 V
10 О 4-
28
Фармакологические свойства
Ванадат является мощным ингибитором некоторых АТФаз плазматической мембраны , таких как Na + / K + -АТФаза и Ca 2+ -АТФаза ( PMCA ). Действуя как аналог фосфата в переходном состоянии, ванадат подвергается нуклеофильной атаке со стороны воды во время переноса фосфорила, по существу «улавливая» АТФазы P-типа в их фосфорилированном состоянии E2. Однако он не ингибирует другие АТФазы, такие как SERCA (Ca 2+ -АТФаза сарко / эндоплазматического ретикулума ), актомиозиновая АТФаза и митохондриальная АТФаза.

