Нигростриатальный путь - Nigrostriatal pathway
| Нигростриатальный путь | |
|---|---|
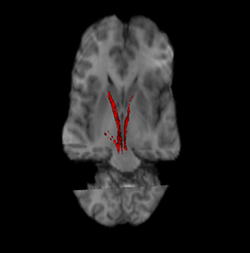 Нигростриатальный путь (слева и справа красным).
| |
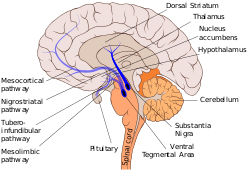 Здесь сплошным синим цветом показан нигростриатальный путь, соединяющий черную субстанцию с дорсальным полосатым телом.
| |
| Анатомическая терминология |
Нигростриатальный путем является двусторонний дофаминергическим пути в мозге , который соединяет черную субстанцию Парс компактов (ВНС) в среднем мозге с дорсальным стриатумом (то есть, хвостатое ядром и скорлупой ) , в переднем мозге. Это один из четырех основных дофаминовых путей в головном мозге, который имеет решающее значение для производства движений как часть системы, называемой моторной петлей базальных ганглиев . Дофаминергические нейроны этого пути высвобождают дофамин из окончаний аксонов, которые синапсируют с ГАМКергическими средними шиповидными нейронами (MSN), также известными как нейроны проекции шипов (SPN), расположенные в полосатом теле.
Дегенерация дофаминергических нейронов в SNc является одним из основных патологических признаков болезни Паркинсона , приводящим к заметному снижению функции дофамина и симптоматическому двигательному дефициту при болезни Паркинсона, включая гипокинезию , тремор , ригидность и постуральный дисбаланс .
Анатомия
Связь между компактной частью черной субстанции и дорсальным полосатым телом опосредуется дофаминергическими аксонами.
Черная субстанция компактная (SNc)
Черная субстанция находится в вентральном мозге каждого полушария. Он состоит из двух отдельных частей: pars compacta (SNc) и pars reticulata (SNr). Компактная часть содержит дофаминергические нейроны из группы клеток A9, которые формируют нигростриатный путь, который, поставляя дофамин в полосатое тело , передает информацию в базальные ганглии . В отличие от этого pars reticulata содержит в основном ГАМКергические нейроны.
SNc состоит из тонкой полосы клеток, которая покрывает SNr и расположена латеральнее группы дофаминергических нейронов A10 в вентральной тегментальной области (VTA), которая формирует мезолимбический дофаминовый путь . SNc легко визуализировать в срезах мозга человека, потому что дофаминовые нейроны содержат черный пигмент, называемый нейромеланином, который, как известно, накапливается с возрастом. Тела дофаминергических клеток в SNc плотно упакованы примерно от 200 000 до 420 000 дофаминовых клеток в SNc человека и от 8 000 до 12 000 дофаминовых клеток в SNc мыши. Эти дофаминовые клеточные тела расположены в одном из двух химически определенных слоев. Те, что находятся в верхнем слое (или на дорсальном уровне), содержат связывающий белок под названием кальбиндин -D28K, который может буферизовать уровни кальция внутри клетки, когда он становится слишком высоким или токсичным. Клеткам дофамина в нижнем слое (или вентральном слое ) не хватает этого белка, и они более уязвимы к воздействию нейротоксинов (например, MPTP ), которые могут вызывать симптомы, похожие на болезнь Паркинсона. Клетки дофамина дорсального уровня имеют дендриты, которые расходятся горизонтально через компактную часть, тогда как клетки дофамина вентрального уровня имеют дендриты, которые простираются вентрально в ретикулатную часть.
Дофаминергические аксоны
В аксонах из нейронов допамина исходят из первичного дендрита и проекта ипсилатерально (на ту же сторону) через медиальный передний мозг пучок к спинному стриатуму. Существует грубая топографическая корреляция между анатомической локализацией тела дофаминовых клеток в SNc и областью терминации в дорсальном полосатом теле. Дофаминергические клетки в латеральных частях SNc проецируются в основном в латеральную и каудальную (заднюю) части полосатого тела, тогда как дофаминовые клетки в медиальном SNc проецируются в медиальное полосатое тело. Кроме того, дофаминовые клетки в дорсальном ярусе проецируются в вентромедиальное полосатое тело, тогда как нейроны вентрального яруса проецируются в дорсальное хвостатое ядро и скорлупу. В целом, в дорсолатеральном полосатом теле наблюдается большая плотность дофаминергического входа.
Каждый дофаминовый нейрон имеет чрезвычайно большую немиелинизированную аксональную ветвь, которая может иннервировать до 6% объема полосатого тела у крысы. Хотя все дофаминовые клетки SNc проецируются как в стриосому (или участок), так и в нейрохимические компартменты матрикса стриатума, большая часть аксональной территории нейрона дорсального уровня находится в компартменте матрикса, в то время как большая часть аксонального поля нейронов вентрального яруса находится в нем. стриосомы. Нигростриатальные аксоны дофамина также могут вызывать образование коллатералей аксонов, которые проецируются в другие области мозга. Например, некоторые нигростриатные дофаминовые аксоны SNc отправляют коллатерали аксонов в педункулопонтинное ядро , вентральный палладий , субталамическое ядро , бледный шар , миндалевидное тело и таламус .
Небольшое количество дофаминовых нейронов дорсального уровня SNc также проецируется непосредственно в кору, хотя большая часть дофаминергической иннервации коры происходит от соседних дофаминовых нейронов VTA.
Дорсальное полосатое тело
Спинной стриатуме расположен в подкорковой области мозга . У приматов и других млекопитающих он разделен передней конечностью белого вещества, называемой внутренней капсулой , на две части: хвостатое ядро и скорлупу . У грызунов внутренняя капсула развита слабо, так что хвостатая часть и скорлупа не разделены, а образуют одно большое образование, называемое хвостатой скорлупой (CPu). Большинство (около 95%) клеток в дорсальном полосатом теле представляют собой ГАМКергические нейроны со средним шипом (MSN), также известные как нейроны с выступами шипов (SPN). Примерно половина этих MSN содержат рецепторы дофамина D1 и проецируются непосредственно на черную субстанцию, чтобы сформировать прямой путь базальных ганглиев, тогда как другая половина экспрессирует рецепторы дофамина D2, которые косвенно проецируются в черную субстанцию через бледный шар и субталамическое ядро с образованием непрямой путь базальных ганглиев. Остальные 5% клеток представляют собой интернейроны, которые являются либо холинергическими нейронами, либо одним из нескольких типов ГАМКергических нейронов. Аксоны и дендриты этих интернейронов остаются в полосатом теле.
Хвостатое ядро и скорлупа получают возбуждающую информацию от всех областей коры головного мозга . Эти глутаматергические входы обычно топографически расположены так, что скорлупа получает информацию в основном от сенсомоторной коры, тогда как хвостатое ядро получает информацию в основном от ассоциативной коры. Кроме того, дорсальное полосатое тело получает возбуждающие сигналы от других структур мозга, таких как таламус, и незначительные возбуждающие сигналы от гиппокампа и миндалины .
Дорсальное полосатое тело содержит нейрохимически определенные компартменты, называемые стриосомами (также известные как пятна), которые демонстрируют плотное окрашивание μ-опиоидных рецепторов, встроенных в матричный отсек, который содержит высшую ацетилхолинэстеразу и кальбиндин-D28K.
Допаминергические окончания аксонов синапса нигростриатного пути на ГАМКергические MSN в дорсальном полосатом теле. Они образуют синапсы на теле клетки и областях дендритных стержней, но в основном на шейках дендритных шипов, которые также получают глутаматергический вход в головки тех же дендритных шипов.
Функция
Основная функция нигростриатного пути - влиять на произвольные движения через моторные петли базальных ганглиев. Наряду с мезолимбическим и мезокортикальным дофаминергическими путями нигростриатальный дофаминовый путь также может влиять на другие функции мозга, включая познание , вознаграждение и зависимость . Нигростриатальные дофаминергические нейроны демонстрируют тонические и фазовые паттерны нейрональной активности. Это может приводить к различным паттернам высвобождения дофамина из окончаний аксонов в дорсальном полосатом теле, а также из тела клетки (сомы) и дендритов в SNc и SNr. Помимо высвобождения дофамина, некоторые аксоны в нигростриатном пути также могут совместно высвобождать ГАМК.
Нигростриатальный путь влияет на движение двумя путями: прямым и косвенным .
Прямой путь движения
Прямой путь участвует в облегчении желавших движений . Проекции дофаминового рецептора D1, содержащего средние шиповатые нейроны в хвостатом ядре и синапсе скорлупы, на тонически активные ГАМКергические клетки в сетчатой части черной субстанции и внутреннем сегменте бледного шара (GPi), которые затем проецируются в таламус. Поскольку стриатонигральный / стриатоэнтопедункулярный и нигроталамический пути являются тормозящими, активация прямого пути создает общий общий возбуждающий эффект на таламус и на движения, генерируемые моторной корой.
Косвенный путь движения
Непрямой путь участвует в подавлении нежелательных перемещений . Проекции от дофаминового рецептора D2, содержащего средние шиповатые нейроны в хвостатом ядре и синапсе скорлупы, на тонически активные ГАМКергические клетки во внешнем сегменте бледного шара (GPe), которые затем проецируются в сетчатую часть черной субстанции через возбуждающее субтальмическое ядро (STN) . Поскольку стриатопаллидный и нигроталамический пути являются тормозящими, а путь от субталамического к черному - возбуждающим, активация непрямого пути создает общий суммарный тормозящий эффект на таламус и движение моторной коры.
Клиническое значение
болезнь Паркинсона
Болезнь Паркинсона характеризуется серьезными двигательными проблемами, в основном гипокинезией , ригидностью, тремором и дисбалансом позы. Потеря дофаминовых нейронов в нигростриатном пути является одним из основных патологических признаков болезни Паркинсона. Дегенерация нейронов, продуцирующих дофамин, в компактной части черной субстанции и в комплексе скорлупа-хвостатое вещество приводит к снижению концентраций дофамина в нигростриатальном пути, что приводит к снижению функции и характерным симптомам. Симптомы болезни обычно не проявляются до тех пор, пока не будет потеряно 80-90% дофаминовой функции.
Дискинезия, вызванная леводопой
Дискинезии, вызванные леводопой (LID), представляют собой осложнение, связанное с длительным применением L-DOPA для лечения болезни Паркинсона, которое характеризуется непроизвольными движениями и сокращениями мышц. Это нарушение возникает у 90% пациентов после 9 лет лечения. Использование L-DOPA у пациентов может привести к прерыванию нигростриатных проекций дофамина, а также к изменениям постсинаптических нейронов в базальных ганглиях.
Шизофрения
Пресинаптический метаболизм дофамина нарушен при шизофрении .
Другие пути дофамина
Другие основные пути дофамина включают:

