Синдром Гурлера - Hurler syndrome
| Синдром Гурлера | |
|---|---|
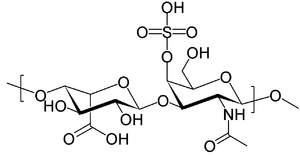 | |
| Структура дерматансульфата , одной из молекул, которая накапливается в лизосомах пациентов с синдромом Гурлера. | |
| Причины | Дефицит фермента альфа-L идуронидазы |
| Дифференциальная диагностика | Синдром Херлера-Шейе ; Синдром Шейе ; Синдром Хантера ; другие мукополисахаридозы |
| Прогноз | Смерть обычно наступает до 12 лет. |
| Частота | 1 из 100 000 |
Синдром Гурлера , также известный как мукополисахаридоз типа IH ( MPS-IH ), болезнь Гурлера и ранее именовавшаяся горгулизмом , представляет собой генетическое заболевание, которое приводит к накоплению в лизосомах больших молекул сахара, называемых гликозаминогликанами (ГАГ) . Неспособность расщепить эти молекулы приводит к широкому спектру симптомов, вызванных повреждением нескольких различных систем органов , включая, помимо прочего, нервную систему , скелетную систему , глаза и сердце .
Основным механизмом является дефицит альфа-L идуронидазы , фермента, ответственного за расщепление ГАГ. Без этого фермента в организме происходит накопление дерматансульфата и гепарансульфата . Симптомы появляются в детстве, и обычно наступает ранняя смерть. Другие, менее тяжелые формы MPS типа I включают синдром Херлера-Шейе (MPS-IHS) и синдром Шейе (MPS-IS).
Синдром Гурлера классифицируется как лизосомная болезнь накопления . Клинически это связано с синдромом Хантера (MPS II); однако синдром Хантера является Х-сцепленным , в то время как синдром Гурлера является аутосомно-рецессивным .
Признаки и симптомы
Дети с синдромом Гурлера могут казаться нормальными при рождении, а симптомы у них развиваются в первые годы жизни. Симптомы у разных пациентов различаются.
Одна из первых аномалий, которую можно обнаружить, - это огрубление черт лица; эти симптомы могут появиться в возрасте 3–6 месяцев. Головка может быть большим с видными лобных костей . Череп может быть удлиненным . Нос может иметь уплощенную переносицу с непрерывными выделениями из носа. Глазницы могут быть широко расставлены, а глаза могут выступать из черепа. Губы могут быть большими, и больные дети могут постоянно держать челюсти открытыми. Скелетные аномалии возникают примерно в возрасте 6 месяцев, но могут не проявляться клинически до 10–14 месяцев. Пациенты могут испытывать изнуряющие деформации позвоночника и бедра, синдром запястного канала и скованность суставов. Пациенты могут иметь нормальный рост в младенчестве, но перестать расти к 2 годам. Они не могут достигать высоты более 4 футов.
Другие ранние симптомы могут включать паховые и пупочные грыжи . Они могут присутствовать при рождении или развиваться в течение первых месяцев жизни. Помутнение роговицы и дегенерация сетчатки могут произойти в течение первого года жизни, что приведет к слепоте. Часто наблюдаются увеличенные печень и селезенка . Дисфункции органов нет, но отложение ГАГ в этих органах может привести к их значительному увеличению. У пациентов также может быть понос . Может возникнуть заболевание аортального клапана .
Обструкция дыхательных путей является частым явлением, обычно вторичным по отношению к аномалиям шейных позвонков. Часто встречаются инфекции верхних и нижних дыхательных путей.
Задержка развития может проявиться в возрасте 1-2 лет, при максимальном функциональном возрасте 2-4 года. Далее следует прогрессирующее ухудшение. У большинства детей развиваются ограниченные языковые способности. Смерть обычно наступает к 10 годам.
Механизмы
Ген IDUA отвечает за кодирование фермента под названием альфа-L-идуронидаза. Через гидролиз альфа-L-идуронидаза отвечает за разрушение молекулы, называемой несульфатированной альфа-L-идуроновой кислотой . Это уроновая кислота, содержащаяся в дерматансульфате и гепарансульфате ГАГ. Фермент альфа-L-идуронидаза находится в лизосомах. Без достаточной ферментативной функции эти ГАГ не могут перевариваться должным образом.
Генетика
Дети с синдромом Гурлера несут две дефектные копии гена IDUA , который был картирован в сайте 4p16.3 на хромосоме 4 . Это ген, который кодирует протеин идуронидазу. По состоянию на 2018 год было показано , что более 201 различных мутаций в гене IDUA вызывают MPS I.
Поскольку синдром Гурлера является аутосомно- рецессивным заболеванием, у больных есть две неработающие копии гена. Носителем называется лицо, рожденное с одной нормальной и одной дефектной копиями . Они будут производить меньше α-L-идуронидазы, чем человек с двумя нормальными копиями гена. Однако сниженное производство фермента в носителях остается достаточным для нормального функционирования; у человека не должно быть никаких симптомов болезни.
Диагностика
Диагноз часто можно установить на основании клинического осмотра и анализа мочи (избыток мукополисахаридов выводится с мочой ). Ферментные анализы (тестирование различных клеток или биологических жидкостей в культуре на дефицит ферментов) также используются для окончательной диагностики одного из мукополисахаридозов. Пренатальная диагностика с использованием амниоцентеза и биопсии ворсин хориона может подтвердить, несет ли плод копию дефектного гена или поражен ли он этим заболеванием. Генетическое консультирование может помочь родителям, у которых в семейном анамнезе есть мукополисахаридозы, определить, являются ли они носителями мутированного гена, вызывающего нарушения.
Классификация
Все члены семейства мукополисахаридозов также являются лизосомными болезнями накопления . Мукополисахаридоз I типа (MPS I) делится на три подтипа в зависимости от тяжести симптомов. Все три типа приводят к отсутствию или снижению функционирования одного и того же фермента. MPS-IH (синдром Гурлера) - наиболее тяжелый из подтипов MPS I. Два других типа - это MPS-IS ( синдром Шейе ) и MPS-IHS ( синдром Херлера-Шей ).
Из-за значительного совпадения между синдромом Херлера, синдромом Херлера-Шейи и синдромом Шейи некоторые источники считают эти термины устаревшими. Вместо этого MPS I можно разделить на «тяжелую» и «ослабленную» формы.
Уход
В настоящее время нет лекарства от синдрома Гурлера. Заместительная ферментная терапия идуронидазой (альдуразим) может улучшить функцию легких и подвижность. Это может уменьшить количество углеводов, которые неправильно хранятся в органах. Может потребоваться хирургическая коррекция деформаций кисти и стопы. Хирургия роговицы может помочь облегчить проблемы со зрением.
Трансплантация костного мозга (BMT) и трансплантация пуповинной крови (UCBT) могут использоваться в качестве лечения MPS I. BMT от братьев и сестер с идентичными генами HLA и от родственников со сходными генами HLA может значительно улучшить выживаемость, когнитивные функции и физические симптомы. У пациентов может развиться болезнь «трансплантат против хозяина» ; это более вероятно у доноров, не являющихся братьями и сестрами. В исследовании 1998 г. у детей от HLA-идентичных братьев и сестер 5-летняя выживаемость составила 75%; дети от доноров, не являющихся братьями и сестрами, имели 5-летнюю выживаемость 53%.
Дети часто не имеют доступа к подходящему донору костного мозга. В этих случаях UCBT от неродственных доноров может увеличить выживаемость, уменьшить физические признаки заболевания и улучшить познавательные способности. Осложнения от этого лечения могут включать болезнь «трансплантат против хозяина» .
Прогноз
Британское исследование 2008 года показало, что средняя ожидаемая продолжительность жизни пациентов с синдромом Херлера составляет 8,7 года. Для сравнения, средняя продолжительность жизни для всех форм МПС типа I составляла 11,6 года. Пациенты, которым была проведена успешная трансплантация костного мозга, имели 2-летнюю выживаемость 68% и 10-летнюю выживаемость 64%. Пациенты, которым не делали трансплантацию костного мозга, имели значительно сокращенную продолжительность жизни, средний возраст составлял 6,8 года.
Эпидемиология
Синдром Гурлера имеет общую частоту один на 100000. В совокупности все мукополисахаридозы имеют частоту примерно один на каждые 25 000 рождений в Соединенных Штатах.
Исследовать
Генная терапия
Существует большой интерес к лечению MPS I с помощью генной терапии . В моделях на животных доставка гена идуронидазы осуществляется с помощью ретровируса , аденовируса , аденоассоциированного вируса и плазмидных векторов. Мышей и собак с MPS I успешно лечили генной терапией. Большинство переносчиков могут вылечить болезнь печени и селезенки, а также могут исправить воздействие на мозг с помощью высоких доз. Генная терапия улучшила выживаемость, неврологические и физические симптомы; однако у некоторых животных развиваются необъяснимые опухоли печени. Если проблемы безопасности удастся решить, генная терапия может стать альтернативным лечением расстройств МПС у человека в будущем.
Компания Sangamo Therapeutics со штаб-квартирой в Ричмонде, штат Калифорния , в настоящее время проводит клинические испытания, включающие редактирование генов с использованием нуклеазы цинковых пальцев (ZFN) для лечения MPS I.
История
В 1919 году немецкий педиатр Гертруда Херлер описала синдром, связанный с помутнением роговицы, аномалиями скелета и умственной отсталостью. Подобное заболевание «горгулий» было описано в 1917 году Чарльзом А. Хантером. Херлер не упомянул статью Хантера. Из-за прерывания связи, вызванного Первой мировой войной , вполне вероятно, что она не знала о его исследовании. Синдром Гурлера теперь относится к MPS IH, а синдром Хантера относится к MPS II. В 1962 году Шейи определил более мягкую форму МПС I, что привело к обозначению синдрома Шейе.
Смотрите также
- Синдром Хантера (МПС II)
- Синдром Санфилиппо (MPS III)
- Синдром Моркио (МПС IV)
- Синдром Марото-Лами (МПС VI)
использованная литература
внешние ссылки
| Классификация | |
|---|---|
| Внешние ресурсы |



