Искусственная матка - Artificial womb
 |
Искусственная матка или искусственная матка является устройством , которое позволит экстракорпоральной беременности путем выращивания плода вне тела организма , которые обычно несут плод до срока.
Искусственная матка , как замещающий орган, может иметь множество применений. Его можно использовать для оказания помощи парам мужского и женского пола в развитии плода. Это потенциально может быть выполнено как переключение с естественной матки на искусственную, тем самым переместив порог жизнеспособности плода на гораздо более раннюю стадию беременности. В этом смысле его можно рассматривать как неонатальный инкубатор с очень расширенными функциями. Его также можно использовать для инициации развития плода. Искусственная матка также может помочь сделать операции на плодах на ранней стадии, вместо того, чтобы откладывать их до срока беременности.
В 2016 году ученые опубликовали два исследования, посвященных человеческим эмбрионам, развивающимся в течение тринадцати дней в экто-маточной среде. В настоящее время правило 14 дней запрещает хранение человеческих эмбрионов в искусственных матках дольше 14 дней. Это правило было закреплено в законах двенадцати стран.
В 2017 году исследователи плода из Детской больницы Филадельфии опубликовали исследование, показывающее, что они выращивали недоношенные плоды ягненка в течение четырех недель с помощью внематочной системы жизнеобеспечения.
Компоненты
Искусственная матка, которую иногда называют «экзомбом», должна обеспечивать питательными веществами и кислородом для вынашивания плода, а также удалять отходы. Объем искусственной матки (или «искусственной системы матки», чтобы подчеркнуть более широкий объем) может также включать интерфейс, выполняющий функцию, в противном случае обеспечиваемую плацентой , амниотический резервуар, функционирующий как амниотический мешок , а также пуповину .
Питание, снабжение кислородом и утилизация отходов
Женщина может по-прежнему поставлять питательные вещества и избавляться от отходов жизнедеятельности, если к ней подключена искусственная матка. Она также может обеспечивать иммунную защиту от болезней, передавая антитела IgG эмбриону или плоду.
Искусственное снабжение и удаление имеют потенциальное преимущество, позволяя плоду развиваться в среде, на которую не влияют наличие болезней, загрязнителей окружающей среды, алкоголя или лекарств, которые могут быть у человека в системе кровообращения. Отсутствует риск иммунной реакции на эмбрион или плод, которая в противном случае могла бы возникнуть из-за недостаточной гестационной иммунной толерантности . Некоторые отдельные функции искусственного поставщика и лица, занимающегося удалением, включают:
- Удаление отходов может осуществляться путем диализа .
- Экстракорпоральная мембранная оксигенация (ЭКМО) - это действенный метод оксигенации эмбриона или плода и удаления углекислого газа , позволяющий успешно поддерживать жизнь козьих плодов в амниотических резервуарах на срок до 237 часов. ЭКМО в настоящее время представляет собой методику, используемую в отдельных отделениях интенсивной терапии новорожденных для лечения доношенных новорожденных с отдельными медицинскими проблемами, которые приводят к неспособности ребенка выжить за счет газообмена с использованием легких. Однако сосуды головного мозга и зародышевый матрикс у плода плохо развиты, и, следовательно , существует недопустимо высокий риск внутрижелудочкового кровоизлияния (ВЖК) при введении ЭКМО на сроке гестации менее 32 недель. Жидкая вентиляция была предложена как альтернативный метод оксигенации или, по крайней мере, как промежуточный этап между маткой и дыханием на открытом воздухе.
- Современные методы искусственного питания проблематичны. Полное парентеральное питание , по данным исследования на младенцах с тяжелым синдромом короткой кишки , дает 5-летнюю выживаемость примерно 20%.
- Также остаются нерешенными вопросы, связанные с гормональной стабильностью.
Теоретически могут использоваться поставщики и средства для удаления животных , но при вовлечении матки животного этот метод может скорее относиться к сфере межвидовой беременности .
Стенка матки
В нормальной матки, миометрии из стенки матки функций , чтобы изгнать плод в конце беременности, и эндометрий , играет определенную роль в формировании плаценты. Искусственная матка может включать компоненты эквивалентной функции. Были рассмотрены способы подключения искусственной плаценты и других «внутренних» компонентов непосредственно к внешнему кровообращению.
Интерфейс (искусственная плацента)
Интерфейс между поставщиком и эмбрионом или плодом может быть полностью искусственным, например, с использованием одной или нескольких полупроницаемых мембран, таких как применяемые при экстракорпоральной мембранной оксигенации (ЭКМО).
Существует также возможность выращивать плаценту с использованием клеток эндометрия человека . В 2002 году было объявлено, что образцы тканей из культивированных клеток эндометрия, взятых у человека-донора, успешно выросли. Затем образец ткани был сконструирован так, чтобы он имел форму естественной матки, и человеческие эмбрионы были имплантированы в ткань. Эмбрионы правильно имплантировались в подкладку искусственной матки и начали расти. Тем не менее, эксперименты были остановлены через шесть дней, чтобы не выходить за рамки разрешенных законом ограничений по экстракорпоральному оплодотворению (ЭКО) в Соединенных Штатах .
Теоретически человеческую плаценту можно пересадить внутрь искусственной матки, но прохождение питательных веществ через эту искусственную матку остается нерешенной проблемой.
Амниотический резервуар (искусственный амниотический мешок)
Основная функция амниотического резервуара - выполнять функцию амниотического мешка по физической защите эмбриона или плода, оптимально позволяя ему свободно двигаться. Он также должен поддерживать оптимальную температуру. Раствор Рингера с лактатом можно использовать как заменитель околоплодных вод .
Пуповина
Теоретически, в случае преждевременного извлечения плода из естественной матки, естественная пуповина может использоваться, оставаясь открытой либо с помощью медикаментозного подавления физиологической окклюзии, либо с помощью антикоагуляции, а также путем стентирования или создания обходного пути для поддержания кровотока. между матерью и плодом.
Исследования и разработки
Эмануэль М. Гринберг
Эмануэль М. Гринберг написал различные статьи на тему искусственной матки и ее потенциального использования в будущем.
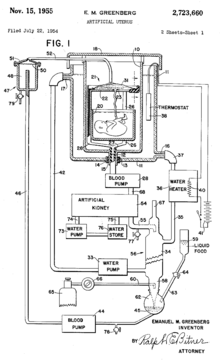
22 июля 1954 года Эмануэль М. Гринберг подал патент на конструкцию искусственной матки. Патент включал два изображения дизайна искусственной матки. Сама конструкция включала резервуар для помещения плода, наполненный околоплодными водами, устройство, подключенное к пуповине, насосы для крови, искусственную почку и водонагреватель. Он получил патент 15 ноября 1955 г.
11 мая 1960 года Гринберг написал редактору американского журнала акушерства и гинекологии. Гринберг утверждал, что в журнале была опубликована статья «Попытки создать« искусственную матку »», в которой не было никаких цитат по теме искусственной матки. По словам Гринберга, это говорит о том, что идея искусственной матки была новой, хотя он сам опубликовал несколько статей по этой теме.
Университет Дзюнтендо в Токио
В 1996 году Университет Джунтендо в Токио разработал метод внематочной инкубации плода (EUFI). Руководил проектом Ёсинори Кувабара, который интересовался развитием недоношенных новорожденных. Система была разработана с использованием четырнадцати козьих плодов, которые затем были помещены в искусственные околоплодные воды в тех же условиях, что и мать-коза. Кувабаре и его команде удалось сохранить козий плод в системе в течение трех недель. Однако система столкнулась с несколькими проблемами и не была готова к испытаниям на людях. Кувабара по-прежнему надеялся, что система будет улучшена и позже будет использоваться на человеческих зародышах.
Детская больница Филадельфии
В 2017 году исследователи Детской больницы Филадельфии смогли продолжить разработку внематочной системы. В исследовании используются плодные ягнята, которых затем помещают в полиэтиленовый пакет, наполненный искусственными околоплодными водами. Система состоит из 3 основных компонентов: артериовенозного контура без помпы, замкнутой стерильной жидкой среды и пупочного сосудистого доступа. Что касается артериовенозного контура без помпы , кровоток управляется исключительно сердцем плода в сочетании с оксигенатором с очень низким сопротивлением, чтобы максимально имитировать нормальное кровообращение плода / плаценты. Закрытая стерильная среда жидкости важна для обеспечения стерильности. Ученые разработали технику канюляции сосуда пуповины, которая поддерживает длину нативной пуповины (5–10 см) между кончиками канюли и брюшной стенкой, чтобы минимизировать случаи деканюляции и риск механической непроходимости. Пуповина ягнят прикреплена к устройству за пределами мешка, которое действует как плацента и обеспечивает кислород и питательные вещества, а также удаляет любые отходы. Исследователи держали машину «в темной теплой комнате, где исследователи могут воспроизводить звуки материнского сердца для плода ягненка». Система смогла помочь недоношенным плодам ягненка нормально развиваться в течение месяца. Действительно, ученые вывели 8 ягнят с поддержанием стабильного уровня потока в контуре, эквивалентного нормальному потоку к плаценте. В частности, они вынашивали 5 плодов от 105 до 108 дней гестации в течение 25–28 дней и 3 плода от 115 до 120 дней беременности в течение 20–28 дней. Самые длительные прогоны были прекращены на 28 день из-за ограничений протокола животных, а не из-за какой-либо нестабильности, что позволяет предположить, что поддержка этих ранних гестационных животных может поддерживаться после 4 недель. Алан Флейк, фетальный хирург Детской больницы Филадельфии, надеется перенести тестирование на недоношенные человеческие плоды, но это может занять от трех до пяти лет, чтобы это стало реальностью. Флаке, который руководил исследованием, называет возможность их технологии воссоздания полной беременности «несбыточной мечтой на данный момент» и лично не намеревается создавать технологию для этого.
Эйндховенский технологический университет (Нидерланды)
С 2016 года исследователи TU / e и партнеры стремятся разработать искусственную матку, которая является адекватной заменой защитной среды материнской утробы в случае преждевременных родов, предотвращая осложнения со здоровьем. Искусственная матка и плацента создадут для ребенка естественную среду с целью облегчения перехода к жизни новорожденного. Система перинатальной поддержки жизни (PLS) будет разработана с использованием передовых технологий: манекен будет имитировать младенца во время тестирования и обучения, расширенный мониторинг и компьютерное моделирование предоставят клинические рекомендации.
Консорциум трех европейских университетов, работающих над проектом, состоит из Аахена, Милаана и Эйндховена. В 2019 году этому консорциуму была предоставлена субсидия в размере 3 миллионов евро, и второй грант в размере 10 миллионов находится в стадии разработки. Вместе партнеры PLS предоставляют совместные медицинские, инженерные и математические знания для разработки и проверки перинатальной системы жизнеобеспечения с использованием передовых технологий моделирования. Междисциплинарный консорциум будет способствовать развитию этих технологий и объединить их для создания первой системы созревания плода ex vivo для клинического использования. Этот проект, координируемый Технологическим университетом Эйндховена, объединяет ведущих мировых экспертов в области акушерства, неонатологии, промышленного дизайна, математического моделирования, поддержки органов ex vivo и неинвазивного мониторинга плода. Этот консорциум возглавляют профессор Франс ван де Воссе и профессор и доктор Гуид Оэй. В 2020 году инженеры Ясмийн Кок и Лайла Кок создали дочернюю компанию Juno Perinatal Healthcare, что обеспечило оценку результатов проведенных исследований. Более подробную информацию о спин-оффе можно найти здесь;
Более подробную информацию о проекте технических университетов и его исследователей можно найти здесь:
Философские соображения
Биоэтика
Развитие искусственной матки и эктогенеза поднимает биоэтические и юридические соображения, а также имеет важные последствия для репродуктивных прав и дебатов об абортах .
Искусственная матка может расширить диапазон жизнеспособности плода , вызывая вопросы о роли, которую жизнеспособность плода играет в рамках закона об абортах . В рамках теории разрыва, например, права на аборт включают только право на удаление плода и не всегда распространяются на прерывание плода. Если перенос плода из утробы женщины в искусственную матку возможен, выбор прерывания беременности таким способом может стать альтернативой прерыванию плода.
Существуют также теоретические опасения, что детям, которые развиваются в искусственной матке, может не хватать «некоторых существенных связей со своими матерями, которые есть у других детей».
Гендерное равенство и ЛГБТ
В книге 1970 года «Диалектика пола» феминистка Суламифь Файерстоун написала, что различия в биологических репродуктивных ролях являются источником гендерного неравенства . Файерстоун выделил беременность и роды, аргументируя это тем, что искусственная матка освободит «женщин от тирании их репродуктивной биологии».
Арати Прасад утверждает в своей колонке на The Guardian в своей статье «Как искусственные матки изменят наши представления о гендере, семье и равенстве», что «это [...] даст мужчинам важный инструмент, чтобы иметь ребенка полностью без женщины, если они выберут. Он попросит нас поставить под сомнение концепции пола и отцовства ". Кроме того, она приводит доводы в пользу преимуществ для однополых пар: «Это также может означать, что разрыв между матерью и отцом может быть устранен: матка вне тела женщины будет служить женщинам, трансгендерным женщинам и однополым парам в равной степени без каких-либо предубеждений. . "
Смотрите также
- Амниотическая жидкость
- Аферез
- Эктогенез
- Колонизация эмбрионального пространства
- Экстракорпоральная мембранная оксигенация
- Гемодиализ
- Экстракорпоральное оплодотворение
- Беременность у мужчин
- Постгендеризм
- Тканевая инженерия
использованная литература
дальнейшее чтение
- Коулман, Стивен (2004). Этика искусственной матки: значение для размножения и аборта . Берлингтон, VT: паб Ashgate. ISBN 978-0-7546-5051-5.
- Скотт Гельфанд, изд. (2006). Эктогенез: технология искусственной матки и будущее воспроизводства человека . Амстердам [ua]: Родопи. ISBN 978-90-420-2081-8.

