Аргиназа - Arginase
| Аргиназа | |||||||||
|---|---|---|---|---|---|---|---|---|---|
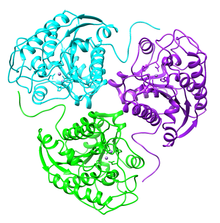 Ленточная диаграмма тримеров аргиназы I. человека. Запись PDB 2pha
| |||||||||
| Идентификаторы | |||||||||
| ЕС нет. | 3.5.3.1 | ||||||||
| № CAS | 9000-96-8 | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| BRENDA | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| Структуры PDB | RCSB PDB PDBe PDBsum | ||||||||
| Генная онтология | Amigo / QuickGO | ||||||||
| |||||||||
| Аргиназа печени | |||||||
|---|---|---|---|---|---|---|---|
 | |||||||
| Идентификаторы | |||||||
| Символ | ARG1 | ||||||
| Ген NCBI | 383 | ||||||
| HGNC | 663 | ||||||
| OMIM | 608313 | ||||||
| RefSeq | NM_000045 | ||||||
| UniProt | P05089 | ||||||
| Прочие данные | |||||||
| Номер ЕС | 3.5.3.1 | ||||||
| Locus | Chr. 6 q23 | ||||||
| |||||||
| Аргиназа, тип II | |||||||
|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||
| Символ | ARG2 | ||||||
| Ген NCBI | 384 | ||||||
| HGNC | 664 | ||||||
| OMIM | 107830 | ||||||
| RefSeq | NM_001172 | ||||||
| UniProt | P78540 | ||||||
| Прочие данные | |||||||
| Номер ЕС | 3.5.3.1 | ||||||
| Locus | Chr. 14 q24.1 | ||||||
| |||||||
Аргиназы ( ЕС 3.5.3.1 , аргинин amidinase , canavanase , L-аргиназа , аргинин трансамидиназа ) представляет собой марганец отработанного фермента . Реакция, катализируемая этим ферментом, следующая : аргинин + H 2 O → орнитин + мочевина . Это последний фермент из цикла мочевины . Он присутствует во всех сферах жизни.
Структура и функции
Аргиназа принадлежит к семейству ферментов уреогидролазы .
Аргиназа катализирует пятую и последнюю стадию цикла мочевины , серию биохимических реакций у млекопитающих, во время которых организм избавляется от вредного аммиака . В частности, аргиназа превращает L- аргинин в L- орнитин и мочевину. Аргиназа млекопитающих активна как тример, но некоторые бактериальные аргиназы являются гексамерными. Фермент требует двухмолекулярного металлического кластера марганца для поддержания надлежащего функционирования. Эти ионы Mn 2+ координируются с водой, ориентируя и стабилизируя молекулу и позволяя воде действовать как нуклеофил и атаковать L-аргинин, гидролизуя его до орнитина и мочевины.
У большинства млекопитающих существует два изофермента этого фермента; первая, аргиназа I, участвует в цикле мочевины и располагается в основном в цитоплазме гепатоцитов (клеток печени). Второй изофермент, аргиназа II, участвует в регуляции внутриклеточных уровней аргинина / орнитина. Он расположен в митохондриях нескольких тканей организма, в основном в почках и простате. В более низких количествах он может быть обнаружен в макрофагах, лактирующих молочных железах и головном мозге. Второй изофермент может быть обнаружен в отсутствие других ферментов цикла мочевины.
Механизм
Активный центр удерживает L-аргинин на месте за счет водородной связи между гуанидиновой группой с Glu227. Это связывание ориентирует L-аргинин для нуклеофильной атаки связанным с металлом гидроксид-ионом по гуанидиновой группе. Это приводит к тетраэдрическому промежуточному соединению. Ионы марганца действуют, стабилизируя как гидроксильную группу в тетраэдрическом промежуточном соединении, так и развивающуюся неподеленную электронную пару sp 3 на группе NH 2, когда образуется тетраэдрический промежуточный продукт.
Активный сайт аргиназы необычайно специфичен. Изменение структуры субстрата и / или стереохимии сильно снижает кинетическую активность фермента. Эта специфичность возникает из-за большого количества водородных связей между субстратом и ферментом; существуют прямые или водородные связи с водородом, насыщающие как четыре акцепторных положения на альфа-карбоксилатной группе, так и все три положения на альфа-аминогруппе. N-гидрокси-L-аргинин (NOHA), промежуточный продукт биосинтеза NO, является умеренным ингибитором аргиназы. Кристаллическая структура его комплекса с ферментом показывает, что он замещает металл-мостиковый гидроксид-ион и связывает биядерный марганцевый кластер.
Кроме того, 2 (S) -амино-6-бороногексоновая кислота (ABH) представляет собой аналог L-аргинина, который также создает тетраэдрический промежуточный продукт, аналогичный тому, который образуется при катализе природного субстрата, и является мощным ингибитором человеческой аргиназы I.
Роль в сексуальной реакции
Аргиназа II коэкспрессируется с синтазой оксида азота (NO) в гладких мышечных тканях, таких как мышцы гениталий как мужчин, так и женщин. Сокращение и расслабление этих мышц связано с NO-синтазой, которая вызывает быстрое расслабление гладкой мышечной ткани и способствует нагрубанию ткани, необходимому для нормальной сексуальной реакции. Однако, поскольку NO-синтаза и аргиназа конкурируют за один и тот же субстрат (L-аргинин), сверхэкспрессированная аргиназа может влиять на активность NO-синтазы и NO-зависимую релаксацию гладких мышц, истощая пул субстрата L-аргинина, который в противном случае был бы доступен для NO. синтаза. Напротив, ингибирование аргиназы с помощью ABH или других ингибиторов бороновой кислоты будет поддерживать нормальные клеточные уровни аргинина, тем самым обеспечивая нормальное расслабление мышц и сексуальную реакцию.
Аргиназа является контролирующим фактором как мужской эректильной функции, так и женского сексуального возбуждения, и поэтому является потенциальной мишенью для лечения сексуальной дисфункции у обоих полов. Кроме того, добавление к диете дополнительного количества L-аргинина уменьшит конкуренцию между аргиназой и NO-синтазой, обеспечивая дополнительный субстрат для каждого фермента.
Патология
Дефицит аргиназы обычно относится к снижению функции аргиназы I, печеночной изоформы аргиназы. Этот дефицит обычно называют гипераргининемией или аргинемией . Заболевание наследственное и аутосомно- рецессивное. Он характеризуется пониженной активностью аргиназы в клетках печени . Считается, что это самый редкий из наследственных дефектов уреагенеза . Дефицит аргиназы, в отличие от других нарушений цикла мочевины, не предотвращает полностью уреагенез. Предполагаемая причина продолжения функции аргиназы заключается в повышенной активности аргиназы II в почках субъектов с дефицитом аргиназы I. Исследователи полагают, что накопление аргинина вызывает повышение экспрессии аргиназы II. Ферменты в почках будут затем катализировать уреагенез, частично компенсируя снижение активности аргиназы I в печени. Благодаря этому альтернативному методу удаления избытка аргинина и аммиака из кровотока, субъекты с дефицитом аргиназы, как правило, имеют более длительную продолжительность жизни, чем те, у кого есть другие дефекты цикла мочевины.
Симптомы расстройства включают неврологические нарушения, слабоумие , задержку роста и гипераммониемию. Хотя некоторые симптомы заболевания можно контролировать с помощью диетических ограничений и фармацевтических разработок, в настоящее время не существует лекарства или полностью эффективной терапии.
Рекомендации
Внешние ссылки
- Аргиназа в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH)
- GeneReviews / NIH / NCBI / UW запись о дефиците аргиназы
- Подпись и профиль семейства аргиназ в PROSITE
