Химия органо-галлия - Organogallium chemistry
Галлийорганические Соединения является химия из металлоорганических соединений , содержащих углерод в галлия (Ga) химической связи . Несмотря на их высокую токсичность, галлийорганические соединения находят применение в органическом синтезе . Соединение триметилгаллий имеет определенное значение для MOCVD как предшественник арсенида галлия через его реакцию с арсином при 700 ° C:
- Ga (CH 3 ) 3 + AsH 3 → GaAs + 3CH 4
Трихлорид галлия - важный реагент для введения галлия в органические соединения.
Основная степень окисления галлия - это Ga (III), как и все элементы низшей группы 13 (например, алюминий ).
Химия галлийорганического (III)
Соединения типа R 3 Ga являются мономерными. Кислотность по Льюису уменьшается в порядке Al> Ga> In, и в результате галлийорганические соединения не образуют мостиковых димеров, как это делают алюминийорганические соединения. Галлийорганические соединения также менее активны, чем алюминийорганические соединения. Они действительно образуют стабильные пероксиды.
Галлийорганические соединения можно синтезировать трансметаллированием , например, реакцией металлического галлия с диметилртутью :
- 2Ga + 3Me 2 Hg → 2Me 3 Ga + 3 Hg
или через литийорганические соединения или Гриньяр :
- GaCl 3 + 3MeMgBr → Me 3 Ga + 3MgBrCl
Электронодефицитная природа галлия может быть устранена путем образования комплекса , например
- Me 2 GaCl + NH 3 → [Me 2 Ga (NH 3 ) Cl] + Cl -
Также известно образование комплекса Pi с алкинами .
Галлийорганические соединения являются реагентами или промежуточными продуктами в нескольких классах органических реакций:
- Реакции типа Барбье с элементарным галлием, аллильными субстратами и карбонильными соединениями
- Реакции карбометаллирования (карбогаллирования)
Высшая группа 13 Металлоорганическая химия
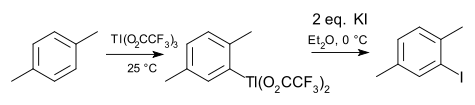
Химия органоиндия и химия органоиндия (Tl) во многих отношениях параллельны химии органоиндия . Индий и таллий в степени окисления +1 являются более распространенными, например, металлоцены циклопентадиенилиндий (I) и циклопентадиенилталлий . Триметилиндий играет важную роль в полупроводниковой промышленности. Особенностью таллия является электрофильное таллирование ареновых соединений , напоминающее меркурирование (сосед группы 12). Обычным реагентом для этой цели является трифторацетат таллия (III) . Промежуточный бисфторацетат арилталлия можно выделить и превратить в арилгалогенид, арилцианид, арилтиол или нитроарен. Примером может служить йодирование пара-ксилола .
Особая тема нишевого исследования индия - опосредованное индием аллилирование .