НАДН пероксидаза - NADH peroxidase
| НАДН пероксидаза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
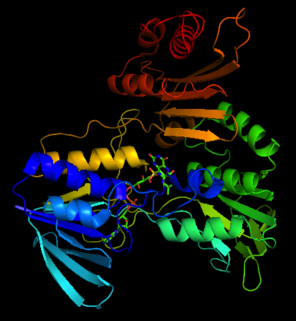
| |||||||||
| Идентификаторы | |||||||||
| ЕС нет. | 1.11.1.1 | ||||||||
| № CAS | 9032-24-0 | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| BRENDA | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| Структуры PDB | RCSB PDB PDBe PDBsum | ||||||||
| Генная онтология | Amigo / QuickGO | ||||||||
| |||||||||
В энзимологии , в NADH пероксидазе ( ЕС 1.11.1.1 ) представляет собой фермент , который катализирует в химическую реакцию
- НАД + Н + + Н 2 О 2 НАД + + 2 Н 2 О
Предполагаемая функция пероксидазы НАДН состоит в том, чтобы инактивировать H 2 O 2, образующийся в клетке, например, глицерин-3-фосфатоксидазой во время метаболизма глицерина или дисмутации супероксида , прежде чем H 2 O 2 вызовет повреждение основных клеточных компонентов.
В 3 субстратов этого фермента НАДНЫ , Н + и Н 2 О 2 , в то время как две его продуктов являются НАД + и Н 2 О . В нем используется один кофактор , FAD , однако дискретного промежуточного соединения FADH 2 не наблюдалось.
Этот фермент принадлежит к семейству оксидоредуктаз , в частности тех, которые действуют на пероксид в качестве акцептора (пероксидазы). Систематическое название данного фермента класса NADH: перекись водорода оксидоредуктаз . Другие имена в общем пользовании включают ДПНА пероксидазу , NAD пероксидазы , diphosphopyridine нуклеотидных пероксидазы , NADH-пероксидазу , никотинамидадениндинуклеотид пероксидазу и NADH2 пероксидазу .
Состав
Кристаллическая структура пероксидазы НАДН напоминает глутатионредуктазу в отношении складки цепи и расположения, а также конформации простетической группы FAD.
His10 пероксидазы NADH расположен рядом с N-концом спирали R1 в пределах сайта связывания FAD. Один из атомов кислорода Cys42-SO 3 H связан водородными связями как с имидазолом His10, так и с N-концом Cys42. His10 частично стабилизирует необычный окислительно-восстановительный центр Cys42-SOH. Arg303 также стабилизирует Cys42-SO 3 H. Glu-14 участвует в образовании плотной границы раздела димеров, которая ограничивает доступность растворителя, что важно для поддержания степени окисления сульфеновой кислоты.
Механизм реакции
Пероксидаза НАДН из Enterococcus faecalis уникальна тем, что использует окислительно-восстановительную пару Cys42 тиол / сульфеновая кислота (-SH / -SOH) в гетеролитическом расщеплении пероксидной связи, чтобы катализировать двухэлектронное восстановление пероксида водорода до воды.
Кинетический механизм пероксидазы дикого типа включает (1) восстановление NADH E (FAD, Cys42-SOH) до EH 2 (FAD, Cys42-SH) на начальной стадии примирования; (2) быстрое связывание НАДН с ЕН 2 ; (3) восстановление H 2 O 2 тиолатом Cys42 с образованием E • NADH; и (4) лимитирующий перенос гидрида из связанного NADH, регенерирующий EH 2 . Однако не наблюдалось дискретного промежуточного соединения FADH 2 , и точные детали восстановления Cys42-SOH не были выяснены.
- E + NADH → (EH 2 '• NAD + ) * → EH 2 ' • NAD + → EH 2 + NAD + + H 2 O
- EH 2 + NADH → EH 2 • NADH *
- EH 2 • NADH * + H 2 O 2 → E • NADH + H 2 O
- E • NADH + H + → EH 2 • NAD + + H 2 O
- EH 2 • NAD + → EH 2 + NAD +
Ингибиторы включают Ag + , Cl - , Co 2+ , Cu 2+ , Hg 2+ , NaN 3 , Pb 2+ и SO 4 2- . При субоптимальных концентрациях H 2 O 2 и концентрациях НАДН, которые являются насыщающими, НАДН ингибирует пероксидазную активность НАДН пероксидазы, превращая фермент в нестабильный промежуточный продукт. НАД + действует как активатор, меняя равновесие, которое приводит к нестабильному промежуточному продукту, превращая фермент в кинетически активный комплекс, восстанавливающий H 2 O 2 .
Биологическая функция
НАДН устраняет потенциально токсичный перекись водорода в аэробных условиях роста и представляет собой ферментативную защиту от окислительного стресса, опосредованного H 2 O 2 . Во-вторых, фермент представляет собой дополнительный механизм регенерации NAD +, необходимый для строго ферментативного метаболизма этого организма. Фермент может также защищать от экзогенного H 2 O 2 и способствовать бактериальной вирулентности .
Фактическая функция пероксидаз и оксидаз NADH в растениях до сих пор неясна, но они могут действовать в раннем сигнале окислительного стресса, продуцируя H 2 O 2 .
Альтернативная роль может включать регуляцию образования H 2 O 2 пероксидазой и оксидазой NADH при разрыхлении и реконструкции клеточной стенки.



