Катализатор Крэбтри - Crabtree's catalyst
|
|

|
|
| Имена | |
|---|---|
|
Название ИЮПАК
( SP -4) - (η 2 , η 2 -циклоокта-1,5-диен) (пиридин) (трициклогексилфосфан) иридия (1+) гексафторидофосфат (1-)
|
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.164.161 |
|
PubChem CID
|
|
| UNII | |
|
Панель управления CompTox ( EPA )
|
|
|
|
|
|
| Характеристики | |
| C 31 H 50 F 6 IrNP 2 | |
| Молярная масса | 804,9026 г / моль |
| Появление | Желтые микрокристаллы |
| Температура плавления | 150 ° С (302 ° F, 423 К) (разлагается) |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
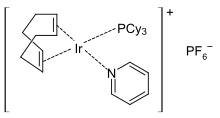
Катализатор Крэбтри представляет собой иридиевое соединение формулы [ C 8 H 12 Ir P (C 6 H 11 ) 3 C 5 H 5 N ] PF 6 . Это гомогенный катализатор реакций гидрирования и переноса водорода, разработанный Робертом Х. Крабтри . Это стабильное на воздухе оранжевое твердое вещество коммерчески доступно и известно своим направленным гидрированием, обеспечивающим трансстереоселективность по отношению к соответствующей направляющей группе.
Структура и синтез
Комплекс имеет плоскую квадратную молекулярную геометрию , как и ожидалось для комплекса ad 8 . Его получают из димера циклооктадиена иридия хлорида .
Реактивность
Катализатор Крэбтри эффективен для гидрирования моно-, ди-, три- и тетразамещенных субстратов. В то время как катализатор Уилкинсона и катализатор Шрока-Осборна не катализируют гидрирование тетразамещенного олефина, катализатор Крэбтри делает это при высоких частотах оборота (таблица).
Частоты оборота Субстрат Катализатор Уилкинсона Катализатор Шрока-Осборна Катализатор Крэбтри Гекс-1-ен 650 4000 6400 Циклогексен 700 10 4500 1-метилциклогексен 13 - 3800 2,3-диметил-бут-2-ен - - 4000
Катализатор реакционноспособен при комнатной температуре. Реакция протекает без осушения растворителей или тщательной деоксигенации водорода. Катализатор толерантен к слабоосновным функциональным группам, таким как сложный эфир, но не к спиртам (см. Ниже) или аминам. Катализатор чувствителен к протоносодержащим примесям.
Катализатор необратимо дезактивируется примерно через десять минут при комнатной температуре, о чем свидетельствует появление желтого цвета. Один процесс дезактивации включает образование димеров с гидридными мостиковыми связями. Как следствие, катализатор Крэбтри обычно используется при очень низкой загрузке катализатора.
Другие каталитические функции: изотопный обмен и изомеризация
Помимо гидрирования, катализатор катализирует изомеризацию и гидроборирование алкенов.
Катализатор Крэбтри используется в реакциях изотопного обмена. В частности, он катализирует прямой обмен атома водорода с его изотопами дейтерием и тритием без использования промежуточных продуктов. Было показано, что изотопный обмен с катализатором Крэбтри очень региоселективен.
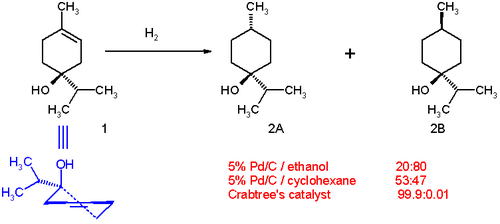
Влияние направляющих функциональных групп
Гидрировании из terpen-4-ола демонстрирует способность соединений с направляющими группами (-ОН группы) , чтобы пройти диастереоселективное гидрирование. С палладием на угле в этаноле распределение продукта составляет 20:80 в пользу цис- изомера ( 2B на схеме 1). Полярная сторона (с гидроксильной группой) взаимодействует с растворителем. Это происходит из-за небольшой гаптофильности, эффекта, при котором функциональная группа связывается с поверхностью гетерогенного катализатора и направляет реакцию. В циклогексане в качестве растворителя распределение изменяется на 53:47, поскольку гаптофильность давно отсутствует (на циклогексане нет направляющей группы). Распределение полностью меняется в пользу цис- изомера 2А, когда катализатор Крэбтри используется в дихлорметане . Эта избирательность предсказуема и практически полезна. Известно также, что карбонильные группы определяют высокую региоселективность гидрирования катализатором Крэбтри.
Направляющий эффект, который вызывает стереоселективность гидрирования терпен-4-ола с катализатором Крэбтри, показан ниже.
История
Крэбтри и аспирант Джордж Моррис открыли этот катализатор в 1970-х годах, работая над иридиевыми аналогами катализатора Уилкинсона на основе родия в Institut de Chimie des Substances Naturelles в Гиф-сюр-Иветт , недалеко от Парижа.
Предыдущие катализаторы гидрирования включали катализатор Уилкинсона и катионный комплекс родия (I) с двумя фосфиновыми группами, разработанный Осборном и Шроком. Эти катализаторы осуществили гидрирование за счет замещения; после добавления водорода через металл растворитель или фосфиновая группа диссоциируют от металлического родия, так что гидрируемый олефин может получить доступ к активному центру. Это смещение происходит быстро для комплексов родия, но практически не происходит для комплексов иридия. Из-за этого исследования в то время были сосредоточены на соединениях родия, а не на соединениях с переходными металлами третьего ряда, такими как иридий. Уилкинсон, Осборн и Шрок также использовали только координирующие растворители.
Крэбтри отметил, что стадия диссоциации лиганда не происходит при гетерогенном катализе , и поэтому предположил, что эта стадия является ограничивающей в гомогенных системах. Они искали катализаторы с «необратимо созданными активными центрами в некоординирующем растворителе». Это привело к разработке катализатора Крэбтри и использованию растворителя CH 2 Cl 2 .