Изогнутая молекулярная геометрия - Bent molecular geometry
| Изогнутая молекулярная геометрия | |
|---|---|
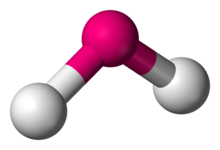 | |
| Примеры | Н 2 О , SO 2 |
| Группа точек | C 2v |
| Координационный номер | 2 |
| Угол крепления | 90 ° <θ <120 ° |
| μ (полярность) | > 0 |

В химии , молекулы с неколлинеарным расположением двух смежных связей имеют изогнутую молекулярную геометрию , также известную как угловые или V-образные . Некоторые атомы, такие как кислород, почти всегда устанавливают свои две (или более) ковалентные связи в неколлинеарных направлениях из-за их электронной конфигурации . Вода (H 2 O) является примером изогнутой молекулы, как и ее аналоги . Угол связи между двумя атомами водорода составляет приблизительно 104,45 °. Нелинейная геометрия обычно наблюдается для других трехатомных молекул и ионов, содержащих только элементы основной группы, яркими примерами которых являются диоксид азота (NO 2 ), дихлорид серы (SCl 2 ) и метилен (CH 2 ).
Эта геометрия почти всегда согласуется с теорией VSEPR , которая обычно объясняет неколлинеарность атомов наличием неподеленных пар . Существует несколько вариантов изгиба, наиболее распространенным из которых является AX 2 E 2, где две ковалентные связи и две неподеленные пары центрального атома (A) образуют полную 8-электронную оболочку . Они имеют центральные углы от 104 ° до 109,5 °, причем последнее согласуется с упрощенной теорией, которая предсказывает тетраэдрическую симметрию четырех sp 3- гибридизованных орбиталей. Наиболее распространенные фактические углы составляют 105 °, 107 ° и 109 °: они различаются из-за различных свойств периферийных атомов (X).
В других случаях также наблюдается орбитальная гибридизация , но в разной степени. Молекулы AX 2 E 1 , такие как SnCl 2 , имеют только одну неподеленную пару и центральный угол около 120 ° (центр и две вершины равностороннего треугольника ). У них есть три орбитали sp 2 . Существуют также sd-гибридизированные соединения AX 2 переходных металлов без неподеленных пар: они имеют центральный угол около 90 ° и также относятся к изогнутым.
