Альтернативное удлинение теломер - Alternative Lengthening of Telomeres
Альтернативное удлинение теломер (также известное как « ALT ») - это независимый от теломеразы механизм, с помощью которого раковые клетки избегают деградации теломер .
Задний план
На каждом конце хромосом большинства эукариотических клеток есть теломеры: область повторяющихся нуклеотидных последовательностей, которая защищает конец хромосомы от разрушения или от слияния с соседними хромосомами. При каждом делении клетки теломеры укорачиваются, что в конечном итоге препятствует дальнейшему делению клеток. Здоровые взрослые соматические клетки млекопитающих не имеют активных ферментов теломеразы, поэтому раковые клетки прекращают пролиферировать, если у них нет мутации, восстанавливающей теломеры. Часто это происходит из-за реактивации фермента теломеразы, но возможны и альтернативные механизмы.
Механизм опосредованного рекомбинацией синтеза теломер
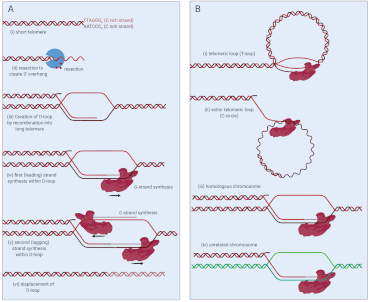
Основным альтернативным механизмом удлинения теломер является тип гомологичной рекомбинации, называемый синтезом теломер, индуцированным разрывом (или BITS). Обычно гомологичная рекомбинация позволяет восстанавливать поврежденные цепи ДНК путем выстраивания с соответствующей последовательностью неповрежденной ДНК, но в BITS этот механизм используется для удлинения теломер. Поскольку теломеры по своей природе повторяются, соответствующие последовательности широко доступны.
В предлагаемых моделях того, как работает BITS, процесс начинается с резекции поврежденного конца теломер: одна из нитей отрезается, чтобы обеспечить единственную цепь ДНК ( цепь, богатую гуанозином ), которая может связываться с совпадающей (гомологичной) цепью. ) шаблон, образуя так называемую петлю смещения ( D-петлю ) (рис. 1а). В ALT есть доказательства того, что эта матрица состоит из: (i) центромерной проксимальной последовательности той же хромосомы ( T-петля ), (ii) кольцевых внехромосомных теломерных последовательностей (C-круги), (iii) гомологичных хромосом или ( iv) другие хромосомы (рисунок 1b). ALT может возникать из комбинации некоторых или всех этих шаблонов. Важно отметить, что поскольку теломеры сильно повторяются, инвазия между теломерами или внутри них не ограничивается требованием расширенной гомологии при гомологичной рекомбинации. После образования D-петли ДНК-полимераза δ удлиняет пораженный конец G-цепи, копируя материал за пределы исходной точки разрыва, что приводит к инициации синтеза отстающей цепи C-цепи, также с помощью ДНК-полимеразы δ.
Вторая особенность ALT - производство неконсервативного продукта ДНК на теломере. По завершении реакции копирования обе нити содержат совершенно новую ДНК. Это отличается от нормальной «полуконсервативной» репликации ДНК , когда одна цепь синтезируется заново, а другая происходит из исходной матрицы. Таким образом, ALT позволяет копировать целые теломерные последовательности с одной хромосомы на другую, не влияя на длину или целостность скопированной последовательности. Недавняя работа предполагает, что копирование ДНК ALT (BITS) происходит с помощью модели миграции D-петли , что подтверждается наблюдением неконсервативных, а не полуконсервативных продуктов репликации, индуцированной разрывом на теломерах ALT и D-образной петле. продукты, наблюдаемые при двумерном гель-электрофорезе на участках, подвергающихся BIR.
Рекомендации
-
^ а б
О'Рурк, JJ; Байтелл-Дуглас, Р. Данн, EA; Динс, AJ (декабрь 2019 г.). «Контроль ALT, исключить: FANCM как противораковая мишень в альтернативном удлинении теломер» . Ядро (Остин, Техас) . 10 (1): 221–230. DOI : 10.1080 / 19491034.2019.1685246 . PMC 6949022 . PMID 31663812 .
 Текст был скопирован из этого источника, доступного по международной лицензии Creative Commons Attribution 4.0 .
Текст был скопирован из этого источника, доступного по международной лицензии Creative Commons Attribution 4.0 .
- ^ Чжан, JM; Ядав, Т; Оуян, Дж; Lan, L; Цзоу, Л. (22 января 2019 г.). «Альтернативное удлинение теломер с помощью двух разных путей репликации, индуцированных разрывом» . Отчеты по ячейкам . 26 (4): 955–968.e3. DOI : 10.1016 / j.celrep.2018.12.102 . PMC 6366628 . PMID 30673617 .
- ^ О'Рурк, Жюльен Дж; Байтелл-Дуглас, Рохан; Данн, Элиз А; Динс, Эндрю Дж (1 января 2019 г.). «Контроль ALT, исключить: FANCM как противораковая мишень в альтернативном удлинении теломер» . Ядро . 10 (1): 221–230. DOI : 10.1080 / 19491034.2019.1685246 . PMC 6949022 . PMID 31663812 .
- ^ Доннианни, РА; Чжоу, ZX; Lujan, SA; Аль-Заин, А; Гарсия, V; Glancy, E; Burkholder, AB; Kunkel, TA; Symington, LS (7 ноября 2019 г.). «ДНК-полимераза дельта синтезирует обе цепи во время репликации, вызванной разрывом» . Молекулярная клетка . 76 (3): 371–381.e4. DOI : 10.1016 / j.molcel.2019.07.033 . PMC 6862718 . PMID 31495565 .
- ^ Мин, Дж; Райт, МЫ; Шей, JW (15 октября 2017 г.). «Альтернативное удлинение теломер, опосредованное митотическим синтезом ДНК, включает процессы репликации, индуцированные разрывом» . Молекулярная и клеточная биология . 37 (20). DOI : 10.1128 / MCB.00226-17 . PMC 5615184 . PMID 28760773 .
- ^ Sneeden, JL; Гросси, С.М. Таппин, я; Гурвиц, Дж; Хейер, WD (май 2013 г.). «Восстановление синтеза ДНК, ассоциированного с рекомбинацией, с человеческими белками» . Исследования нуклеиновых кислот . 41 (9): 4913–25. DOI : 10.1093 / NAR / gkt192 . PMC 3643601 . PMID 23535143 .
