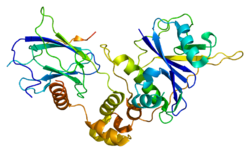
Подавитель опухолей фон Хиппеля – Линдау - Von Hippel–Lindau tumor suppressor
Опухолевый супрессор Гиппеля-Линдау также известный как pVHL является белком , который, в организме человека, кодируется VHL гена . Мутации гена VHL связаны с болезнью фон Хиппеля – Линдау .
Функция
Белок, кодируемый геном VHL, является компонентом распознавания субстрата белкового комплекса, который включает элонгин B , элонгин C и кулин-2 , и обладает активностью убиквитинлигазы E3 . Этот комплекс участвует в убиквитинировании и последующей деградации факторов, индуцируемых гипоксией (HIF), которые являются факторами транскрипции, которые играют центральную роль в регуляции экспрессии генов в ответ на изменение уровня кислорода. Субъединица РНК-полимеразы II POLR2G / RPB7, как сообщается, также является мишенью для этого белка. Наблюдались альтернативно сплайсированные варианты транскриптов, кодирующие разные изоформы.

Результирующий белок продуцируется в двух формах: белок 18 кДа и белок 30 кДа, который действует как супрессор опухоли . Считается, что основным действием белка VHL является его активность убиквитинлигазы E3, которая приводит к тому, что определенные целевые белки «маркируются» для деградации.
Наиболее изученной из этих мишеней является фактор 1а, индуцируемый гипоксией (HIF1a), фактор транскрипции, который индуцирует экспрессию ряда факторов, связанных с ангиогенезом .
HIF необходимы для роста опухоли, потому что большинство видов рака требуют высокой метаболической активности и снабжаются только структурно или функционально неадекватной сосудистой сетью. Активация HIF способствует усилению ангиогенеза , что, в свою очередь, способствует увеличению поглощения глюкозы. В то время как HIF в основном активны в условиях гипоксии, VHL-дефектные клетки карциномы почек обнаруживают конститутивную активацию HIF даже в насыщенной кислородом среде.
Понятно, что VHL и HIF тесно взаимодействуют. Во-первых, все мутации почечно-клеточного рака в VHL, которые были протестированы, влияют на способность белка модифицировать HIF. Кроме того, активация HIF может быть обнаружена на самых ранних этапах онкогенеза у пациентов с синдромом VHL. В нормальных клетках в условиях гипоксии HIF1A активируется с небольшой активацией HIF2A. Однако в опухолях баланс HIF1A и HIF2A склоняется в сторону HIF2A. В то время как HIF1A служит проапоптотическим фактором, HIF2A взаимодействует с циклином D1 . Это приводит к увеличению выживаемости из-за более низкой скорости апоптоза и увеличения пролиферации из-за активации циклина D1. Недавний полногеномный анализ связывания HIF при раке почки показал, что HIF1A связывается выше основных генов хорошего прогноза, тогда как HIF2A связывается выше по течению с генами в основном плохого прогноза. Это указывает на то, что распределение факторов транскрипции HIF при раке почки имеет большое значение в определении исхода для пациентов.
В нормальной клетке с активным белком VHL альфа HIF регулируется гидроксилированием в присутствии кислорода. Когда присутствуют железо, 2-оксоглутарат и кислород, HIF инактивируется гидроксилазами HIF. Гидроксилирование HIF создает сайт связывания для pVHL (белковый продукт гена VHL). pVHL управляет полиубиквитилированием HIF1A, гарантируя, что этот белок будет расщепляться протеасомой. В условиях гипоксии субъединицы HIF1A накапливаются и связываются с HIFB. Этот гетеродимер HIF представляет собой фактор транскрипции, который активирует гены, кодирующие белки, такие как фактор роста эндотелия сосудов ( VEGF ) и эритропоэтин, белки, которые оба участвуют в ангиогенезе. Клетки с аномальным pVHL неспособны нарушить образование этих димеров и поэтому ведут себя так, как будто они гипоксичны, даже в насыщенной кислородом среде.
HIF также был связан с mTOR , центральным контролером решений о росте. Недавно было показано, что активация HIF может инактивировать mTOR.
HIF может помочь объяснить органо-специфическую природу синдрома VHL. Было высказано предположение, что постоянная активация HIF в любой клетке может привести к раку, но есть избыточные регуляторы HIF в органах, не затронутых синдромом VHL. Эта теория многократно опровергалась, поскольку потеря функции VHL во всех типах клеток приводит к конститутивной активации HIF и его последующим эффектам. Другая теория утверждает, что, хотя во всех клетках потеря VHL приводит к активации HIF, в большинстве клеток это не дает преимущества в пролиферации или выживании. Кроме того, природа мутации в белке VHL приводит к фенотипическим проявлениям в структуре развивающегося рака. Нонсенс или делеционные мутации белка VHL были связаны с VHL 1 типа с низким риском феохромоцитомы (опухоли надпочечников). VHL типа 2 связана с миссенс-мутациями и связана с высоким риском феохромоцитомы. Тип 2 также был дополнительно подразделен в зависимости от риска почечно-клеточного рака. В типах 1, 2A и 2B мутант pVHL дефектен в регуляции HIF, в то время как мутант типа 2C дефектен в регуляции протеинкиназы C. Эти корреляции генотип-фенотип предполагают, что миссенс-мутации pVHL приводят к « усилению функции » белка.
Участие VHL в почечно-клеточном раке может быть объяснено множеством характеристик почечных клеток. Во-первых, они более чувствительны к воздействию факторов роста, создаваемых после активации HIF, чем другие клетки. Во-вторых, связь с циклином D1 (как упоминалось выше) наблюдается только в почечных клетках. Наконец, многие клетки почек обычно работают в условиях гипоксии. Это может дать им пролиферативное преимущество перед другими клетками в гипоксической среде.
Помимо взаимодействия с HIF, белок VHL также может связываться с тубулином . Затем он способен стабилизировать и, таким образом, удлинить микротрубочки. Эта функция играет ключевую роль в стабилизации веретена во время митоза. Удаление VHL вызывает резкое увеличение разориентированных и вращающихся веретен во время митоза. Благодаря еще не известному механизму VHL также увеличивает концентрацию MAD2 , важного белка контрольной точки веретена. Таким образом, потеря VHL приводит к ослаблению контрольной точки и, следовательно, к неправильной сегрегации хромосом и анеуплоидии .
Патология
Синдром фон Хиппеля – Линдау (ВХЛ) является доминантно наследуемым наследственным онкологическим синдромом, предрасполагающим к целому ряду злокачественных и доброкачественных опухолей глаза, головного, спинного мозга, почек, поджелудочной железы и надпочечников. Мутация зародышевой линии этого гена является основой семейного наследования синдрома ВХЛ. Люди с синдромом VHL наследуют одну мутацию в белке VHL, которая вызывает потерю или изменение нормальной функции белка. Со временем спорадические мутации во второй копии белка VHL могут привести к карциномам, в частности гемангиобластомам, поражающим печень и почки, почечным (и вагинальным) светлоклеточным аденокарциномам.
Потеря активности белка VHL приводит к увеличению количества HIF1a и, таким образом, к увеличению уровней ангиогенных факторов, включая VEGF и PDGF . В свою очередь, это приводит к нерегулируемому росту кровеносных сосудов , что является одной из предпосылок опухоли . Кроме того, VHL участвует в поддержании дифференцированного фенотипа в почечных клетках. Более того, эксперименты на культуре клеток с VHL - / - клетками показали, что добавление pVHL может индуцировать переход от мезенхимы к эпителию . Эти данные свидетельствуют о том, что VHL играет центральную роль в поддержании дифференцированного фенотипа в клетке.
Кроме того, pVHL важен для образования внеклеточного матрикса . Этот белок также может играть важную роль в ингибировании матриксных металлопротеиназ. Эти идеи чрезвычайно важны при метастазировании VHL-дефицитных клеток. При классической болезни VHL одного аллеля дикого типа в VHL, по-видимому, достаточно для поддержания нормальной сердечно-легочной функции.
Уход
Предлагаемые мишени для рака, связанного с VHL, включают мишени пути HIF, такие как VEGF. Ингибиторы рецептора VEGF сорафениб , сунитиниб , пазопаниб и недавно акситиниб были одобрены FDA. Аналоги ингибитора mTOR рапамицина эверолимус и темсиролимус или моноклональное антитело к VEGF бевацизумаб также могут быть вариантом.
Поскольку железо, 2-оксоглутарат и кислород необходимы для инактивации HIF, было высказано предположение, что недостаток этих кофакторов может снизить способность гидроксилаз инактивировать HIF. Недавнее исследование показало, что в клетках с высокой активацией HIF даже в насыщенной кислородом среде происходило обратное действие путем снабжения клеток аскорбатом. Таким образом, витамин С может быть потенциальным средством лечения опухолей, индуцированных HIF.
Взаимодействия
Было показано, что опухолевый супрессор фон Хиппеля-Линдау взаимодействует с:
Смотрите также
использованная литература
дальнейшее чтение
- Conaway RC, Conaway JW (2003). Комплекс опухолевых супрессоров фон Хиппеля – Линдау и регуляция индуцируемой гипоксией транскрипции . Достижения в исследованиях рака . 85 . С. 1–12. DOI : 10.1016 / S0065-230X (02) 85001-1 . ISBN 978-0120066858. PMID 12374282 .
- Чзык-Кшеска М.Ф., Меллер Дж. (Апрель 2004 г.). «Подавитель опухолей фон Хиппеля – Линдау: не только палач HIF». Тенденции молекулярной медицины . 10 (4): 146–9. DOI : 10.1016 / j.molmed.2004.02.004 . PMID 15162797 .
- Эстебан М.А., Хартен С.К., Тран М.Г., Максвелл PH (июль 2006 г.). «Формирование первичных ресничек в почечном эпителии регулируется опухолевым супрессорным белком фон Хиппеля – Линдау» . Журнал Американского общества нефрологов . 17 (7): 1801–1806. DOI : 10,1681 / ASN.2006020181 . PMID 16775032 .
- Hoebeeck J, Vandesompele J, Nilsson H, De Preter K, Van Roy N, De Smet E, Yigit N, De Paepe A, Laureys G, Påhlman S, Speleman F (август 2006 г.). «Уровень экспрессии гена-супрессора опухоли фон Хиппеля-Линдау имеет прогностическое значение при нейробластоме» . Международный журнал рака . 119 (3): 624–9. DOI : 10.1002 / ijc.21888 . PMID 16506218 . S2CID 632377 .
- Kaelin WG (сентябрь 2004 г.). "Ген-супрессор опухоли фон Хиппеля-Линдау и рак почки" . Клинические исследования рака . 10 (18 Pt 2): 6290S – 5S. DOI : 10.1158 / 1078-0432.CCR-sup-040025 . PMID 15448019 .
- Kaelin WG (январь 2007 г.). "Белок-супрессор опухоли фон Хиппеля-Линдау и светлоклеточная карцинома почек" . Клинические исследования рака . 13 (2 Pt 2): 680–684 с. DOI : 10.1158 / 1078-0432.CCR-06-1865 . PMID 17255293 .
- Камура Т., Конавей Дж. У., Конавей Р. К. (2002). «Роль убиквитинлигаз SCF и VHL в регуляции роста клеток». Распад белка при здоровье и болезнях . Прогресс в молекулярной и субклеточной биологии . 29 . С. 1–15. DOI : 10.1007 / 978-3-642-56373-7_1 . ISBN 978-3-642-62714-9. PMID 11908068 .
- Kralovics R, Skoda RC (январь 2005 г.). "Молекулярный патогенез миелопролиферативных нарушений, отрицательных по филадельфийской хромосоме". Обзоры крови . 19 (1): 1–13. DOI : 10.1016 / j.blre.2004.02.002 . PMID 15572213 .
- Lonser RR, Glenn GM, Walther M, Chew EY, Libutti SK, Linehan WM, Oldfield EH (июнь 2003 г.). «Болезнь фон Хиппеля – Линдау». Ланцет . 361 (9374): 2059–67. DOI : 10.1016 / S0140-6736 (03) 13643-4 . PMID 12814730 . S2CID 13783714 .
- Neumann HP, Wiestler OD (май 1991 г.). «Кластеризация признаков синдрома фон Хиппеля-Линдау: свидетельство сложного генетического локуса». Ланцет . 337 (8749): 1052–4. DOI : 10.1016 / 0140-6736 (91) 91705-Y . PMID 1673491 . S2CID 24022884 .
- Russell RC, Ohh M (январь 2007 г.). «Роль VHL в регуляции E-кадгерина: новое соединение в старом пути» . Клеточный цикл . 6 (1): 56–9. DOI : 10.4161 / cc.6.1.3668 . PMID 17245122 .
- Схипани Э. (2006). «Гипоксия и HIF-1 альфа в хондрогенезе». Семинары по клеточной биологии и биологии развития . 16 (4–5): 539–46. DOI : 10.1016 / j.semcdb.2005.03.003 . PMID 16144691 .
- Такахаши К., Иида К., Окимура Ю., Такахаши Ю., Наито Дж., Нисикава С., Кадоваки С., Игучи Г., Кадзи Н., Чихара К. (2006). «Новая мутация в гене-супрессоре опухоли фон Хиппеля-Линдау, идентифицированная в японской семье с феохромоцитомой и гемангиомой печени» . Внутренняя медицина . 45 (5): 265–9. DOI : 10.2169 / internalmedicine.45.1547 . PMID 16595991 .
- Графф Дж. В. (2005). «Справочник ВХЛ: что нужно знать о ВХЛ». Семейный альянс ВХЛ . 12 (1): 1–56.