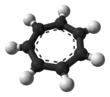
Катион тропилия - Tropylium cation
 |
|||
|
|
|||
| Имена | |||
|---|---|---|---|
|
Предпочтительное название IUPAC
Циклогептатриенилий |
|||
| Другие имена
цикл - C
7ЧАС+ 7, Циклогепта-2,4,6-триенилий, Циклогепта-1,3,5-триен, 2,4,6-Циклогептатриенилий |
|||
| Идентификаторы | |||
|
3D модель ( JSmol )
|
|||
| 1902352 | |||
| ChemSpider | |||
|
PubChem CID
|
|||
|
|||
|
|||
| Характеристики | |||
|
C 7ЧАС+ 7 |
|||
| Молярная масса | 91,132 г · моль -1 | ||
| Структура | |||
| Д 7ч | |||
| правильный семиугольник | |||
| Родственные соединения | |||
|
Другие анионы
|
Тропилий тетрафторборат | ||
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|||
| Ссылки на инфобоксы | |||
В области органической химии , то тропилия ион или циклогептатриенил катион представляет Н. ароматические виды с формулой [C 7 H 7 ] + . Его название происходит от молекулы тропина, из которой циклогептатриен (тропилиден) был впервые синтезирован в 1881 году. Соли катиона тропилия могут быть стабильными, даже с нуклеофилами умеренной силы, например тетрафторборатом тропилия и бромидом тропилия ( см. Ниже ). Его бромидные и хлоридные соли могут быть получены из циклогептатриена и брома или пентахлорида фосфора соответственно.
Это правильный семиугольный , планарный, циклический ион. Он имеет 6 π-электронов (4 n + 2, где n = 1), что соответствует правилу ароматичности Хюккеля . Он может координироваться как лиганд с атомами металла . Показанная структура представляет собой композицию из семи резонансных составляющих, в которых каждый атом углерода несет часть положительного заряда.
История
В 1891 г. Г. Мерлинг получил водорастворимое бромсодержащее соединение по реакции циклогептатриена и брома . В отличие от большинства гидрокарбилбромидов, это соединение, позднее названное бромидом тропилия, растворимо в воде, но нерастворимо во многих органических растворителях. Очищается кристаллизацией из горячего этанола. Реакция с водным раствором нитрата серебра немедленно дает бромид серебра, что указывает на лабильный бромид. Бромид тропилия был выведен как соль, C
7ЧАС+
7Br-
, По Doering и Нокс в 1954 году путем анализа его инфракрасного и ультрафиолетового спектров. Ионные структуры перхлората тропилия ( C
7ЧАС+
7ClO-
4) и иодид тропилия ( C
7ЧАС+
7я-
) подтверждены рентгеноструктурным анализом . Длина связи углерод-углерод больше (147 мкм), чем у бензола (140 мкм), но все же короче, чем у типичных соединений с одинарными связями, таких как этан (154 мкм).
Кислотность
Ион тропилия представляет собой кислоту в водном растворе (т.е. кислоту Аррениуса ) вследствие своей кислотности Льюиса: сначала он действует как кислота Льюиса, образуя аддукт с водой, который затем может отдавать протон другой молекуле воды:
-
C
7ЧАС+
7+ 2 часа
2O ⇌ C
7ЧАС
7ОН + Н
3О+
( Борная кислота дает кислые водные растворы почти таким же образом.) Константа равновесия равна1,8 × 10 -5 , что делает его примерно таким же кислым в воде, как уксусная кислота .
Масс-спектрометрии
Ион тропилия часто встречается в масс-спектрометрии в виде сигнала при m / z = 91 и используется в масс-спектрометрии . Этот фрагмент часто встречается для ароматических соединений, содержащих бензильное звено. При ионизации бензильный фрагмент образует катион ( PhCH+
2), который перестраивается в высокостабильный катион тропилия ( C
7ЧАС+
7).
Реакции
Катион тропилия реагирует с нуклеофилами с образованием замещенных циклогептатриенов, например:
-
C
7ЧАС+
7+ CN-
→ С
7ЧАС
7CN
Восстановление алюмогидридом лития дает циклогептатриен .
Реакция с циклопентадиенидной солью натрия или лития дает 7-циклопентадиенилциклогепта-1,3,5-триен :
-
C
7ЧАС+
7Икс-
+ C
5ЧАС-
5Na+
→ С
7ЧАС
7C
5ЧАС
5+ NaX
При обработке окислителями, такими как хромовая кислота , катион тропилия претерпевает перегруппировку в бензальдегид :
-
C
7ЧАС+
7+ HCrO-
4→ С
6ЧАС
5CHO + CrO
2+ H
2О
Известно много металлических комплексов иона тропилия. Одним из примеров является [Mo ( η 7 -C 7 H 7 ) (CO) 3 ] + , который получают отщеплением гидрида от трикарбонила циклогептатриенмолибдена .