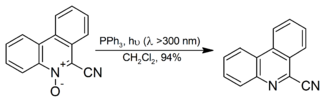Трифенилфосфин - Triphenylphosphine

|
|

|
|

|
|

|
|
| Имена | |
|---|---|
|
Предпочтительное название IUPAC
Трифенилфосфан |
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.009.124 |
| Номер ЕС | |
|
PubChem CID
|
|
| Номер RTECS | |
| UNII | |
|
Панель управления CompTox ( EPA )
|
|
|
|
|
|
| Характеристики | |
| C 18 H 15 P | |
| Молярная масса | 262,292 г · моль -1 |
| Появление | Белый твердый |
| Плотность | 1,1 г см -3 , твердое вещество |
| Температура плавления | 80 ° С (176 ° F, 353 К) |
| Точка кипения | 377 ° С (711 ° F, 650 К) |
| Нерастворимый | |
| Растворимость | органические растворители |
| Кислотность (p K a ) | 7,64 (p K a конъюгированной кислоты в ацетонитриле) |
| -166,8 · 10 −6 см 3 / моль | |
|
Показатель преломления ( n D )
|
1,59; ε r и т. д. |
| Состав | |
| Пирамидальный | |
| 1,4 - 1,44 Д | |
| Опасности | |
| Паспорт безопасности | Джей Ти Бейкер |
|
Классификация ЕС (DSD) (устарела)
|
Нет в списке |
| R-фразы (устаревшие) | R20 R22 R40 R43 R50 R53 |
| S-фразы (устаревшие) | S36 S37 S45 S57 S60 |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | 180 ° С (356 ° F, 453 К) |
| Родственные соединения | |
|
Родственные третичные фосфины
|
Триметилфосфин фосфин |
|
Родственные соединения
|
Трифениламин Трифениларсин Трифенилфосфиноксид Трифенилфосфинсульфид Трифенилфосфин дихлорид Трифенилфосфин селенид , Pd (PPh 3 ) 4 |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
Трифенилфосфин (название IUPAC: трифенилфосфан ) представляет собой обычное фосфорорганическое соединение с формулой P (C 6 H 5 ) 3 и часто сокращенно P Ph 3 или Ph 3 P. Он широко используется в синтезе органических и металлоорганических соединений. PPh 3 существует в виде относительно устойчивых на воздухе бесцветных кристаллов при комнатной температуре. Растворяется в неполярных органических растворителях, таких как бензол и диэтиловый эфир .
Подготовка и состав
Трифенилфосфин может быть получен в лаборатории путем обработкой трихлорида фосфора с фенилмагнийбромид или фениллитиями . Промышленный синтез включает реакцию между трихлоридом фосфора , хлорбензолом и натрием:
- PCl 3 + 3 PhCl + 6 Na → PPh 3 + 6 NaCl
Трифенилфосфин кристаллизуется в триклинной и моноклинной модификации. В обоих случаях молекула принимает пирамидальную структуру с пропеллероподобным расположением трех фенильных групп.
Основные реакции с халькогенами, галогенами и кислотами
Окисление
Трифенилфосфин подвергается медленному окислению воздухом с образованием оксида трифенилфосфина , Ph 3 PO:
- 2 PPh 3 + O 2 → 2 OPPh 3
Эта примесь может быть удалена перекристаллизацией PPh 3 из горячего этанола или горячего изопропанола . Этот метод основан на том факте, что OPPh 3 более полярен и, следовательно, более растворим в полярных растворителях, чем PPh 3 .
Трифенилфосфин извлекает серу из полисульфидных соединений, эписульфидов и элементарной серы . Однако простые сероорганические соединения, такие как тиолы и тиоэфиры, не вступают в реакцию. Фосфорсодержащий продукт - сульфид трифенилфосфина , Ph 3 PS. Эту реакцию можно использовать для анализа содержания «лабильного» S 0 в образце, например, вулканизированной резине. Селенид трифенилфосфина, Ph 3 PSe, может быть легко получен обработкой PPh 3 красным (альфа-моноклинным) Se . Соли селеноцианата , SeCN - , используются в качестве источника Se 0 . PPh 3 также может образовывать аддукт с Te, хотя этот аддукт в основном существует как (Ph 3 P) 2 Te, а не PPh 3 Te.
Арильные азиды реагируют с PPh 3 , чтобы дать phosphanimines, аналоги OPPh 3 , с помощью реакции Staudinger . Показательным является получение фенилимида трифенилфосфина :
- PPh 3 + НЗП 3 → PhNPPh 3 + N 2
Фосфанимин можно гидролизовать до амина. Обычно промежуточный фосфанимин не выделяют.
- PPh 3 + RN 3 + H 2 O → OPPh 3 + N 2 + RNH 2
Хлорирование
Cl 2 добавляют к PPh 3 с образованием дихлорида трифенилфосфина ([PPh 3 Cl] Cl), который существует в виде чувствительного к влаге галогенида фосфония . Этот реагент используется для превращения спиртов в алкилхлориды в органическом синтезе . Бис (трифенилфосфин) иминийхлорид (PPN + Cl - , формула [(C 6 H 5 ) 3 P) 2 N] Cl получают из дихлорида трифенилфосфина:
- 2 Ph 3 PCl 2 + NH 2 OH · HCl + Ph 3 P → {[Ph 3 P] 2 N} Cl + 4HCl + Ph 3 PO
Протонирование
PPh 3 - слабая база. Он образует выделяемые соли трифенилфосфония с сильными кислотами, такими как HBr:
- P (C 6 H 5 ) 3 + HBr → [HP (C 6 H 5 ) 3 ] + Br -
Органические реакции
PPh 3 широко используется в органическом синтезе . Свойства, которые определяют его использование, - это его нуклеофильность и его восстанавливающий характер. На нуклеофильность PPh 3 указывает его реакционная способность по отношению к электрофильным алкенам, таким как акцепторы Михаэля и алкилгалогениды. Он также используется в синтезе биарильных соединений, таких как реакция Сузуки .
Кватернизация
PPh 3 соединяется с алкилгалогенидами с образованием солей фосфония . Эта реакция кватернизации особенно быстра для бензиловых и аллильных галогенидов:
- PPh 3 + CH 3 I → [CH 3 PPh 3 ] + I -
Эти соли, которые часто можно выделить в виде кристаллических твердых веществ, реагируют с сильными основаниями с образованием илидов , которые являются реагентами в реакциях Виттига .
Арилгалогениды будут кватернизовать PPh 3 с образованием солей тетрафенилфосфония :
- PPh 3 + PhBr → [PPh 4 ] Br
Однако реакция требует повышенных температур и металлических катализаторов.
Мицунобу реакция
В реакции Мицунобу смесь трифенилфосфина и диизопропилазодикарбоксилата («DIAD» или его диэтиловый аналог, DEAD ) превращает спирт и карбоновую кислоту в сложный эфир. ДИАД уменьшается , поскольку это служит в качестве акцептора водорода, и PPh 3 окисляется до OPPh 3 .
Реакция Аппеля
В реакции Аппеля смесь PPh 3 и CX 4 (X = Cl, Br) используется для превращения спиртов в алкилгалогениды. Оксид трифенилфосфина (OPPh 3 ) является побочным продуктом.
- PPh 3 + CBr 4 + RCH 2 OH → OPPh 3 + RCH 2 Br + HCBr 3
Эта реакция начинается с нуклеофильной атаки PPh 3 на CBr 4 , что является продолжением реакции кватернизации, указанной выше.
Деоксигенация
Легкая оксигенация PPh 3 используется для деоксигенации органических пероксидов, что обычно происходит с сохранением конфигурации:
- PPh 3 + RO 2 H → OPPh 3 + ROH (R = алкил)
Он также используется для разложения органических озонидов на кетоны и альдегиды, хотя диметилсульфид более популярен для реакции в качестве побочного продукта, диметилсульфоксид легче отделяется от реакционной смеси, чем оксид трифенилфосфина. Ароматические N- оксиды восстанавливаются до соответствующего амина с высоким выходом при комнатной температуре с облучением:
Сульфирование
Сульфирование PPh 3 дает трис (3-сульфофенил) фосфин, P (C 6 H 4 -3-SO 3 - ) 3 ( TPPTS ), обычно выделяемый в виде тринатриевой соли. В отличие от PPh 3 , TPPTS водорастворим, как и его производные в металлах. Комплексы родия TPPTS используются в некоторых промышленных реакциях гидроформилирования .

Восстановление до дифенилфосфида
Литий в THF, а также Na или K реагируют с PPh 3 с образованием Ph 2 PM (M = Li, Na, K). Эти соли являются универсальными предшественниками третичных фосфинов. Например, 1,2-дибромэтан и Ph 2 PM реагируют с образованием Ph 2 PCH 2 CH 2 PPh 2 . Слабые кислоты, такие как хлорид аммония , превращают Ph 2 PM (M = Li, Na, K) в дифенилфосфин :
- (C 6 H 5 ) 2 PM + H 2 O → (C 6 H 5 ) 2 PH + MOH
Комплексы переходных металлов
Трифенилфосфин хорошо связывается с большинством переходных металлов , особенно с металлами средних и поздних переходов групп 7–10. Что касается стерического объема, PPh 3 имеет угол конуса Толмена 145 °, который является промежуточным между углами конуса P (C 6 H 11 ) 3 (170 °) и P (CH 3 ) 3 (115 °). На раннем этапе применения в гомогенном катализе NiBr 2 ( PPh 3 ) 2 использовался Вальтером Реппе для синтеза сложных эфиров акрилата из алкинов , монооксида углерода и спиртов . Использование PPh 3 стало популярным благодаря его использованию в катализаторе гидроформилирования RhH (PPh 3 ) 3 (CO).
Полимерно-закрепленные производные PPh 3
Известны полимерные аналоги PPh 3 , в которых полистирол модифицирован группами PPh 2 в пара-положении. Такие полимеры могут использоваться во многих областях применения PPh 3 с тем преимуществом, что полимер, будучи нерастворимым, может быть отделен от продуктов простой фильтрацией реакционных суспензий. Такие полимеры получают путем обработки 4-lithiophenyl-замещенный полистирол с chlorodiphenylphosphine (PPh 2 Cl).
Смотрите также
Рекомендации
- ^ Международный союз чистой и прикладной химии (2014). Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные наименования 2013 . Королевское химическое общество . п. 431. DOI : 10.1039 / 9781849733069 . ISBN 978-0-85404-182-4.
- ^ Хаав, Кристьян; Сааме, Яан; Кютт, Агнес; Лейто, Иво (2012). «Основность фосфанов и дифосфанов в ацетонитриле». Европейский журнал органической химии . 2012 (11): 2167–2172. DOI : 10.1002 / ejoc.201200009 . ISSN 1434-193X .
- ^ Warchol, M .; Дикарло, EN; Марьянов, Калифорния; Мислоу, К. (1975). «Доказательства вклада неподеленной пары в молекулярный дипольный момент триарилфосфинов». Буквы тетраэдра . 16 (11): 917–920. DOI : 10.1016 / S0040-4039 (00) 72019-3 .
- ^ Corbridge, декабрь (1995). Фосфор: Очерк его химии, биохимии и технологии (5-е изд.). Амстердам: Эльзевир. ISBN 0-444-89307-5.
- ^ Kooijman, H .; Spek, AL; ван Боммель, KJC; Verboom, W .; Рейнхудт Д. Н. (1998). «Триклинная модификация трифенилфосфина» (PDF) . Acta Crystallographica . C54 (11): 1695–1698. DOI : 10.1107 / S0108270198009305 .
- ^ Данн, Би Джей; Орпен, AG (1991). «Трифенилфосфин: новое определение» (PDF) . Acta Crystallographica . C47 (2): 345–347. DOI : 10.1107 / S010827019000508X .
- ^ Armarego, WLF; Perrin, DD; Перрин, Д.Р. (1980). Очистка лабораторных химикатов (2-е изд.). Нью-Йорк: Пергамон. п. 455. ISBN 9780080229614.
- ^ Джонс, CHW; Шарма, RD (1987). " 125 Te ЯМР и мессбауэровская спектроскопия комплексов теллура-фосфина и теллуроцианатов". Металлоорганические соединения . 6 (7): 1419–1423. DOI : 10.1021 / om00150a009 .
- ^ Ерш, JK; Шленц, WJ (1974). μ-nitrido-Бис (triphenylphosphorus) (1+ ( "ППН") Соли с карбонила металла анионами . .. Inorg Synth . Неорганические синтезы 15 . С. 84-90.. DOI : 10.1002 / 9780470132463.ch19 . ISBN 9780470132463.
- ^ Hercouet, A .; ЛеКорре, М. (1988) Трифенилфосфония бромид: удобный и количественный источник газообразного бромистого водорода. Синтез, 157–158.
- ^ Кобб, JE; Криббс, см; Хенке, BR; Uehling, DE; Hernan, AG; Martin, C .; Райнер, CM (2004). «Трифенилфосфин». В Л. Пакетте (ред.). Энциклопедия реагентов для органического синтеза . Нью-Йорк: J. Wiley & Sons. DOI : 10.1002 / 047084289X.rt366.pub2 . ISBN 0471936235.
- ^ Берк, SD; Danheiser, RL (1999). «Трифенилфосфин». Справочник реагентов для органического синтеза, окислителей и восстановителей . Вайли. п. 495. ISBN 978-0-471-97926-5.
- ^ Херрманн, Вашингтон; Кольпайнтнер, CW (1998). Синтезы водорастворимых фосфинов и комплексов их переходных металлов . Неорг. Synth . Неорганические синтезы. 32 . С. 8–25. DOI : 10.1002 / 9780470132630.ch2 . ISBN 9780470132630.
- ^ Джордж У. Лютер III, Гордон Бейерле (1977). «Дифенилфосфид лития и дифенил (триметилсилил) фосфин». Неорганические синтезы . Неорганические синтезы. 17 . С. 186–188. DOI : 10.1002 / 9780470132487.ch51 . ISBN 9780470132487.CS1 maint: использует параметр авторов ( ссылка )
- ^ а б В. Д. Бьянко С. Доронцо (1976). «Дифенилфосфин». Неорганические синтезы . Неорганические синтезы. 16 . С. 161–188. DOI : 10.1002 / 9780470132470.ch43 . ISBN 9780470132470.CS1 maint: использует параметр авторов ( ссылка )
- ^ Elschenbroich, C .; Зальцер, А. (1992). Металлоорганические соединения: краткое введение (2-е изд.). Вайнхайм: Wiley-VCH. ISBN 3-527-28165-7.
- ^ Immirzi, A .; Муско, А. (1977). «Метод измерения размеров лигандов фосфора в координационных комплексах». Inorganica Chimica Acta . 25 : L41 – L42. DOI : 10.1016 / S0020-1693 (00) 95635-4 .
- ^ * Reppe, W .; Schweckendiek, WJ (1948). "Cyclisierende Polymerisation von Acetylen. III Benzol, Benzolderivate und hydroaromatische Verbindungen". Юстус Либигс Аннален дер Хеми . 560 (1): 104–116. DOI : 10.1002 / jlac.19485600104 .