Тетраиодид титана - Titanium tetraiodide
|
|

|
|
| Имена | |
|---|---|
|
Название ИЮПАК
Иодид титана (IV)
|
|
| Другие имена
Тетраиодид титана
|
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.028.868 |
| Номер ЕС | |
|
PubChem CID
|
|
|
Панель управления CompTox ( EPA )
|
|
|
|
|
|
| Характеристики | |
| TiI 4 | |
| Молярная масса | 555,485 г / моль |
| Появление | красно-коричневые кристаллы |
| Плотность | 4,3 г / см 3 |
| Температура плавления | 150 ° С (302 ° F, 423 К) |
| Точка кипения | 377 ° С (711 ° F, 650 К) |
| гидролиз | |
| Растворимость в других растворителях | растворим в CH 2 Cl 2 CHCl 3 CS 2 |
| Состав | |
| кубическая ( a = 12,21 Å) | |
| четырехгранный | |
| 0 Д | |
| Опасности | |
| Основные опасности | насильственный гидролиз коррозионные |
| R-фразы (устаревшие) | 34–37 |
| S-фразы (устаревшие) | 26-36 / 37 / 39-45 |
| Родственные соединения | |
|
Другие анионы
|
Бромид титана (IV) Хлорид титана (IV) Фторид титана (IV) |
|
Другие катионы
|
Тетраиодид кремния Иодид циркония (IV) Иодид гафния (IV) |
|
Родственные соединения
|
Иодид титана (III) |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
Тетраиодид титана представляет собой неорганическое соединение с формулой TiI 4 . Это черное летучее твердое вещество, о котором впервые сообщил Рудольф Вебер в 1863 году. Это промежуточное соединение в процессе очистки титана ван Аркеля – де Бура .
Физические свойства
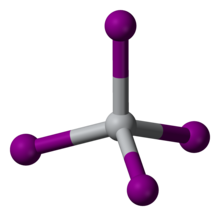
TiI 4 - редкий молекулярный бинарный иодид металла, состоящий из изолированных молекул тетраэдрических центров Ti (IV). Расстояния Ti-I составляют 261 пм . Отражая его молекулярный характер, TiI 4 можно перегонять без разложения при одной атмосфере; это свойство лежит в основе его использования в процессе Ван Аркеля – де Бура. Разница в температуре плавления между TiCl 4 (температура плавления -24 ° C) и TiI 4 (температура плавления 150 ° C) сопоставима с разницей между температурами плавления CCl 4 (температура плавления -23 ° C) и CI 4 (температура плавления 168 ° C). C), что отражает более сильную межмолекулярную ван-дер-ваальсовую связь в иодидах.
Существует два полиморфа TiI 4 , один из которых хорошо растворяется в органических растворителях. В менее растворимой кубической форме расстояния Ti-I составляют 261 пм .
Производство
Хорошо известны три метода: 1) Из элементов, обычно с использованием трубчатой печи при 425 ° C:
- Ti + 2 I 2 → TiI 4
Эту реакцию можно обратить, чтобы получить пленки металлического Ti высокой чистоты.
2) Обменная реакция тетрахлорида титана и HI.
- TiCl 4 + 4 HI → TiI 4 + 4 HCl
3) Оксидно-иодидный обмен от иодида алюминия .
- 3 TiO 2 + 4 AlI 3 → 3 TiI 4 + 2 Al 2 O 3
Реакции
Подобно TiCl 4 и TiBr 4 , TiI 4 образует аддукты с основаниями Льюиса, и он также может быть восстановлен. Когда восстановление проводят в присутствии металлического Ti, получают полимерные производные Ti (III) и Ti (II), такие как CsTi 2 I 7 и цепной CsTiI 3 соответственно.
TiI 4 проявляет обширную реакционную способность по отношению к алкенам и алкинам, что приводит к образованию йодорганических производных. Он также влияет на связывание пинакола и другие реакции образования связи CC.
