Дисульфид кремния - Silicon disulfide

|
|
|
|
|
|
| Имена | |
|---|---|
|
Название ИЮПАК
сульфид кремния (IV)
|
|
| Другие имена
дисульфид кремния
|
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.033.935 |
|
PubChem CID
|
|
| UNII | |
|
Панель управления CompTox ( EPA )
|
|
|
|
|
|
| Характеристики | |
| SiS 2 | |
| Молярная масса | 92,218 г / моль |
| Появление | Белые (иногда серая или коричневая) хвоя. Запах тухлых яиц во влажном воздухе. |
| Плотность | 1,853 г / см 3 |
| Температура плавления | 1090 ° C (1,990 ° F, 1360 K) возгоны |
| Разлагается | |
| Состав | |
| Ромбическая , oI12 | |
| Ибам, №72 | |
| Тетраэдр | |
| Опасности | |
| NFPA 704 (огненный алмаз) | |
| Родственные соединения | |
|
Другие анионы
|
диоксид кремния |
|
Другие катионы
|
сероуглерод дисульфид германия сульфид олова (IV) сульфид свинца (IV) |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
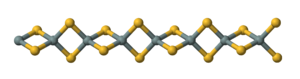
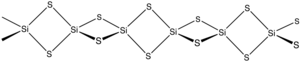
Дисульфид кремния представляет собой неорганическое соединение с формулой Si S 2 . Как и диоксид кремния , этот материал является полимерным , но он имеет одномерную структуру, сильно отличающуюся от обычных форм SiO 2 .
Синтез, структура и свойства
Материал образуется при нагревании кремния и серы или в результате реакции обмена между SiO 2 и Al 2 S 3 . Материал состоит из цепочек тетраэдров с общими ребрами Si (μ-S) 2 Si (μS) 2 и т. Д.
Подобно другим кремнийсодержащим соединениям серы (например, бис (триметилсилил) сульфиду ) SiS 2 легко гидролизуется с выделением H 2 S. Сообщается, что в жидком аммиаке образуется имид Si (NH) 2 и NH 4 SH, но в недавнем отчете есть идентифицировал кристаллический (NH 4 ) 2 [SiS 3 (NH 3 )] · 2NH 3 как продукт, который содержит тетраэдрический тиосиликатный анион SiS 3 (NH 3 ).
Реакция с этанолом дает тетраэтилортосиликат алкоксида и H 2 S. С объемистым трет-бутанолом алкоголиз дает трис (трет-бутокси) силантиол :
- 3 (CH 3 ) 3 COH + SiS 2 → [(CH 3 ) 3 CO] 3 SiSH + H 2 S
Реакция с сульфидом натрия , сульфида магния и алюминия сульфида дают thiosilicates .
Утверждается, что SiS 2 встречается в некоторых межзвездных объектах.
использованная литература

