Диоксид селена - Selenium dioxide

|
|
|
|

|
|
| Имена | |
|---|---|
| Другие имена
Оксид селена (IV)
Селеновый ангидрид |
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.028.358 |
|
PubChem CID
|
|
| Номер RTECS | |
| UNII | |
| Номер ООН | 3283 |
|
Панель управления CompTox ( EPA )
|
|
|
|
|
|
| Характеристики | |
| SeO 2 | |
| Молярная масса | 110,96 г / моль |
| Внешность | Белые кристаллы, слегка розовеют со следами разложения |
| Запах | гнилой редис |
| Плотность | 3,954 г / см 3 , твердый |
| Температура плавления | 340 ° C (644 ° F, 613 K) (герметичная трубка) |
| Точка кипения | 350 ° C (662 ° F, 623 K) субл. |
| 38,4 г / 100 мл (20 ° C) 39,5 г / 100 мл (25 ° C) 82,5 г / 100 мл (65 ° C) |
|
| Растворимость | растворим в бензоле |
| Растворимость в этаноле | 6,7 г / 100 мл (15 ° С) |
| Растворимость в ацетоне | 4,4 г / 100 мл (15 ° С) |
| Растворимость в уксусной кислоте | 1,11 г / 100 мл (14 ° С) |
| Растворимость в метаноле | 10,16 г / 100 мл (12 ° С) |
| Давление газа | 1,65 кПа (70 ° C) |
| Кислотность (p K a ) | 2,62; 8,32 |
| −27,2 · 10 −6 см 3 / моль | |
|
Показатель преломления ( n D )
|
> 1,76 |
| Структура | |
| см текст | |
| тригональный (Se) | |
| Опасности | |
| Паспорт безопасности | ICSC 0946 |
|
Классификация ЕС (DSD) (устарела)
|
Токсично ( T ) Опасно для окружающей среды ( N ) |
| R-фразы (устаревшие) | R23 / 25 , R33 , R50 / 53 |
| S-фразы (устаревшие) | (S1 / 2) , S20 / 21 , S28 , S45 , S60 , S61 |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | Негорючий |
| Смертельная доза или концентрация (LD, LC): | |
|
LC Lo ( самый низкий опубликованный )
|
5890 мг / м 3 (кролик, 20 мин) 6590 мг / м 3 (коза, 10 мин) 6590 мг / м 3 (овца, 10 мин) |
| Родственные соединения | |
|
Другие анионы
|
Дисульфид селена |
|
Другие катионы
|
Диоксид серы Диоксид теллура |
| Триоксид селена | |
|
Родственные соединения
|
Селеновая кислота |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
Диоксид селена - это химическое соединение с формулой SeO 2 . Это бесцветное твердое вещество - одно из наиболее часто встречающихся соединений селена .
Характеристики
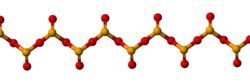
Твердый SeO 2 - это одномерный полимер , цепочка которого состоит из чередующихся атомов селена и кислорода . Каждый атом Se имеет пирамидальную форму и несет концевую оксидную группу. Длина мостиковой связи Se-O составляет 179 пм, а конечное расстояние Se-O составляет 162 пм. Относительная стереохимия у Se чередуется вдоль полимерной цепи ( синдиотактическая ). В газовой фазе диоксид селена присутствует в виде димеров и других олигомерных частиц, при более высоких температурах он является мономерным. Мономерная форма имеет изогнутую структуру, очень похожую на структуру диоксида серы, с длиной связи 161 мкм. Димерная форма была выделена в низкотемпературной матрице аргона, и колебательные спектры показывают, что она имеет форму центросимметричного кресла. Растворение SeO 2 в оксидихлориде селена дает тример [Se (O) O] 3 . Мономерный SeO 2 представляет собой полярную молекулу с дипольным моментом 2,62 D, направленным от середины двух атомов кислорода к атому селена.
Твердое вещество легко возгоняется. При очень низких концентрациях пар имеет отвратительный запах, напоминающий разложившийся хрен. При более высоких концентрациях пар имеет запах, напоминающий соус хрена, и может обжечь нос и горло при вдыхании. В то время как SO 2 имеет тенденцию быть молекулярным, а SeO 2 представляет собой одномерную цепь, TeO 2 представляет собой сшитый полимер.
SeO 2 считается кислым оксидом : он растворяется в воде с образованием селеновой кислоты . Часто термины селеновая кислота и диоксид селена используются как взаимозаменяемые. Он реагирует с основанием с образованием солей селенита, содержащих SeO 2-
3 анион. Например, реакция с гидроксидом натрия дает селенит натрия :
- SeO 2 + 2 NaOH → Na 2 SeO 3 + H 2 O
Подготовка
Диоксид селена получают путем окисления селена путем сжигания на воздухе или путем реакции с азотной кислотой или перекисью водорода , но, возможно, наиболее удобным способом получения является дегидратация селеновой кислоты .
- 2 Н 2 О 2 + Se → SeO 2 + 2 Н 2 О
- 3 Se + 4 HNO 3 + H 2 O → 3 H 2 SeO 3 + 4 NO
- H 2 SeO 3 ⇌ SeO 2 + H 2 O
Вхождение
Естественная форма диоксида селена, даунейит, является очень редким минералом. Он встречается только на очень немногих горящих отвалах угля.
Использует
Органический синтез
SeO 2 - важный реагент в органическом синтезе . Окисление паральдегида (тример ацетальдегида) SeO 2 дает глиоксаль, а окисление циклогексанона дает циклогексан-1,2-дион. Исходный селен восстанавливается до селен и выпадает в осадок в виде красного аморфного твердого вещества, которое можно легко отфильтровать. Этот тип реакции называется окислением Райли . Он также известен как реагент для «аллильного» окисления, реакции, которая влечет за собой следующее превращение
В более общем виде это можно описать как;
- R 2 C = CR'-CHR " 2 + [O] → R 2 C = CR'-C (OH) R" 2
где R, R ', R "могут быть алкильными или арильными заместителями.
Как краситель
Двуокись селена придает стеклу красный цвет . Он используется в небольших количествах, чтобы нейтрализовать цвет из-за примесей железа и, таким образом, создать (по-видимому) бесцветное стекло. В больших количествах дает темно-рубиново-красный цвет.
Диоксид селена является активным ингредиентом некоторых растворов для воронения .
Он также использовался в качестве тонера при проявке фотографий .
Безопасность
Селен является важным элементом , но прием более 5 мг в день приводит к неспецифическим симптомам .


