Пирофосфорная кислота - Pyrophosphoric acid

|
|
|
|
| Имена | |
|---|---|
|
Имена ИЮПАК
Дифосфорная кислота
μ-оксидо-бис (дигидроксидооксидофосфор) |
|
| Другие имена
Дифосфорная кислота
|
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard |
100.017.795 |
|
PubChem CID
|
|
| UNII | |
|
Панель управления CompTox ( EPA )
|
|
|
|
|
|
| Характеристики | |
| H 4 P 2 O 7 | |
| Молярная масса | 177,97 г / моль |
| Температура плавления | 71,5 ° С (160,7 ° F, 344,6 К) |
| Чрезвычайно растворим | |
| Растворимость | Хорошо растворим в спирте , эфире |
| Основание конъюгата | Пирофосфат |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
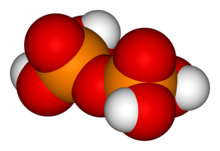
Пирофосфорная кислота , также известная как дифосфорная кислота , представляет собой неорганическое соединение с формулой H 4 P 2 O 7 или, более описательно, [(HO) 2 P (O)] 2 O. Бесцветное и без запаха, оно растворимо в воде , диэтиловый эфир и этиловый спирт . Безводная кислота кристаллизуется в виде двух полиморфов , которые плавятся при 54,3 ° C и 71,5 ° C. Соединение не особенно полезно, за исключением того, что оно является компонентом полифосфорной кислоты и сопряженной кислоты пирофосфат-аниона. Анионы , соли и сложные эфиры пирофосфорной кислоты называются пирофосфатами .
Подготовка
Лучше всего его приготовить ионным обменом из пирофосфата натрия или обработкой пирофосфата свинца сероводородом . Его не получают путем обезвоживания фосфорной кислоты. Вместо этого пирофосфорная кислота производится только как один из продуктов.
Реакции
В расплавленном состоянии пирофосфорная кислота быстро образует равновесную смесь фосфорной кислоты, пирофосфорной кислоты и полифосфорных кислот. Весовой процент пирофосфорной кислоты составляет около 40%, и ее трудно перекристаллизовать из расплава. В водном растворе пирофосфорная кислота, как и все полифосфорные кислоты, гидролизуется и в конечном итоге устанавливается равновесие между фосфорной кислотой, пирофосфорной кислотой и полифосфорными кислотами.
- H 4 P 2 O 7 + H 2 O ⇌ 2 H 3 PO 4
Пирофосфорная кислота - неорганическая кислота средней силы .
Безопасность
Хотя пирофоспоровая кислота вызывает коррозию, в остальном она токсична.
История
Название пирофосфорная кислота было дано «мистером Кларком из Глазго» в 1827 году, которому приписывают ее открытие после нагревания до красного каления соли фосфата натрия. Было обнаружено, что фосфорная кислота при нагревании до красного каления образует пирофосфорную кислоту, которая легко превращается в фосфорную кислоту горячей водой.
Смотрите также
- Пирофосфат натрия
- Болезнь отложения дигидрата пирофосфата кальция
- Диметилаллил пирофосфат
- ADP
- АТФ
- Орто кислоты
- трифосфорная кислота
Рекомендации
- ^ Corbridge, D. (1995). «Глава 3: Фосфаты». Исследования по неорганической химии vol. 20 . Elsevier Science BV, стр. 169–305. DOI : 10.1016 / B978-0-444-89307-9.50008-8 . ISBN 0-444-89307-5 .
- ^ Паспорт безопасности материала: Пирофосфорная кислота MSDS www.sciencelab.com
- ^ Бек, Льюис Калеб (1834). Руководство по химии: краткое изложение современного состояния науки с многочисленными ссылками на более обширные трактаты, оригинальные статьи и т . Д. EW&C Скиннер. п. 160 . Проверено 30 января 2015 года .
