Платина (IV) хлорид - Platinum(IV) chloride

|
|
| Имена | |
|---|---|
|
Название ИЮПАК
Тетрахлорид платины
|
|
| Другие названия
Платина (IV) хлорид
|
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.033.300 |
|
PubChem CID
|
|
| UNII | |
|
Панель управления CompTox ( EPA )
|
|
|
|
|
|
| Характеристики | |
| PtCl 4 | |
| Молярная масса | 336,89 г / моль |
| Появление | коричнево-красный порошок |
| Плотность | 4,303 г / см 3 (безводный) 2,43 г / см 3 (пентагидрат) |
| Температура плавления | 370 ° С (698 ° F, 643 К) разлагается |
| Точка кипения | разлагается |
| 58,7 г / 100 мл (безводный) хорошо растворим (пентагидрат) |
|
| Растворимость |
безводный растворим в ацетоне мало растворим в этаноле нерастворим в эфире пентагидрат растворим в спирте , эфире |
| −93,0 · 10 −6 см 3 / моль | |
| Состав | |
| Квадратный планарный | |
| Опасности | |
|
Классификация ЕС (DSD) (устаревшая)
|
нет в списке |
| Смертельная доза или концентрация (LD, LC): | |
|
LD 50 ( средняя доза )
|
276 мг / кг (крыса, перорально) |
| Родственные соединения | |
|
Другие анионы
|
Бромид платины (IV) Фторид платины (IV) Сульфид платины (IV) |
|
Другие катионы
|
Хлорид иридия (IV) |
|
Родственные соединения
|
Хлорид платины (II ) Фторид платины (VI) |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
| Ссылки на инфобоксы | |
Платины (IV) , хлорид представляет собой неорганическое соединение из платины и хлора с эмпирической формулой PtCl 4 . Это коричневое твердое вещество содержит платину в степени окисления 4+.
Состав
Типичные для Pt (IV) металлические центры имеют октаэдрическую координационную геометрию {PtCl 6 }. Эта геометрия достигается за счет образования полимера, в котором половина хлоридных лигандов соединяется между платиновыми центрами. Из-за своей полимерной структуры PtCl 4 растворяется только после разрушения лигандов, связывающих хлоридный мостик . Таким образом, добавление HCl дает H 2 PtCl 6 . Основание Льюиса аддукты из Pt (IV) типа цис-PtCl 4 L 2 известны, но большинство из них получают путем окисления (II) производных Pt.
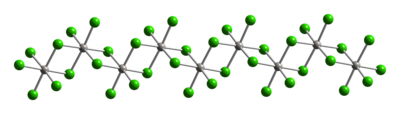
|
| Часть цепочки (PtCl 4 ) ∞ из кристаллической структуры хлорида платины (IV) |
Образование и реакции
PtCl 4 в основном встречается при обращении с платинохлористоводородной кислотой , полученной растворением металлической Pt в царской водке . Нагревание H 2 PtCl 6 дает PtCl 4 :
- H 2 PtCl 6 → PtCl 4 + 2 HCl
Если удалить избыток кислот, PtCl 4 кристаллизуется из водных растворов в виде больших красных кристаллов пентагидрата PtCl 4 · 5 (H 2 O), которые могут быть обезвожены нагреванием примерно до 300 ° C в токе сухого хлора. Пентагидрат стабилен и используется как коммерческая форма PtCl 4 .
Обработка PtCl 4 водным основанием дает ион [Pt (OH) 6 ] 2– . При использовании метиловых реагентов Гриньяра с последующим частичным гидролизом PtCl 4 превращается в кубовидный кластер [Pt (CH 3 ) 3 (OH)] 4 . При нагревании PtCl 4 эволюционирует хлора с получением PtCl 2 :
- PtCl 4 → PtCl 2 + Cl 2
Также известны более тяжелые галогениды PtBr 4 и PtI 4 .
Рекомендации
- Хлопок, С. А. Химия драгоценных металлов , Чепмен и Холл (Лондон): 1997. ISBN 0-7514-0413-6 .
