Спектроскопия ядерного магнитного резонанса углеводов - Nuclear magnetic resonance spectroscopy of carbohydrates
Спектроскопия ЯМР углеводов - это применение спектроскопии ядерного магнитного резонанса (ЯМР) для структурного и конформационного анализа углеводов . Этот метод позволяет ученым выяснить структуру моносахаридов , олигосахаридов , полисахаридов , гликоконъюгатов и других производных углеводов из синтетических и природных источников. К структурным свойствам, которые можно определить с помощью ЯМР, относятся первичная структура (включая стереохимию), конформацию сахарида, стехиометрию заместителей и соотношение отдельных сахаридов в смеси. Современные приборы ЯМР с высоким полем, используемые для образцов углеводов, обычно с частотой 500 МГц или выше, могут проводить серию одномерных, двухмерных и трехмерных экспериментов для определения структуры углеводных соединений.
Наблюдаемые углеводным ЯМР
Химический сдвиг
Общие диапазоны химического сдвига ядер в углеводных остатках:
- Типичные химические сдвиги 1 H ЯМР протонов углеводного кольца составляют 3–6 м.д. (4,5–5,5 м.д. для аномерных протонов).
- Типичные химические сдвиги атомов углерода в кольце углеводного цикла 13 C ЯМР составляют 60–110 м.д.
В случае простых моно- и олигосахаридных молекул все сигналы протонов обычно отделены друг от друга (обычно на ЯМР на 500 МГц или лучше) и могут быть отнесены только с использованием 1D ЯМР-спектра. Однако более крупные молекулы демонстрируют значительное перекрытие сигналов протонов, особенно в неаномерной области (3-4 ppm). ЯМР углерода-13 преодолевает этот недостаток за счет более широкого диапазона химических сдвигов и специальных методов, позволяющих блокировать спиновое взаимодействие углерод-протон, тем самым делая все сигналы углерода высокими и узкими синглетами, отличимыми друг от друга.
Типичные диапазоны химических сдвигов конкретных углеводных углеродов в незамещенных моносахаридах:
- Аномерные атомы углерода: 90-100 частей на миллион
- Углероды сахарного кольца, несущие гидроксильную функцию: 68-77
- Сахарный углерод открытой формы, несущий гидроксильную функцию: 71-75
- Углероды сахарного кольца с аминогруппой: 50-56
- Экзоциклические гидроксиметильные группы: 60-64
- Экзоциклические карбоксильные группы: 172-176
- Дезоксигенированные сахарные кольцевые атомы углерода: 31-40
- Углерод при замыкании пиранозного кольца: 71-73 (α-аномеры), 74-76 (β-аномеры)
- Углерод при замыкании фуранозного кольца: 80-83 (α-аномеры), 83-86 (β-аномеры)
Константы связи
Константы прямого взаимодействия углерод-протон используются для изучения аномерной конфигурации сахара. Константы протон-протонного взаимодействия Vicinal используются для изучения стереоориентации протонов относительно других протонов в сахарном кольце, таким образом идентифицируя моносахарид. Константы вицинального гетероядерного взаимодействия HCOC используются для изучения торсионных углов вдоль гликозидной связи между сахарами или вдоль экзоциклических фрагментов, таким образом выявляя молекулярную конформацию.
Сахарные кольца - относительно жесткие молекулярные фрагменты, поэтому характерны вицинальные протон-протонные взаимодействия:
- Экваториально-осевой: 1–4 Гц
- Экваториальный к экваториальному: 0–2 Гц
- Аксиально-осевой неаномерный: 9–11 Гц
- Аксиально-аксиальный аномерный: 7–9 Гц
- Аксиальный к экзоциклическому гидроксиметилу: 5 Гц, 2 Гц
- Близнецы между гидроксиметильными протонами: 12 Гц
Ядерные эффекты Оверхаузера (НЯ)
NOE чувствительны к межатомным расстояниям, что позволяет использовать их в качестве конформационного зонда или доказательства образования гликозидной связи. Обычной практикой является сравнение рассчитанных с экспериментальными протон-протонными NOE в олигосахаридах для подтверждения теоретической конформационной карты. Расчет NOE подразумевает оптимизацию молекулярной геометрии.
Другие наблюдаемые ЯМР
Сообщалось о релаксации, скорости ядерной релаксации, форме линии и других параметрах, которые могут быть полезны при структурных исследованиях углеводов.
Выяснение структуры углеводов методом ЯМР-спектроскопии.
Структурные параметры углеводов
Ниже приводится список структурных особенностей, которые могут быть выяснены с помощью ЯМР:
- Химическая структура каждого углеводного остатка в молекуле, включая
- размер углеродного скелета и тип сахара (альдоза / кетоза)
- размер цикла (пираноза / фураноза / линейный)
- стерео конфигурация всех атомов углерода (идентификация моносахаридов)
- стерео конфигурация аномерного углерода (α / β)
- абсолютная конфигурация (D / L)
- расположение амино-, карбокси-, дезокси- и других функций
- Химическая структура неуглеводных остатков в молекуле (аминокислот, жирных кислот, спиртов, органических агликонов и т. Д.)
- Положения замещения в остатках
- Последовательность остатков
- Стехиометрия концевых остатков и боковых цепей
- Расположение фосфатных и сульфатных диэфирных связей
- Степень полимеризации и расположение рамки (для полисахаридов)
ЯМР-спектроскопия по сравнению с другими методами
Широко известные методы структурного исследования, такие как масс-спектрометрия и рентгеноструктурный анализ, лишь ограниченно применимы к углеводам. Такие структурные исследования, как определение последовательности или идентификация новых моносахаридов, наиболее выигрывают от ЯМР-спектроскопии. Абсолютную конфигурацию и степень полимеризации не всегда можно определить с помощью только ЯМР, поэтому процесс структурного выяснения может потребовать дополнительных методов. Хотя мономерный состав может быть определен с помощью ЯМР, хроматографические и масс-спектроскопические методы иногда легче предоставляют эту информацию. Остальные структурные особенности, перечисленные выше, могут быть определены исключительно методами ЯМР-спектроскопии. Ограничение структурных исследований ЯМР углеводов заключается в том, что выяснение структуры трудно автоматизировать и требует, чтобы специалист-человек получил структуру из спектров ЯМР.
Применение различных методов ЯМР к углеводам
Сложные гликаны обладают множеством перекрывающихся сигналов, особенно в протонном спектре. Следовательно, для назначения сигналов выгодно использовать двумерные эксперименты. В таблице и на рисунках ниже перечислены наиболее распространенные методы ЯМР, используемые в исследованиях углеводов.
| ЯМР эксперимент | Описание | Полученная информация |
|---|---|---|
| 1 ч 1Д | 1D протонный спектр | измерение муфт, общая информация, идентификация остатков, основа для присвоения углеродного спектра |
| 13 C BB | Разделенный протонами одномерный спектр углерода-13 | подробная информация, идентификация остатков, положения замещения |
| 31 P BB, 15 N BB | Протонно-развязанные одномерные гетероядерные спектры | Дополнительная информация |
| КВАРТИРА, 13 C ОТДЕЛЕНИЕ | прикрепленный протонный тест, управляемая усиленная передача поляризации (отредактированный 1D спектр углерода-13) | Назначение СН 2 групп |
| 13 C закрытый, 31 P закрытый | Протонно-связанные одномерные спектры углерода-13 и гетероядер | измерение гетероядерных связей, выяснение аномерной конфигурации, конформационные исследования |
| 1 H, 1 H J-разрешено | 2D-график ЯМР, показывающий J-соединения во втором измерении | точные значения J-связи и химического сдвига для переполненных спектральных областей |
| 1 ЧАСНАЯ ДОЗИРОВКА | График 2D ЯМР со спектрами протонов в зависимости от коэффициента молекулярной диффузии | измерение коэффициента диффузии, оценка размера / веса молекул, спектральное разделение различных молекул в смеси |
| 1 час, 1 час уютный | Корреляция спина протона | отнесение спектра протонов с использованием вицинальных связей |
| УЮТНЫЙ RCT, УЮТНЫЙ RCT2 | Корреляция спина протона с одно- или двухступенчатой ретрансляционной передачей когерентности | отнесение протонного спектра, когда сигналы соседних вицинальных протонов перекрываются |
| DQF УЮТНЫЙ | Спиновая корреляция протонов с двойной квантовой фильтрацией | Величины J-связи и количество протонов, участвующих в J-взаимодействии |
| 1 H HD диф. | Селективная дифференциальная гоморазвязка | анализ формы линий перекрывающихся сигналов протонов |
| ТОКСИ (ХОХАХА) | Полная корреляция всех протонов в спиновой системе | выделение спиновых систем остатков |
| 1D TOCSY | TOCSY одиночного сигнала | извлечение из спиновой системы определенного остатка |
| НЕСИ, РОЗИ | Корреляция гомонуклеарного ядерного эффекта Оверхаузера (в космосе) | выявление пространственно проксимальных пар протонов, определение последовательности остатков, определение усредненной конформации |
| 1 H NOE diff | Селективное дифференциальное измерение NOE | исследования протонных пространственных контактов |
| 1 H, 13 C HSQC | Гетероядерная одноквантовая когерентность, прямая корреляция между протонами и углеродом. | присвоение спектра углерода |
| 1 H, 31 P HSQC | Гетероядерная одноквантовая когерентность, спиновая корреляция протон-фосфор | локализация остатков фосфорной кислоты в фосфогликанах |
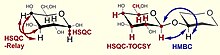
| 1 H, 13 C HMBC | Гетероядерная корреляция кратных связей, вицинальная корреляция спина протона и углерода | определение последовательности остатков, паттерна ацетилирования / амидирования, подтверждение позиций замещения |
| 1 H, X 1D HMBC | HMBC для одиночного сигнала | назначение протона вокруг определенного углерода или гетероатома |
| 1 H, 13 C реле HSQC | Неявная корреляция углерод-углерод через вицинальные связи присоединенных протонов | отнесение соседних атомов углерода |
| 1 H, 13 C HSQC-TOCSY | Корреляция протонов со всеми атомами углерода в спиновой системе, и наоборот | определение C5 с использованием H6 и решение аналогичных задач, разделение спектра углерода на субспектры остатков |
| 1 H, X 1D NOE | Гетероядерное измерение NOE | гетероядерные пространственные контакты, конформации |
Схема исследования
ЯМР-спектроскопическое исследование включает следующие этапы:
- Экстракция углеводного материала (для природных гликанов)
- Химическое удаление фрагментов, маскирующих закономерность (для полимеров)
- Разделение и очистка углеводного материала (для 2D-ЯМР-экспериментов рекомендуется 10 мг или более)
- Подготовка проб (обычно в D2O)
- Получение одномерных спектров
- Планирование, сбор и обработка других экспериментов ЯМР (обычно требуется от 5 до 20 часов)
- Отнесение и интерпретация спектров (см. Примерный рисунок)
- Если структурная проблема не может быть решена: химическая модификация / разложение и ЯМР-анализ продуктов.
- Получение спектров нативного (немаскированного) соединения и их интерпретация на основе модифицированной структуры.
- Представление результатов
Базы данных и инструменты для ЯМР углеводов
Были созданы многочисленные базы данных по химическому сдвигу и соответствующие службы, чтобы помочь в структурном объяснении и экспертном анализе их ЯМР-спектров. Из них несколько инструментов информатики посвящены исключительно углеводам:
- GlycoSCIENCES.de
- более 2000 спектров ЯМР гликанов млекопитающих
- поиск структуры по сигналам ЯМР и наоборот
-
CSDB (база данных структуры углеводов) содержит:
- более 4000 спектров ЯМР гликанов бактерий, растений и грибов,
- поиск структуры по сигналам ЯМР и наоборот
- программа моделирования эмпирических спектров, оптимизированная для углеводов,
- статистическая оценка химического сдвига на основе алгоритма HOSE, оптимизированного для углеводов,
- инструмент построения структуры и ранжирования на основе ЯМР.
- КАСПЕР (компьютерная оценка спектра обычных полисахаридов). содержит:
- база данных химического сдвига,
- программа моделирования эмпирических спектров, оптимизированная для углеводов,
- онлайн-интерфейс.
- инструмент сопоставления структуры. Химические сдвиги C и H протонов и углерода можно использовать для доступа к структурной информации.
Моделирование наблюдаемых ЯМР

Было рассмотрено несколько подходов к моделированию наблюдаемых ЯМР углеводов. Они включают:
- Подходы к универсальным статистическим базам данных (ACDLabs, Modgraph и т. Д.)
- Использование нейронных сетей для уточнения прогнозов
- Методы, основанные на регрессии
- ЗАРЯЖАТЬ
- Эмпирические схемы, оптимизированные для углеводов (CSDB / BIOPSEL, CASPER).
- Комбинированный расчет молекулярной механики / динамической геометрии и квантово-механическое моделирование / итерация наблюдаемых ЯМР (программное обеспечение PERCH NMR)
- Подходы ONIOM (оптимизация разных частей молекулы с разной точностью)
- Расчеты ab initio .
Растущая вычислительная мощность позволяет использовать тщательные квантово-механические расчеты на высоких теоретических уровнях и большие базовые наборы для уточнения молекулярной геометрии углеводов и последующего предсказания наблюдаемых ЯМР с использованием GIAO и других методов с учетом или без учета эффекта растворителя. Среди комбинаций теоретического уровня и базисного набора, которые, как сообщается, достаточно для предсказаний ЯМР, были B3LYP / 6-311G ++ (2d, 2p) и PBE / PBE (см. Обзор). Для сахаридов было показано, что оптимизированные для углеводов эмпирические схемы обеспечивают значительно лучшую точность (0,0-0,5 ppm на резонанс 13 C), чем квантово-химические методы (более 2,0 ppm на резонанс), признанные лучшими для моделирования ЯМР, и работают в тысячи раз быстрее. Однако эти методы могут предсказывать только химические сдвиги и плохо подходят для неуглеводных частей молекул. В качестве репрезентативного примера см. Рисунок справа.
Смотрите также
- Методы 1D и 2D ЯМР спектроскопии в структурных исследованиях природных гликополимеров (лекция)
- Базы данных по углеводам за последнее десятилетие (лекция; включает данные моделирования ЯМР)
- Углеводов
- Гликан
- Ядерный магнитный резонанс
- Спектроскопия ядерно-магнитного резонанса нуклеиновых кислот
- Спектроскопия белков ядерного магнитного резонанса
- ЯМР спектроскопия
- Ядерный эффект Оверхаузера
Рекомендации
дальнейшее чтение
- Д. Ловицки; А. Чарни; Я. Млынарский (2013). Ядерный магнитный резонанс: ЯМР углеводов . Королевское химическое общество . п. 383. ISBN. 978-1-84973-577-3 .
Внешние ссылки
-
 СМИ, связанные со спектроскопией ядерного магнитного резонанса углеводов на Викискладе?
СМИ, связанные со спектроскопией ядерного магнитного резонанса углеводов на Викискладе?