Мутаза метилмалонил-КоА - Methylmalonyl-CoA mutase
| метилмалонил-КоА мутаза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| ЕС нет. | 5.4.99.2 | ||||||||
| № CAS | 9023-90-9 | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| BRENDA | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| Структуры PDB | RCSB PDB PDBe PDBsum | ||||||||
| Генная онтология | Amigo / QuickGO | ||||||||
| |||||||||
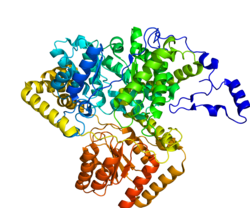
Метилмалонил-КоА-мутаза (MCM), митохондриальная , также известная как метилмалонил-КоА-изомераза , представляет собой белок, который у человека кодируется геном MUT . Этот витамин B 12 -зависимый фермент катализирует изомеризацию метилмалонил-КоА в сукцинил-КоА у людей. Мутации в гене MUT могут приводить к различным типам метилмалоновой ацидурии .
MCM был впервые обнаружен в печени крыс и почках овцы в 1955 году. В латентной форме он состоит из 750 аминокислот . При входе в митохондрии лидерная последовательность митохондрий из 32 аминокислот на N-конце белка расщепляется, образуя полностью процессированный мономер. Затем мономеры объединяются в гомодимеры и связывают AdoCbl (по одному для каждого активного центра мономера) с образованием конечной активной формы холофермента .
Состав
Ген
Ген MUT расположен на хромосоме 6p12.3 и состоит из 13 экзонов , занимающих более 35 килобайт.
Протеин
Зрелый фермент представляет собой гомодимер с N-концевым доменом связывания CoA и C-концевым доменом связывания кобаламина.
Функция
Мутаза метилмалонил-КоА экспрессируется в высоких концентрациях в почках , в промежуточных концентрациях в сердце , яичниках , головном мозге , мышцах и печени и в низких концентрациях в селезенке . Фермент можно найти повсюду в центральной нервной системе (ЦНС). MCM находится в митохондриях, где ряд веществ, включая аминокислоты с разветвленной цепью изолейцин и валин , а также метионин , треонин , тимин и жирные кислоты с нечетной цепью , метаболизируются через метилмалонат полуальдегид (MMlSA) или пропионил-CoA. (Pr-CoA) в обычное соединение - метилмалонил-CoA (MMl-CoA). MCM катализирует обратимую изомеризацию l-метилмалонил-КоА в сукцинил-КоА, требуя в качестве кофактора кобаламина (витамин B12) в форме аденозилкобаламина (AdoCbl). В качестве важного этапа катаболизма пропионата эта реакция необходима для разложения жирных кислот с нечетной цепью , аминокислот валина , изолейцина , метионина и треонина , а также холестерина , в результате чего метаболиты распада этих аминокислот превращаются в трикарбоновую кислоту. цикл .
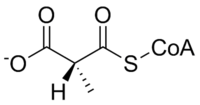
Мутаза метилмалонил-КоА катализирует следующую реакцию:
| L-метилмалонил-КоА | метилмалонил-КоА мутаза | Сукцинил-КоА | |
|

|
||

|
|||
| метилмалонил-КоА мутаза | |||
Субстрат мутазы метилмалонил-КоА, метилмалонил-КоА , в основном происходит из пропионил-КоА , вещества, образующегося в результате катаболизма и переваривания изолейцина , валина , треонина , метионина , тимина , холестерина или жирных кислот с нечетной цепью. Продукт фермента, сукцинил-КоА , является ключевой молекулой цикла трикарбоновых кислот .
Клиническое значение
Дефицит этого фермента является причиной наследственного нарушения метаболизма, дефицита метилмалонил-КоА-мутазы , который является одной из причин метилмалоновой ацидемии (также называемой метилмалоновой ацидурией или ММА). ММА - аутосомно-рецессивная наследственная врожденная ошибка метаболизма, характеризующаяся повторяющимися эпизодами рвоты, летаргии, глубокого кетоацидоза , гипераммониемии и панцитопении в младенчестве и может вызвать преждевременную смерть. Осложнения включают кардиомиопатию , метаболический инсульт , панкреатит и прогрессирующую почечную недостаточность .
Либо мутации гена MUT (кодирует мутазу метилмалонил-КоА), либо MMAA (кодирует белок-шаперон мутазы метилмалонил-КоА, белок MMAA ) могут привести к метилмалонилацидемии. Мутации в MUT можно разделить на MUT 0 (не проявляет активности даже в присутствии избытка AdoCbl) или MUT 1 (демонстрирует очень низкую активность в присутствии избытка AdoCbl). Более половины мутаций MUT являются миссенс-мутациями, в то время как бессмысленные мутации составляют значительную оставшуюся часть (примерно 14%).
Общие методы лечения ММА включают пересадку печени или пересадку печени и почек для борьбы с заболеванием почек метилмалоновой ацидемией. Однако пагубные неврологические эффекты могут продолжать беспокоить пациентов даже после успешной операции. Считается, что это связано с широким распространением мутазы метилмалонил-КоА в центральной нервной системе. Из-за потери функциональности фермента уровни субстрата накапливаются в ЦНС. Субстрат, L-метилмалонил-КоА, гидролизуется с образованием метилмалоната (метилмалоновой кислоты), нейротоксической дикарбоновой кислоты, которая из-за плохой транспортной способности дикарбоновой кислоты гематоэнцефалическим барьером эффективно задерживается в ЦНС, что приводит к неврологической истощенности. Для борьбы с этими эффектами не рекомендуются периоперационные антикатаболические режимы и отказ от диеты.
Мышиная модель доказала адекватный и точный способ изучения влияния ММЫ и потенциальных методы лечения.
Механизм
Механизм реакции MCM начинается с гомолитического расщепления связи C- Co (III) AdoB12, каждый из атомов C и Co приобретает по одному из электронов, образующих расщепленную электронную парную связь. Ион Co, следовательно, колеблется между состояниями окисления Co (III) и Co (II) [эти два состояния различимы спектроскопически: Co (III) красный и диамагнитный (нет неспаренных электронов), тогда как Co (II) желтый и парамагнитные (неспаренные электроны)]. Следовательно, роль кофермента B-12 в каталитическом процессе - роль обратимого генератора свободных радикалов . Связь C-Co (III) является слабой с энергией диссоциации = 109 кДж / моль и, по-видимому, дополнительно ослабляется из-за стерических взаимодействий с ферментом. Гомолитический реакция является необычным в биологии, как это имеет место наличие металла-углеродную связь.
Мутаза метилмалонил-КоА является членом подсемейства изомераз зависимых от аденозилкобаламина ферментов. Кроме того, он классифицируется как класс I, так как это фермент «DMB-off» / «His-on». Это относится к природе кофактора AdoCbl в активном центре метилмалонил-КоА. AdoCbl состоит из центрального кобальта -содержащий Коррина кольцо , верхний осевой лиганд (β-аксиального лиганда), и нижний аксиальный лиганд (α-аксиального лиганда). В мутазе метилмалонил-КоА β-аксиальный лиганд 5'-дезокси-5'-аденозин обратимо диссоциирует с образованием дезоксиаденозильного радикала . Α-Аксиальный лиганд 5,6-диметилбензимидазол (DMB) участвует в организации активного сайта, чтобы гистидин- 610 мог связываться с Co, вместо DMB (причина обозначения DMB-off / His-on. ). Связывание остатка гистидина-610 увеличивает скорость гомолитического β-аксиального лиганда - разрыва связи Co в 10–12 раз .

Другие важные остатки метилмалонил-КоА мутазы включают гистидин-244, который действует как обычная кислота рядом с субстратом и защищает радикальные частицы от побочных реакций с участием кислорода, глутамат- 370, водородная связь которого с 2'-ОН группой рибозы β-аксиального лиганда усиливает взаимодействие между радикалами β-аксиального лиганда и субстратом, а тирозин -89 стабилизирует реакционноспособные радикальные промежуточные соединения и объясняет стереоселективность фермента.
Процессирующий белок, белок MMAA , выполняет важную роль, способствуя загрузке и обмену кофакторов. Белок MMAA способствует ассоциации с апоферментом MCM и позволяет переносить кофактор AdoCbl к активному центру фермента. Более того, если связанный AdoCbl накапливает окислительное повреждение во время нормального функционирования, белок MMAA способствует обмену поврежденного кофактора на новый AdoCbl через GTP- зависимый путь.
Взаимодействия
использованная литература
дальнейшее чтение
- Ледли Ф. Д., Розенблатт Д. С. (1997). «Мутации в mut метилмалоновой ацидемии: клинические и ферментативные корреляции». Человеческая мутация . 9 (1): 1–6. DOI : 10.1002 / (SICI) 1098-1004 (1997) 9: 1 <1 :: AID-HUMU1> 3.0.CO; 2-E . PMID 8990001 .
- Людвиг ML, Мэтьюз RG (1997). «Взгляды на структуру B12-зависимых ферментов». Ежегодный обзор биохимии . 66 : 269–313. DOI : 10.1146 / annurev.biochem.66.1.269 . PMID 9242908 .
- Лубрано Р., Элли М., Росси М., Травассо Е., Рагги С., Барсотти П., Кардуччи С., Берлоко П. (август 2007 г.). «Трансплантация почки при метилмалоновой ацидемии: может ли это быть лучшим вариантом? Отчет о случае через 10 лет и обзор литературы». Детская нефрология . 22 (8): 1209–14. DOI : 10.1007 / s00467-007-0460-Z . PMID 17401587 . S2CID 24610554 .
- Френкель Е.П., Кухни RL (декабрь 1975 г.). «Внутриклеточная локализация печеночной пропионил-КоА карбоксилазы и метилмалонил-КоА мутазы у людей и нормальных крыс с дефицитом витамина В12». Британский журнал гематологии . 31 (4): 501–13. DOI : 10.1111 / j.1365-2141.1975.tb00885.x . PMID 24458 . S2CID 1232083 .
- Крейн А.М., Янсен Р., Эндрюс Е.Р., Ледли Ф. Д. (февраль 1992 г.). «Клонирование и экспрессия мутантной мутазы метилмалонил-кофермента А с измененным сродством к кобаламину, которая вызывает мут-метилмалоновую ацидурию» . Журнал клинических исследований . 89 (2): 385–91. DOI : 10.1172 / JCI115597 . PMC 442864 . PMID 1346616 .
- Крейн А.М., Мартин Л.С., Валле Д., Ф. Д. Ледли (май 1992 г.). «Фенотип заболевания у трех пациентов с идентичными мутациями метилмалонил-КоА мутазы». Генетика человека . 89 (3): 259–64. DOI : 10.1007 / BF00220536 . PMID 1351030 . S2CID 5624280 .
- Рафф М.Л., Крейн А.М., Янсен Р., Ледли Ф.Д., Розенблатт Д.С. (январь 1991 г.). «Генетическая характеристика мутации локуса MUT, различающей гетерогенность mut0 и mut-метилмалоновой ацидурии за счет межараллельной комплементации» . Журнал клинических исследований . 87 (1): 203–7. DOI : 10.1172 / JCI114972 . PMC 295026 . PMID 1670635 .
- Янсен Р., Ледли Ф. Д. (ноябрь 1990 г.). «Гетерозиготные мутации в локусе mut в фибробластах с mut0 метилмалоновой ацидемией, идентифицированные клонированием кДНК с помощью полимеразной цепной реакции» . Американский журнал генетики человека . 47 (5): 808–14. PMC 1683687 . PMID 1977311 .
- Nham SU, Wilkemeyer MF, Ledley FD (декабрь 1990 г.). «Структура локуса метилмалонил-КоА-мутазы (MUT) человека». Геномика . 8 (4): 710–6. DOI : 10.1016 / 0888-7543 (90) 90259-W . PMID 1980486 .
- Ledley FD, Lumetta M, Nguyen PN, Kolhouse JF, Allen RH (май 1988 г.). «Молекулярное клонирование мутазы L-метилмалонил-КоА: перенос генов и анализ линий мутных клеток» . Труды Национальной академии наук Соединенных Штатов Америки . 85 (10): 3518–21. Bibcode : 1988PNAS ... 85.3518L . DOI : 10.1073 / pnas.85.10.3518 . PMC 280243 . PMID 2453061 .
- Янсен Р., Калоусек Ф., Фентон В. А., Розенберг Л. Е., Ледли Ф. Д. (февраль 1989 г.). «Клонирование полноразмерной метилмалонил-КоА мутазы из библиотеки кДНК с использованием полимеразной цепной реакции». Геномика . 4 (2): 198–205. DOI : 10.1016 / 0888-7543 (89) 90300-5 . PMID 2567699 .
- Фентон В.А., Хак А.М., Краус Дж. П., Розенберг Л. Е. (март 1987 г.). «Иммунохимические исследования фибробластов пациентов с дефицитом апофермента метилмалонил-КоА мутазы: обнаружение мутации, препятствующей импорту митохондрий» . Труды Национальной академии наук Соединенных Штатов Америки . 84 (5): 1421–4. Bibcode : 1987PNAS ... 84.1421F . DOI : 10.1073 / pnas.84.5.1421 . PMC 304442 . PMID 2881300 .
- Zoghbi HY, O'Brien WE, Ledley FD (ноябрь 1988 г.). «Отношения сцепления мутазы метилмалонил-КоА человека с локусами HLA и D6S4 на хромосоме 6». Геномика . 3 (4): 396–8. DOI : 10.1016 / 0888-7543 (88) 90135-8 . PMID 2907507 .
- Колхаус Дж. Ф., Атли С., Аллен Р. Х. (апрель 1980 г.). «Выделение и характеристика мутазы метилмалонил-КоА из плаценты человека» . Журнал биологической химии . 255 (7): 2708–12. DOI : 10.1016 / S0021-9258 (19) 85795-2 . PMID 6102092 .
- Фентон В.А., Хак А.М., Уиллард Х.Ф., Гертлер А., Розенберг Л.Е. (апрель 1982 г.). «Очистка и свойства мутазы метилмалонил-кофермента А из печени человека». Архивы биохимии и биофизики . 214 (2): 815–23. DOI : 10.1016 / 0003-9861 (82) 90088-1 . PMID 6124211 .
- Куреши А.А., Крейн А.М., Матиашук Н.В., Резвани И., Ледли Ф.Д., Розенблатт Д.С. (апрель 1994 г.). «Клонирование и экспрессия мутаций, демонстрирующих внутригенную комплементацию при mut0 метилмалоновой ацидурии» . Журнал клинических исследований . 93 (4): 1812–9. DOI : 10.1172 / JCI117166 . PMC 294249 . PMID 7909321 .
- Крейн AM, Ledley FD (июль 1994 г.). «Кластеризация мутаций в мутазе метилмалонил-КоА, связанных с мут-метилмалоновой ацидемией» . Американский журнал генетики человека . 55 (1): 42–50. PMC 1918235 . PMID 7912889 .
- Джаната Дж., Когекар Н., Фентон В.А. (сентябрь 1997 г.). «Экспрессия и кинетическая характеристика мутазы метилмалонил-КоА у пациентов с мут-фенотипом: доказательства естественной межараллельной комплементации» . Молекулярная генетика человека . 6 (9): 1457–64. DOI : 10.1093 / HMG / 6.9.1457 . PMID 9285782 .
внешние ссылки
- GeneReviews / NIH / NCBI / UW запись о метилмалоновой ацидемии
- Метилмалонил-КоА + мутаза в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH)