Оксид лития - Lithium oxide

|
|
|
|
 |
|

|
|
| Имена | |
|---|---|
|
Название ИЮПАК
Оксид лития
|
|
| Другие названия
Лития, Кикерит
|
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.031.823 |
|
PubChem CID
|
|
| Номер RTECS | |
| UNII | |
|
Панель управления CompTox ( EPA )
|
|
|
|
|
|
| Характеристики | |
|
Ли 2О |
|
| Молярная масса | 29,88 г / моль |
| Появление | белое твердое вещество |
| Плотность | 2,013 г / см 3 |
| Температура плавления | 1438 ° С (2620 ° F, 1711 К) |
| Точка кипения | 2600 ° С (4710 ° F, 2870 К) |
| бурно реагирует с образованием LiOH | |
| журнал P | 9,23 |
|
Показатель преломления ( n D )
|
1,644 |
| Состав | |
| Антифторит (кубический), cF12 | |
| Фм 3 м, №225 | |
| Тетраэдр (Li + ); кубический (O 2- ) | |
| Термохимия | |
|
Теплоемкость ( C )
|
1,8 · 105 Дж / г К или 54,1 Дж / моль К |
|
Стандартная мольная
энтропия ( S |
37,89 Дж / моль К |
|
Std энтальпия
формации (Δ F H ⦵ 298 ) |
-20,01 кДж / г или -595,8 кДж / моль |
|
Свободная энергия Гиббса (Δ f G )
|
-562,1 кДж / моль |
| Опасности | |
| Основные опасности | Едкий, бурно реагирует с водой |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | Не воспламеняется |
| Родственные соединения | |
|
Другие анионы
|
Сульфид лития |
|
Другие катионы
|
Оксид натрия Оксид калия Оксид рубидия Оксид цезия |
|
Перекись лития Супероксид лития |
|
|
Родственные соединения
|
Гидроксид лития |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
Оксид лития ( Li
2O ) или лития - неорганическое химическое соединение . Это белое твердое вещество. Хотя это не имеет особого значения, многие материалы оцениваются на основе содержания в них Li 2 O. Например, содержание Li 2 O в основном литиевом минерале сподумене (LiAlSi 2 O 6 ) составляет 8,03%.
Производство
Оксид лития получают термическим разложением пероксида лития при 300-400 ° C.
Оксид лития образуется вместе с небольшими количествами перекиси лития, когда металлический литий горит на воздухе и соединяется с кислородом:
- 4Li + O
2→ 2 ли
2O .
Чистый Ли
2Вывода может быть получен путем термического разложения из лития пероксида , Li
2О
2, при 450 ° C
- 2 Ли
2О
2→ 2 ли
2О + О
2
Состав
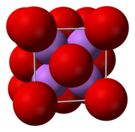
Твердый оксид лития имеет антифтористую структуру с четырехкоординированными центрами Li + и восьмикоординированными оксидами.
Газовая фаза основного состояния Li
2Молекула O линейна с длиной связи, соответствующей сильной ионной связи. Теория VSEPR предсказывает изогнутую форму, подобную H
2O .
Использует
Оксид лития используется в качестве флюса в керамической глазури; и создает синий цвет с медью и розовый с кобальтом . Оксид лития реагирует с водой и паром , образуя гидроксид лития, и его следует изолировать от них.
Его использование также исследуется для оценки неразрушающей эмиссионной спектроскопии и мониторинга деградации в системах термобарьерных покрытий . Его можно добавлять в качестве сопутствующей добавки с оксидом иттрия в верхнее покрытие из циркониевой керамики без значительного уменьшения ожидаемого срока службы покрытия. При высоких температурах оксид лития излучает хорошо различимую спектральную картину, интенсивность которой увеличивается по мере разрушения покрытия. Реализация позволит осуществлять мониторинг таких систем на месте, давая возможность эффективно прогнозировать срок службы до отказа или необходимого обслуживания.
Металлический литий можно получить из оксида лития электролизом, выделяя кислород в качестве побочного продукта.


