Боргидрид лития - Lithium borohydride

|
|
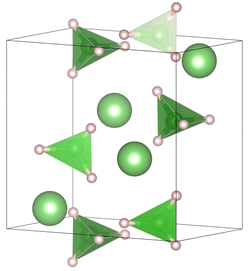 Элементарная ячейка борогидрида лития при комнатной температуре
|
|
| Имена | |
|---|---|
|
Название ИЮПАК
Тетрагидридоборат лития (1–)
|
|
| Другие имена
Гидроборат
лития , тетрагидроборат лития борат (1-), тетрагидро-, литий, боранат лития |
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.037.277 |
|
PubChem CID
|
|
| Номер RTECS | |
| UNII | |
|
Панель управления CompTox ( EPA )
|
|
|
|
|
|
| Характеристики | |
| LiBH 4 | |
| Молярная масса | 21,784 г / моль |
| Появление | Белое твердое вещество |
| Плотность | 0,666 г / см 3 |
| Температура плавления | 268 ° С (514 ° F, 541 К) |
| Точка кипения | 380 ° С (716 ° F, 653 К) разлагается |
| реагирует | |
| Растворимость в эфире | 2,5 г / 100 мл |
| Состав | |
| ромбический | |
| ПНМА | |
|
а = 7,17858 (4), b = 4,43686 (2), с = 6,80321 (4)
|
|
|
Объем решетки ( В )
|
216,685 (3) А 3 |
|
Формула единиц ( Z )
|
4 |
| [4] B | |
| Термохимия | |
|
Теплоемкость ( C )
|
82,6 Дж / моль К |
|
Стандартная мольная
энтропия ( S |
75,7 Дж / моль К |
|
Std энтальпия
формации (Δ F H ⦵ 298 ) |
-198,83 кДж / моль |
| Опасности | |
| > 180 ° С (356 ° F, 453 К) | |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
Боргидрид лития (LiBH 4 ) представляет собой боргидрид , и известен в органическом синтезе в качестве восстановителя для сложных эфиров . Хотя литиевая соль менее распространена, чем родственный борогидрид натрия , она обладает некоторыми преимуществами, так как является более сильным восстановителем и хорошо растворяется в простых эфирах, оставаясь при этом более безопасным в обращении, чем литийалюминийгидрид .
Подготовка
Боргидрид лития может быть получен реакцией метатезиса, которая происходит при шаровой мельнице более широко доступных боргидрида натрия и бромида лития :
- NaBH 4 + LiBr → NaBr + LiBH 4
В качестве альтернативы он может быть синтезирован путем обработки трифторида бора с гидрид лития в диэтиловом эфире :
- BF 3 + 4 LiH → LiBH 4 + 3 LiF
Реакции
Боргидрид лития является более сильным восстановителем, чем боргидрид натрия . В смесях метанола и диэтилового эфира борогидрид лития способен восстанавливать сложные эфиры до спиртов и первичные амиды до аминов . Напротив, эти субстраты не подвержены действию боргидрида натрия. Повышенная реакционная способность объясняется поляризацией карбонильного субстрата за счет комплексообразования с катионом лития.
Хемоселективность
Использование боргидрида лития особенно выгодно в некоторых препаратах из-за его более высокой хемоселективности по сравнению с другими популярными восстанавливающими агентами, такими как алюмогидрид лития . Например, в отличие от алюмогидрида лития, борогидрид лития восстанавливает сложные эфиры, нитрилы , лактоны , первичные амиды и эпоксиды , сохраняя при этом нитрогруппы , карбаминовые кислоты , алкилгалогениды и вторичные / третичные амиды.
Производство водорода
Боргидрид лития реагирует с водой с образованием водорода. Эта реакция может быть использована для получения водорода.
Хранилище энергии

Боргидрид лития известен как один из химических энергоносителей с самой высокой плотностью энергии . Хотя в настоящее время это не имеет практического значения, твердое вещество будет выделять 65 МДж / кг тепла при обработке кислородом воздуха. Поскольку он имеет плотность 0,67 г / см 3 , окисление жидкого борогидрида лития дает 43 МДж / л . Для сравнения: бензин дает 44 МДж / кг (или 35 МДж / л), а жидкий водород дает 120 МДж / кг (или 8,0 МДж / л). Высокая удельная плотность энергии боргидрида лития сделала его привлекательным кандидатом для использования в автомобильном и ракетном топливе, но, несмотря на исследования и пропаганду, он не получил широкого распространения. Как и все энергоносители на основе химического гидрида, боргидрид лития очень сложно перерабатывать (то есть перезаряжать) и, следовательно, страдает низкой эффективностью преобразования энергии . В то время как батареи, такие как ионно-литиевые, имеют плотность энергии до 0,72 МДж / кг и 2,0 МДж / л, их эффективность преобразования постоянного тока в постоянный может достигать 90%. Ввиду сложности механизмов рециркуляции гидридов металлов такая высокая эффективность преобразования энергии непрактична с существующей технологией.
| Вещество | Удельная энергия МДж / кг | Плотность г / см 3 | Плотность энергии МДж / л |
|---|---|---|---|
| LiBH 4 | 65,2 | 0,666 | 43,4 |
| Обычный бензин | 44 год | 0,72 | 34,8 |
| Жидкий водород | 120 | 0,0708 | 8 |
| литий-ионный аккумулятор | 0,72 | 2,8 | 2 |
Смотрите также
Примечания
- ^ Большее отношение плотности энергии к удельной энергии для водорода связано с очень низкой массовой плотностью (0,071 г / см 3 ).

