Гипофосфорная кислота - Hypophosphoric acid
|
|
| Имена | |
|---|---|
|
Название ИЮПАК
Гиподифосфорная кислота
|
|
| Другие названия
Дифосфорная кислота
|
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| ЧЭБИ | |
| ChemSpider | |
|
PubChem CID
|
|
| UNII | |
|
Панель управления CompTox ( EPA )
|
|
|
|
|
|
| Свойства | |
| H 4 P 2 O 6 | |
| Молярная масса | 161,98 г / моль |
| вид | Белое твердое вещество (дигидрат) |
| Температура плавления | 54 ° С (129 ° F, 327 К) |
| Основание конъюгата | Гипофосфат |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
| Ссылки на инфобоксы | |
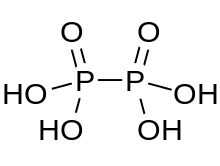
Гипофосфорная кислота - это минеральная кислота с формулой H 4 P 2 O 6 с фосфором в формальной степени окисления +4. В твердом состоянии он присутствует в виде дигидрата H 4 P 2 O 6 · 2H 2 O. В гипофосфорной кислоте атомы фосфора идентичны и соединены непосредственно связью P-P. Изогипофосфорная кислота представляет собой структурный изомер гипофосфорной кислоты, в котором один фосфор имеет водород, непосредственно связанный с ним, и этот атом фосфора связан с другим атомом через кислородный мостик с образованием смешанного ангидрида фосфористой кислоты и фосфорной кислоты . Два атома фосфора находятся в степенях окисления +3 и +5 соответственно.
Подготовка и реакции
Гипофосфорную кислоту можно получить реакцией красного фосфора с хлоритом натрия при комнатной температуре.
- 2 P + 2 NaClO 2 + 2 H 2 O → Na 2 H 2 P 2 O 6 + 2 HCl
Смесь гипофосфорной кислоты, фосфористой кислоты (H 3 PO 3 ) и фосфорной кислоты (H 3 PO 4 ) образуется, когда белый фосфор окисляется на воздухе при частичном погружении в воду.
Тетранатриевая соль Na 4 P 2 O 6 · 10H 2 O кристаллизуется при pH 10, а динатриевая соль Na 2 H 2 PO 6 · 6H 2 O при pH 5,2. Динатриевую соль можно пропустить через ионообменную колонку с образованием дигидрата кислоты H 4 P 2 O 6 · 2H 2 O.
Безводная кислота может быть образована вакуумной дегидратацией над P 4 O 10 или реакцией H 2 S на гипофосфате свинца, Pb 2 P 2 O 6 .
Гипофосфорная кислота является тетрапротонной с константами диссоциации p K a1 = 2,2, p K a2 = 2,8, p K a3 = 7,3 и p K a4 = 10,0.
При стоянии безводная кислота подвергается перегруппировке и диспропорционированию с образованием смеси изогипофосфорной кислоты, HPO (OH) -O-PO 2 (OH); пирофосфорная кислота H 2 P 2 O 7 и пирофосфорная кислота.
Гипофосфорная кислота нестабильна в горячей соляной кислоте , в 4 М HCl она гидролизуется с образованием H 3 PO 3 + H 3 PO 4 .
Структура
Гипофосфорная кислота содержит ионы оксония и лучше всего имеет формулу [H 3 O + ] 2 [H 2 P 2 O 6 ] 2– . Кислота изоструктурна диаммониевой соли, которая содержит анион [HOPO 2 PO 2 OH] 2- с длиной связи P-P 219 мкм.
НОРО 2 PO 2 ОН 2- анион в Na - H 2 P 2 O 6 · 6H 2 O имеет симметричный шахматном этан -подобной структуры с Р-Р связью длиной 219 мкм. Каждый атом фосфора имеет две связи P-O длиной 151 пм и длину связи P-OH 159 пм.
Гипофосфатные соли
Известно много гипофосфатных солей, например, K 4 P 2 O 6 · 8H 2 O, Ca 2 P 2 O 6 · 2H 2 O, K 3 HP 2 O 6 · 3H 2 O, K 2 H 2 P 2 O 6. · 2H 2 O, KH 3 P 2 O 6 .
При нахождении на воздухе гипофосфаты имеют тенденцию окисляться до пирофосфатов, содержащих P
2О4-
7ion, где P имеет формальную степень окисления +5. Гипофосфаты устойчивы к гидроксидам щелочных металлов. В конденсированном гидроксиде натрия они быстро превращаются в ортофосфат, содержащий ПО.3-
4.
Полигипофосфаты
Известны полигипофосфаты, содержащие линейные анионы, например Na 5 P 3 O 8, содержащий O (PO
2) 3 O 5− с цепочкой P − P − P и Na 6 P 4 O 10 · 2H 2 O, содержащим O (PO
2) 4 O 6− , с цепочкой P − P − P − P. Циклический анион (ПО
2)6-
6, (гипогексаметафосфат), где каждый атом фосфора имеет степень окисления +3, образуется, когда суспензия красного фосфора в КОН окисляется бромом.
Смотрите также
- Дитионовая кислота , эквивалент серы.
