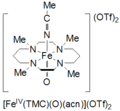Высоковалентное железо - High-valent iron
Высоковалентное железо обычно обозначает соединения и промежуточные продукты, в которых железо находится в формальной степени окисления > 3, которые показывают количество связей > 6 с координационным числом ≤ 6. Этот термин довольно необычен для гептакоординированных соединений железа. Его следует отличать от терминов гипервалентный и гиперкоординированный , поскольку соединения высоковалентного железа не обязательно нарушают правило 18-электронов и не обязательно показывают координационные числа> 6. Ион феррата (VI) [FeO 4 ] 2– был первой структурой. в этом классе синтезированы. Синтетические соединения, обсуждаемые ниже, в целом содержат сильно окисленное железо, поскольку эти концепции тесно связаны.
Соединения оксоирона
Оксоферрильные соединения обычно предлагаются в качестве промежуточных продуктов в каталитических циклах , особенно в биологических системах, в которых требуется активация O 2 . Двухатомный кислород имеет высокий потенциал восстановления (E 0 = 1,23 В), но первым шагом, необходимым для использования этого потенциала, является термодинамически невыгодное одноэлектронное восстановление E 0 = -0,16 В. Это восстановление происходит в природе путем образования супероксидного комплекса. в котором восстановленный металл окисляется O 2 . Продуктом этой реакции является более активный перекисный радикал. Обилие этих видов в природе и доступный им химический состав - вот причины, по которым изучение этих соединений так важно. Широко применяемым методом получения высоковалентных оксоферрильных частиц является окисление йодозобензолом :
- символическое окисление соединения железа с использованием йодозобензола ; L обозначает поддерживающий лиганд
Fe (IV) O
Сообщалось о нескольких формах синтеза оксо железа (IV). Эти соединения моделируют биологические комплексы, такие как цитохром P450 , NO-синтаза и изопенициллин-N-синтаза. Двумя такими сообщенными соединениями являются оксоирон с тиолатным лигированием (IV) и оксоирон с ацетатом циклама (IV). Оксоирон (IV), связанный с тиолятом, образуется в результате окисления предшественника, [Fe II (TMCS)] (PF 6 ) (TMCS = 1-меркаптоэтил-4,8,11-триметил-1,4,8,11- тетразациклотетрадекан) и 3-5 эквивалентов H 2 O 2 при -60 ° C в метаноле . Соединение железа (IV) темно-синего цвета и демонстрирует интенсивные абсорбционные характеристики при 460 нм, 570 нм, 850 нм и 1050 нм. Этот вид Fe IV (= O) (TMCS) + стабилен при -60 ˚C, но сообщается о разложении при повышении температуры. Соединение 2 было идентифицировано с помощью мессбауэровской спектроскопии , масс-спектрометрии с ионизацией электрораспылением высокого разрешения (ESI-MS), рентгеновской абсорбционной спектроскопии , расширенной тонкой структуры поглощения рентгеновских лучей (EXAFS), ультрафиолетовой и видимой спектроскопии (UV-vis), преобразования Фурье инфракрасную спектроскопию (FT-IR) и результаты сравнивали с расчетами по теории функционала плотности (DFT).
Тетраметилциклам оксоирон (IV) образуется по реакции Fe II (TMC) (OTf) 2 , TMC = 1,4,8,11-тетраметил-1,4,8,11-тетраазациклотетрадекан; OTf = CF 3 SO 3 , с йодозилбензолом (PhIO) в CH 3 CN при -40 ˚C. О втором способе образования оксоирона циклама (IV) сообщается как реакция Fe II (TMC) (OTf) 2 с 3 эквивалентами H 2 O 2 в течение 3 часов. Этот вид имеет бледно-зеленый цвет и имеет максимум поглощения при 820 нм. Сообщается, что он стабилен не менее 1 месяца при -40 ˚C. Он был охарактеризован мессбауэровской спектроскопией, ESI-MS, EXAFS, УФ- видимой , рамановской спектроскопией и FT-IR.
Комплексы биспидина с высоким валентным железом могут окислять циклогексан до циклогексанола и циклогексанона с выходом 35% при соотношении спирта к кетону до 4.
Fe (V) O
Fe V TAML (= O), TAML = тетраамидо -макроциклический лиганд , образуется в результате реакции [Fe III (TAML) (H 2 O)] (PPh 4 ) с 2-5 эквивалентами метахлорпербензойной кислоты при - 60 ˚C в н-бутиронитриле. Это темно-зеленое соединение (два λ max при 445 и 630 нм соответственно) стабильно при 77 К. Стабилизация Fe (V) объясняется сильной π-донорной способностью депротонированных амидных атомов азота.
Fe (VI) O
Феррат (VI) представляет собой неорганическое анион из химической формулы [FeO 4 ] 2- . Он светочувствителен и придает своим соединениям и растворам бледно-фиолетовый цвет. Это один из самых сильных известных окислителей, устойчивых к воде . Хотя он классифицируется как слабое основание , концентрированные растворы феррата (VI) стабильны только при высоком pH .
Электронная структура
Проведен обзор электронной структуры порфириновых соединений оксо железа.
Соединения нитридо-железа и имидо-железа
Соединения нитридо- железа и имидо- железа тесно связаны с химией диазот железа . Биологическое значение nitridoiron (V) порфирины было рассмотрено. Широко применимый метод получения форм высокомолекулярного нитридо железа - термическое или фотохимическое окислительное отщепление молекулярного азота от азидного комплекса.
- символическое окислительное удаление азота дает комплекс нитридо-железа; L обозначает поддерживающий лиганд.
Fe (IV) N
Существует несколько структурно охарактеризованных соединений нитридо-железа (IV).
Fe (V) N
Первое соединение нитридо-железа (V) было синтезировано и охарактеризовано Вагнером и Накамото (1988, 1989) с использованием фотолиза и рамановской спектроскопии при низких температурах.
Fe (VI) N
Сообщалось о второй разновидности Fe VI, помимо иона феррата (VI) , [(Me 3 cy-ac) FeN] (PF 6 ) 2 . Этот вид образуется в результате окисления с последующим фотолизом с образованием частиц Fe (VI). Характеристика комплекса Fe (VI) была проведена расчетами Мёссбауэра, EXAFS, ИК и DFT. В отличие от феррат-иона (VI) соединение 5 диамагнитно .
μ-нитридосоединения и окислительный катализ
Мостиковые μ-ди-nitrido железо фталоцианин соединения катализируют окисление метана до метанола , формальдегида и муравьиной кислоты с использованием перекиси водорода в качестве окислителя жертвенного.
Электронная структура
Виды нитридо железа (IV) и нитридо железа (V) были впервые теоретически исследованы в 2002 году.
Смотрите также
- Катализатор Якобсена (высоковалентный марганец)
использованная литература
дальнейшее чтение
- Solomon et al .; Angewandte Chemie International Edition, том 47, выпуск 47, страницы 9071–9074, 10 ноября 2008 г .; DOI : 10.1002 / anie.200803740