Гликозидная связь - Glycosidic bond
Гликозидная связь или гликозидная связь представляет собой тип ковалентной связи , который присоединяется к углеводу (сахар) молекулы к другой группе, которая может быть или не может быть другими углеводами.
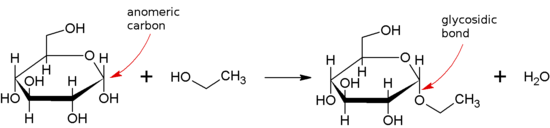
Гликозидная связь образуется между полуацетальной или гемикетальной группой сахарида (или молекулой, производной от сахарида) и гидроксильной группой некоторого соединения, такого как спирт . Вещество, содержащее гликозидную связь, представляет собой гликозид .
Термин «гликозид» теперь расширен, чтобы также охватывать соединения со связями, образованными между полуацетальными (или гемикетальными) группами сахаров и несколькими химическими группами, отличными от гидроксилов, такими как -SR (тиогликозиды), -SeR (селеногликозиды), -NR 1 R. 2 (N-гликозиды) или даже -CR 1 R 2 R 3 (C-гликозиды).
В частности, в встречающихся в природе гликозидах соединение ROH, из которого был удален углеводный остаток, часто называют агликоном, а сам углеводный остаток иногда называют «гликоном».
S-, N-, C- и O-гликозидные связи
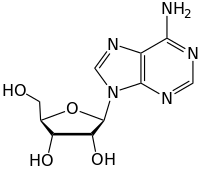
Гликозидные связи обсуждаемой выше формы известны как О-гликозидные связи по отношению к гликозидному кислороду, который связывает гликозид с агликоном или восстанавливающим концевым сахаром. По аналогии, можно также рассматривать S-гликозидные связи (которые образуют тиогликозиды ), где кислород гликозидной связи заменен атомом серы . Таким же образом в N-гликозидных связях кислород гликозидной связи заменяется азотом . Вещества, содержащие N-гликозидные связи, также известны как гликозиламины . С-гликозильные связи имеют гликозидный кислород, замещенный атомом углерода ; Термин «С-гликозид» IUPAC считает неправильным и не приветствуется. Все эти модифицированные гликозидные связи имеют разную восприимчивость к гидролизу, а в случае C-гликозильных структур они обычно более устойчивы к гидролизу.
Нумерация и различие α / β гликозидных связей
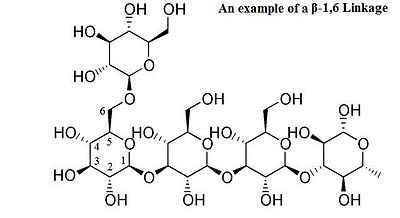
Когда аномерный центр участвует в гликозидной связи (что является обычным явлением в природе), тогда можно различать α- и β-гликозидные связи по относительной стереохимии аномерного положения и стереоцентра, наиболее удаленного от C1 в сахариде.
Фармакологи часто присоединяют вещества к глюкуроновой кислоте через гликозидные связи, чтобы повысить их растворимость в воде ; это известно как глюкуронизация . Многие другие гликозиды выполняют важные физиологические функции.
Химические подходы
Nüchter et al. (2001) продемонстрировали новый подход к гликозидации Фишера . Используя микроволновую печь, оборудованную дефлегматором, в роторном реакторе с бомбами высокого давления , Nüchter et al. (2001) смогли достичь 100% выхода α- и β-D-глюкозидов. Этот метод можно выполнять в многокилограммовой шкале.
- Метод Вишала Й Джоши
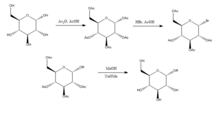
Джоши и др. (2006) предлагают метод Кенигса-Кнорра для стереоселективного синтеза алкил-D-глюкопиранозидов посредством гликозилирования, за исключением использования карбоната лития, который менее дорог и токсичен, чем традиционный метод с использованием солей серебра или ртути . D-глюкоза сначала защищается путем образования перацетата добавлением уксусного ангидрида в уксусной кислоте , а затем добавлением бромистого водорода, который бромируется в 5-положении. При добавлении спирта ROH и карбоната лития OR заменяет бром, и при снятии защиты с ацетилированных гидроксилов продукт синтезируется с относительно высокой чистотой. Было предложено Joshi et al. (2001), что литий действует как нуклеофил, который атакует углерод в 5-м положении, и в переходном состоянии спирт замещает группу брома. Преимущества этого метода, а также его стереоселективность и низкая стоимость литиевой соли включают то, что его можно проводить при комнатной температуре, а его выход относительно хорошо сравнивается с традиционным методом Кенигса-Кнорра.
Гликозид гидролазы
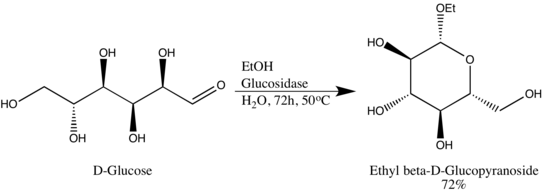
Гликозидгидролазы (или гликозидазы) - это ферменты , разрушающие гликозидные связи. Гликозидгидролазы обычно могут действовать либо на α-, либо на β-гликозидные связи, но не на оба. Эта специфичность позволяет исследователям получать гликозиды в высоком эпимерном избытке, одним из примеров является превращение Wen-Ya Lu D-глюкозы в этил-β-D-глюкопиранозид с использованием глюкозидазы природного происхождения. Стоит отметить, что Wen-Ya Lu использовала глюкозидазу обратным образом, противоположным биологической функциональности фермента:
Гликозилтрансферазы
Прежде чем моносахаридные единицы будут включены в гликопротеины, полисахариды или липиды в живых организмах, они обычно сначала «активируются» путем присоединения через гликозидную связь к фосфатной группе нуклеотида, такого как дифосфат уридина (UDP), дифосфат гуанозина (GDP) , тимидиндифосфат (TDP) или цитидинмонофосфат (CMP). Эти активированные биохимические промежуточные продукты известны как сахарные нуклеотиды или доноры сахара. Во многих биосинтетических путях используются моно- или олигосахариды, активируемые дифосфатной связью с липидами, такими как долихол . Эти активированные доноры затем являются субстратами для ферментов, известных как гликозилтрансферазы , которые переносят сахарную единицу от активированного донора к принимающему нуклеофилу (акцепторный субстрат).
Дисахарид фосфорилазы
В последние десятилетия были разработаны различные биокаталитические подходы к синтезу гликозидов, которые с использованием «гликозилтрансфераз» и «гликозидгидролаз» являются одними из наиболее распространенных катализаторов. Для первого часто требуются дорогие материалы, а для второго часто наблюдается низкая урожайность, De Winter et al. исследовали использование целлобиозофосфорилазы (ЦП) для синтеза альфа-гликозидов в ионных жидкостях. Было обнаружено, что наилучшие условия для использования CP были в присутствии IL AMMOENG 101 и этилацетата.
Направленное гликозилирование
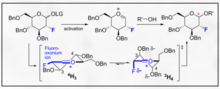
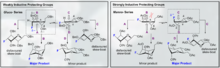
Существует множество химических подходов, способствующих селективности α- и β-гликозидных связей. Высокосубстратно-специфический характер селективности и общей активности пиранозида может создавать серьезные трудности при синтезе. Общая специфичность гликозилирования может быть улучшена путем использования подходов, которые принимают во внимание относительные переходные состояния, в которых аномерный углерод может претерпевать во время типичного гликозилирования. В частности, признание и включение моделей Фелкина-Ан-Эйзенштейна в обоснование химического дизайна в целом может обеспечить надежные результаты при условии, что преобразование может подвергаться такому типу конформационного контроля в переходном состоянии.
Фтор-направленное гликозилирование является обнадеживающим средством как для селективности B, так и для введения неприродной биомиметической C2-функциональности в углевод. Один новаторский пример, представленный Bucher et al. обеспечивает способ использования иона фтора оксония и трихлорацетимидата для усиления стереоселективности B за счет гош-эффекта. Эта разумная стереоселективность очевидна при визуализации моделей Фелкина-Ана возможных форм стульев.
Этот метод представляет собой обнадеживающий способ селективного включения B-этила, изопропила и других гликозидов с типичным химическим составом трихлорацетимидата.
О-связанные гликопептиды; фармацевтическое применение O-гликозилированных пептидов
Недавно было показано, что О-связанные гликопептиды демонстрируют превосходную проницаемость для ЦНС и эффективность на множестве животных моделей с болезненными состояниями. Кроме того, одним из наиболее интригующих аспектов этого является способность O-гликозилирования увеличивать период полужизни, уменьшать клиренс и улучшать PK / PD своего активного пептида за пределами увеличения проникновения в ЦНС. Врожденное использование сахаров в качестве солюбилизирующих фрагментов в метаболизме в фазах II и III (глюкуроновые кислоты) значительно дало эволюционное преимущество, заключающееся в том, что ферменты млекопитающих не эволюционируют напрямую для разложения О-гликозилированных продуктов на более крупные фрагменты.
Своеобразная природа О-связанных гликопептидов состоит в том, что существует множество примеров, которые проникают в ЦНС. Считается, что фундаментальная основа этого эффекта связана с «прыжками через мембрану» или «диффузией хмеля». Считается, что процесс «диффузии хмеля», вызванный неброуновским движением, происходит из-за разрыва плазматической мембраны. «Диффузия хмеля» заметно сочетает в себе свободную диффузию и межсравнительные переходы. Недавние примеры, в частности, включают высокую проницаемость аналогов мет-энкефалина среди других пептидов. Полный агонист mOR пентапептид DAMGO также проникает в ЦНС при гликозилировании.
использованная литература
- Марко Брито-Ариас, «Синтез и характеристика гликозидов», второе издание, редакция Springer, 2016 г.
внешние ссылки
- Определение гликозидов из Компендиума химической терминологии ИЮПАК , « Золотая книга »
- Варки А. и соавт. Основы гликобиологии. Лабораторный пресс Колд-Спринг-Харбор; 1999. Доступен для поиска в Интернете.