Положительный аллостерический модулятор рецептора ГАМК А -GABAA receptor positive allosteric modulator
В фармакологии , ГАМК рецепторов положительные аллостерические модуляторы являются положительными аллостерическая модулятор (РАМ) молекулы , которые увеличивают активность ГАМК А рецептора белка в позвоночных центральной нервной системы .
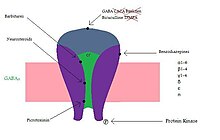
ГАМК является основным тормозным нейромедиатором в центральной нервной системе. После связывания он запускает рецептор ГАМК A, чтобы открыть свой хлоридный канал, чтобы позволить ионам хлора проникать в нейрон , делая клетку гиперполяризованной и менее склонной к срабатыванию . ГАМК A PAM усиливают эффект ГАМК, заставляя канал открываться чаще или на более длительные периоды. Однако они не действуют, если нет ГАМК или другого агониста .
В отличие от агонистов рецептора ГАМК А , ГАМК А PAM не связываются в том же самом активном центре, что и молекула нейромедиатора γ-аминомасляной кислоты (ГАМК) : они влияют на рецептор, связываясь в другом сайте белка. Это называется аллостерической модуляцией .
В психофармакологии ПАМ-рецепторы ГАМК- А, используемые в качестве лекарственных средств, обладают в основном седативным и анксиолитическим действием. Примеры ГАМК A PAM включают алкоголь ( этанол ), бензодиазепины, такие как диазепам (валиум) и алпразолам (ксанакс) , Z-препараты, такие как золпидем (амбиен), и препараты барбитуратов .
История
Рецепторы ГАМК А исторически были целью исследований по лечению лекарств. Самыми ранними соединениями были ионы, такие как бромид .
Барбитураты
В 1903 году первое психоактивное производное барбитуровой кислоты было синтезировано и продано для лечения головных болей. В течение 30 лет было разработано множество других барбитуратов, которые нашли применение в качестве седативных , снотворных и общих анестетиков . Хотя барбитураты перестали пользоваться популярностью, они продолжают служить анестетиками короткого действия и противоэпилептическими препаратами.
Бензодиазепины
Бензодиазепины были открыты в 1955 году и в значительной степени заменили барбитураты из-за их более высокого терапевтического индекса . Сначала бензодиазепины считались безопасными и эффективными второстепенными транквилизаторами, но затем подверглись критике за их эффекты, вызывающие зависимость . Некоторые эффективные бензодиазепины позволяют выбрать лекарственную форму , продолжительность действия, метаболическое взаимодействие и безопасность.
Бензодиазепины действуют путем связывания с бензодиазепиновым участком на большинстве, но не на всех рецепторах ГАМК А. Модуляция ГАМК А агонистами бензодиазепиновых сайтов является самоограничивающейся. Проводимость канала не выше в присутствии бензодиазепина и ГАМК, чем проводимость в присутствии только высоких концентраций ГАМК. Кроме того, в отсутствие ГАМК присутствие только бензодиазепинов не открывает хлоридный канал.
Некоторые метаболиты прогестерона и дезоксикортикостерона являются мощными и селективно-положительными аллостерическими модуляторами рецептора γ-аминомасляной кислоты типа A (ГАМК A ). Ганс Селье продемонстрировал в 1940 году, что некоторые стероиды прегнана могут вызывать как анестезию, так и седативный эффект, но 40 лет спустя появился молекулярный механизм, объясняющий их депрессивный эффект. В препарате среза головного мозга крысы синтетический стероидный анестетик альфаксалон (5α-прегнан-3α-ол-11,20 дион) усиливал как вызванное стимулом ингибирование, так и эффекты экзогенно применяемого мусцимола, который является селективным агонистом ГАМК А.
Рецептор
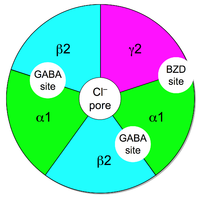
Рецепторы ГАМК А состоят из субъединиц, которые образуют рецепторный комплекс. У человека 19 рецепторных субъединиц, которые подразделяются на α (1–6), β (1–3), γ (1–3), δ, ε, π, θ и ρ (1–3). Функция рецептора различается в зависимости от того, как устроен пентамерный комплекс. Наиболее распространенным комплексом, который включает около 40% рецепторов ГАМК A, является комбинация α1β2γ2. Экспрессия субъединиц может сильно отличаться в зависимости от области мозга. Комбинация субъединиц влияет на то, как действует рецептор. Например, если субъединицы α1 и β2 экспрессируются вместе, они имеют высокую чувствительность к ГАМК, но низкую проводимость канала . Но если γ2 выражается с помощью α1 и β2, чувствительность низкая, а проводимость канала высокая. Субъединица γ2 должна присутствовать для связывания бензодиазепина с высоким сродством. Мало что известно о том, где в головном мозге расположены различные комплексы, что затрудняет открытие лекарств. Например, сайт связывания нейростероидов в рецепторе ГАМК A неизвестен, и барбитураты связываются с бета-субъединицей, которая отличается от сайта связывания бензодиазепина.
Доступные агенты
- Хлоралгидрат (и родственные пролекарства трихлорэтанола )
- Барбитураты
- Бензодиазепины
- Небензодиазепины (например, залеплон , золпидем , зопиклон )
- Ингаляционные анестетики (например, диэтиловый эфир , галотан , изофлуран )
- Этомидат
- Пропофол
- Нейростероиды (например, брексанолон , альфаксалон (ветеринарный))
Приложения
Барбитураты
Точные места действия барбитуратов еще не определены. Второй и третий трансмембранные домены субъединицы β, по-видимому, являются критическими; Связывание может включать карман, образованный метионином 286 β-субъединицы, а также метионином 236 α-субъединицы.
Бессонница
Барбитураты были введены как снотворные для больных шизофренией . Это вызвало состояние глубокого и продолжительного сна. Но это использовалось недолго из-за побочных эффектов.
Противосудорожное средство
Фенобарбитал был первым по-настоящему эффективным лекарством от эпилепсии. Он был обнаружен случайно, когда давали пациентам с эпилепсией, чтобы помочь им уснуть. Положительными побочными эффектами были противосудорожные свойства, которые снижали количество и интенсивность приступов.
Седация
Пентобарбитал используется как снотворное, когда обезболивание не требуется. Его часто используют при компьютерной томографии, когда необходима седация. Это эффективно, безопасно и быстро восстанавливается. В 2013 году барбитураты, фенобарбитал и бутабарбитал по-прежнему используются в некоторых случаях в качестве седативных средств, а также для противодействия таким лекарствам, как эфедрин и теофиллин . Фенобарбитал применяется при синдромах отмены лекарств. Он используется как обычное и неотложное лечение в некоторых случаях эпилепсии.

Бензодиазепин
Синаптическое действие бензодиазепинов: рецепторы ГАМК А, расположенные в синапсах, активируются при воздействии на них высокой концентрации ГАМК. Бензодиазепины усиливают сродство рецептора к ГАМК, увеличивая затухание спонтанных миниатюрных тормозных постсинаптических токов (mIPSC).
Анальгезия
Седативное действие бензодиазепинов ограничивает их полезность в качестве анальгетиков , и поэтому они, как правило, не считаются подходящими. Это ограничение можно обойти путем интратекального введения. Рецепторы ГАМК А в периакведуктальном сером цвете про-ноцицептивны в надспинальных участках, в то время как ГАМК А , обнаруженные в спинном мозге, обладают антигипералгезирующим действием. Спинальные α2- и α3- рецепторы, содержащие рецепторы GABA A , ответственны за антигипералгезическое действие интратекального диазепама . Это было показано, когда антигипералгезическое действие снижалось при введении α2 и α3 мышам при воспалительной боли и при невропатической боли. Кроме того, исследования на мышах α5 показали, что спинномозговой α5-содержащий рецептор GABA A играет незначительную роль в воспалительной боли. Селективный положительный аллостерический агонист α2, α3 и / или α5, такой как, например, L-838,417 , может быть использован в качестве обезболивающего лекарственного средства против воспалительной или невропатической боли. Дальнейшие исследования на моделях нейропатической боли на животных показали, что стабилизация котранспотера 2 хлорида калия ( KCC2 ) на мембранах нейронов может не только усилить анальгезию, индуцированную L-838,417, но и спасти его анальгетический потенциал при высоких дозах, раскрывая новую стратегию обезболивания в патологическая боль, путем сочетании нацеливание соответствующих ГАМК а рецепторов подтипов (то есть α 2 , α 3 ) и восстановление Cl - гомеостаза.
Шизофрения
Бензодиазепины используются в качестве поддерживающего лечения пациентов с шизофренией .
Депрессия
Была предложена ГАМК-эргическая гипотеза депрессии. Эта гипотеза ставит систему ГАМК в центральной роли в патофизиологии от депрессии и в дополнение к этому клинические исследования показали , что алпразолам и adinazolam антидепрессивные деятельности у пациентов с большим депрессивным расстройством. К сожалению, мы не знаем, какой подтип рецептора отвечает за антидепрессивную активность. Исследования на мышах с нокаутом y2 показали, что они демонстрируют повышенную тревожность и симптомы депрессии в тестах, основанных на отчаянии. У мышей также была повышенная концентрация кортикостерона, что является симптомом большой депрессии у людей. Субъединица y2 связана с субъединицами α1-α6, которые все являются известными субъединицами α, поэтому эти исследования не показывают, какая из субъединиц α связана с депрессивно-подобными симптомами. Другие исследования с мышами с нокаутом α2 показали усиление тревожных и депрессивных симптомов в тестах на кормление, основанных на конфликте, и тот факт, что тревога и депрессия часто связаны, по-видимому, указывает на то, что субъединица α2 может быть действительной мишенью для антидепрессанта ГАМК А.
Инсульт
Доклинические исследования показали, что бензодиазепины могут быть эффективными в снижении эффекта инсульта в течение до трех дней после приема препарата.
Нейростероиды
Нейростероиды могут действовать как аллостерические модуляторы рецепторов нейромедиаторов, таких как рецепторы GABA A , NMDA и сигма . Нейростероид прогестерон (PROG), который активирует рецепторы прогестерона, экспрессируемые в периферических и центральных глиальных клетках. Кроме того, было высказано предположение, что прегнановые стероиды, восстановленные с 3α-гидроксильным кольцом A, аллопрегнанолон и тетрагидродезоксикортикостерон, увеличивают GABA- опосредованные хлоридные токи, в то время как сульфат прегненолона и дегидроэпиандростерон (DHEA), с другой стороны, проявляют антагонистические свойства в отношении рецепторов GABA A.
Синтез
Барбитуровая кислота
Барбитуровая кислота является исходным соединением барбитуратов, хотя сама барбитуровая кислота не является фармакологически активной. Барбитураты были синтезированы в 1864 году Адольфом фон Байером путем объединения мочевины и малоновой кислоты (рис. 5). Процесс синтеза был позже разработан и усовершенствован французским химиком Эдуардом Гримо в 1879 году, что сделало возможным последующее широкое развитие производных барбитуратов. Позднее малоновая кислота была заменена диэтилмалонатом , поскольку использование сложного эфира позволяет избежать необходимости иметь дело с кислотностью карбоновой кислоты и ее нереакционноспособного карбоксилата (см. Рисунок 6). Барбитуровая кислота может образовывать большое количество препаратов барбитуратов с помощью реакции конденсации Кневенагеля .
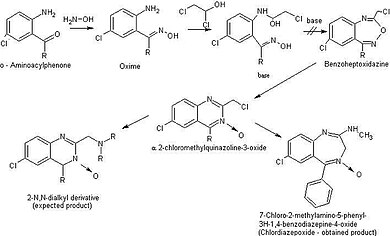
Бензодиазепины
Структура, на которой основан первый бензодиазепин, была открыта Лео Х. Штернбахом . Он думал, что соединение имеет структуру гептоксдиазина (рис. 7), но позже было установлено, что это хиназолин-3-оксид. Затем из этого соединения синтезировали возможные лекарственные препараты-кандидаты и проверили активность. Одним из этих соединений был активный хлордиазепоксид . Он появился на рынке в 1960 году и стал первым бензодиазепиновым препаратом.
Биосинтез нейростероидов
Нейростероиды синтезируются в центральной нервной системе (ЦНС) и периферической нервной системе (ПНС) из холестерина и предшественников стероидов, которые импортируются из периферических источников. Эти источники включают производные 3β-гидрокси-Δ5, такие как прегненолон (PREG) и дегидроэпиандростерон (DHEA), их сульфаты и восстановленные метаболиты, такие как тетрагидропроизводное прогестерона 3α-гидрокси-5α-прегнан-20-он (3α, 5α -THPROG). В результате местного синтеза или метаболизма гонадных стероидов надпочечниками многие нейростероиды накапливаются в головном мозге.
Взаимосвязь структура-деятельность
Барбитураты

Барбитураты имеют специальное применение и делятся на 4 класса: ультракороткого, короткого, среднего и длительного действия. Эмпирически SAR барбитуратов основаны на тысячах испытанных (на животных) соединений. Они показали, что R и R´ не могут быть H в позиции 5 (см. Рисунок 8). Также позиция 5 наделяет седативно-снотворными свойствами. Обычно алкильное разветвление в положении 5 означает меньшую растворимость липидов и меньшую активность. Ненасыщенность проявляет меньшую активность в положении 5, а алициклические и ароматические кольца проявляют меньшую активность. Полярные заместители (-NH 2 , -OH, -COOH) уменьшают растворимость липидов, но также устраняют активность. R´´ в положении 1 обычно представляет собой H, но CH 3 в этом положении дает меньшую растворимость липидов и меньшую продолжительность. Замена S на атом O в положении 2 дает тиобарбитураты, которые более растворимы в липидах, чем оксибарбитураты. В целом, чем более жирорастворимый барбитурат, тем быстрее он начинает действовать, тем короче его продолжительность и тем выше степень снотворного действия. Барбитураты показали некоторые гидролитические проблемы в отношении приготовления жидких лекарственных форм. Трудность заключается в катализируемой -ОН деградации уреидных колец, но это можно исправить, если в рецептуре pH равен 6. S (-) форма барбитурата проявляет большую депрессивную активность, в то время как R (+) изомеры обладают возбуждающим действием.
Бензодиазепины
Согласно исследованию, проведенному Maddalena et al. С использованием искусственных нейронных сетей , позиция 7 оказывает наибольшее влияние на сродство к рецепторам . Когда активная группа в положении 7 становится более липофильной и увеличивается электронный заряд, увеличивается сродство к рецептору. В том же исследовании было обнаружено, что позиция 2´ является второй по важности в влиянии на аффинность, но группа в этой позиции должна быть электрофильной, чтобы иметь эффект. Позиции 3, 6 'и 8 менее важны. Изменения на 6, 8, 9 или 4 уменьшают активность. Если группа в положении 1 изменяется на N-алкил, галогеналкил, алкинил и малый цикл или аминоалкил, активность увеличивается. Гидроксилирование в положении 3 может вызывать быстрое конъюгацию и уменьшать продолжительность и эффективность, что может быть клинически полезным.
Нейростероиды
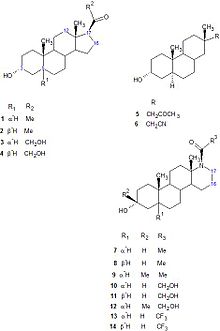
В середине 1980-х годов нейроактивные стероиды 3 & alpha;, 5 & alpha; tetrahydroprogesterone или аллопрегнанолон (3 & alpha;, 5α-ТНР) и 3 & alpha;, 5α- тетрагидродеоксикортикостерон (3α, 5α-THDOC) было показано , что модулируют возбудимость нейронов через их взаимодействие с ГАМК А рецепторов. Стероиды 3α, 5α-THP и 3α, 5α-THDOC были способны усиливать GABA-индуцированный ток Cl - . Кроме того, эти стероиды могут усиливать связывание мусцимола и бензодиазепинов с рецепторами ГАМК А. Исследования структурной активности (SAR) показали, что 3альфа-ОН группа важна для анестезирующего действия этих стероидов, они также имеют оптимально расположенную группу, принимающую водородную связь, на β-грани стероида в положении C-17. Четыре стероидных кольца образуют жесткую основу для размещения этих водородных групп в трехмерном пространстве. Аналоги 5 и 6 (фиг. 10) являются слабыми модуляторами функции рецептора ГАМК А, поскольку гибкие боковые цепи в этих аналогах не имеют конформации, необходимых для высокой биологической активности.
Смотрите также
использованная литература
дальнейшее чтение
- Файзи М., Дабириан С., Таджали Х., Ахмади Ф., Заварех Э.Р., Шаххоссейни С., Табатабай С.А. (февраль 2015 г.). «Новые агонисты бензодиазепиновых рецепторов: дизайн, синтез, анализ связывания и фармакологическая оценка производных 1,2,4-триазоло [1,5-a] пиримидинона и 3-амино-1,2,4-триазола». Биоорганическая и медицинская химия . 23 (3): 480–7. DOI : 10.1016 / j.bmc.2014.12.016 . PMID 25564376 .