Переносчик дофамина - Dopamine transporter
Переносчик дофамина (также допамин активного переносчик , DAT , SLC6A3 ) представляет собой трансмембранный белок , который перекачивает нейромедиатор дофамин из синаптической щели сзади в цитозол . В цитозоле другие переносчики секвестрируют дофамин в пузырьки для хранения и последующего высвобождения. Обратный захват дофамина через DAT обеспечивает первичный механизм, посредством которого дофамин выводится из синапсов , хотя может быть исключение в префронтальной коре, где данные указывают на возможно большую роль переносчика норадреналина .
DAT участвует в ряде заболеваний, связанных с допамином, включая синдром дефицита внимания с гиперактивностью , биполярное расстройство , клиническую депрессию , алкоголизм и расстройство, связанное с употреблением психоактивных веществ . Ген , который кодирует белок DAT расположен на человеческой хромосоме 5, состоит из 15 кодирующих экзонов , и примерно 64 т.п.н. долго. Доказательства связи между DAT и расстройствами, связанными с дофамином, получены из типа генетического полиморфизма , известного как VNTR , в гене DAT ( DAT1 ), который влияет на количество экспрессируемого белка.
Функция
DAT - это интегральный мембранный белок, который удаляет дофамин из синаптической щели и откладывает его в окружающие клетки, тем самым прерывая сигнал нейромедиатора. Дофамин лежит в основе нескольких аспектов познания, включая вознаграждение, а DAT способствует регулированию этого сигнала.
Механизм
DAT - симпортер, который перемещает дофамин через клеточную мембрану, связывая это движение с энергетически выгодным движением ионов натрия, перемещающихся от высокой к низкой концентрации в клетке. Функция DAT требует последовательного связывания и совместного транспорта двух ионов Na + и одного иона Cl - с дофаминовым субстратом. Движущей силой DAT-опосредованного обратного захвата дофамина является градиент концентрации ионов, создаваемый Na + / K + АТФазой плазматической мембраны .
В наиболее широко распространенной моделью для моноаминов переносчика функции, ионы натрия должен связываться с внеклеточным доменом переносчика дофамина , прежде чем может связываться. Как только дофамин связывается, белок претерпевает конформационное изменение, которое позволяет как натрию, так и дофамину расщепляться на внутриклеточной стороне мембраны.
Исследования с использованием электрофизиологии и радиоактивно меченного дофамина подтвердили, что переносчик дофамина подобен другим переносчикам моноаминов в том, что одна молекула нейромедиатора может переноситься через мембрану с одним или двумя ионами натрия. Ионы хлора также необходимы для предотвращения накопления положительного заряда. Эти исследования также показали, что скорость и направление переноса полностью зависят от градиента натрия.
Из-за тесной связи мембранного потенциала и градиента натрия, вызванные активностью изменения полярности мембраны могут резко повлиять на скорость переноса. Кроме того, переносчик может способствовать высвобождению дофамина при деполяризации нейрона.
Соединение DAT – Ca v
Предварительные данные свидетельствуют о том, что переносчик дофамина соединяется с потенциалозависимыми кальциевыми каналами L-типа (особенно Ca v 1,2 и Ca v 1,3 ), которые экспрессируются практически во всех дофаминовых нейронах. В результате связывания DAT – Ca v субстраты DAT, которые продуцируют деполяризующие токи через транспортер, способны открывать кальциевые каналы, которые связаны с транспортером, что приводит к притоку кальция в дофаминовые нейроны. Этот приток кальция , как полагают, индуцирует CaMKII опосредованного фосфорилирования переносчика дофамина как ниже по течению эффекта; поскольку фосфорилирование DAT с помощью CAMKII приводит к оттоку дофамина in vivo , активация связанных с транспортером кальциевых каналов является потенциальным механизмом, с помощью которого определенные лекарства (например, амфетамин) запускают высвобождение нейротрансмиттера.
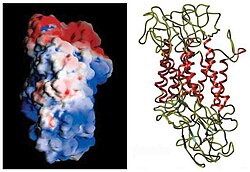
Белковая структура
Первоначальное определение топологии мембраны DAT было основано на анализе гидрофобных последовательностей и сходстве последовательностей с транспортером ГАМК. Эти методы предсказали двенадцать трансмембранных доменов (TMD) с большой внеклеточной петлей между третьим и четвертым TMD. Дальнейшая характеристика этого белка использовала протеазы , которые расщепляют белки на более мелкие фрагменты, и гликозилирование, которое происходит только на внеклеточных петлях, и в значительной степени подтвердило первоначальные предсказания топологии мембраны. Точная структура дофаминового транспортера Drosophila melanogaster (dDAT) была выяснена в 2013 году с помощью рентгеновской кристаллографии .
Расположение и распространение
|
Фармакодинамика амфетамина в дофаминовом нейроне
|
Региональное распределение DAT было обнаружено в областях мозга с установленной дофаминергической схемой, включая нигростриатальный , мезолимбический и мезокортикальный пути. Эти ядра , которые составляют эти пути имеют различные паттерны экспрессии. Паттерны экспрессии генов у взрослых мышей демонстрируют высокую экспрессию в компактной части черной субстанции .
Было обнаружено, что DAT в мезокортикальном пути , меченный радиоактивными антителами, обогащен дендритами и клеточными телами нейронов компактной части черной субстанции и вентральной тегментальной области . Эта закономерность имеет смысл для белка, регулирующего уровень дофамина в синапсе.
Окрашивание полосатого тела и прилежащего ядра мезолимбического пути было плотным и неоднородным. В полосатом теле DAT локализуется в плазматической мембране окончаний аксонов. Двойная иммуноцитохимия продемонстрировала совместную локализацию DAT с двумя другими маркерами нигростриатных окончаний, тирозингидроксилазой и рецепторами допамина D2 . Таким образом, было продемонстрировано, что последний является ауторецептором клеток, выделяющих дофамин. TAAR1 представляет собой пресинаптический внутриклеточный рецептор, который также колокализуется с DAT и при активации оказывает эффект, противоположный ауторецептору D2; т.е. он интернализует переносчики дофамина и индуцирует отток за счет обратной функции переносчика посредством передачи сигналов PKA и PKC .
Удивительно, но DAT не был идентифицирован ни в одной синаптической активной зоне. Эти результаты предполагают, что обратный захват дофамина полосатым телом может происходить вне синаптических специализаций, когда дофамин диффундирует из синаптической щели.
В черной субстанции DAT локализован на аксональной и дендритной (т.е. пре- и постсинаптической) плазматической мембране .
В perikarya из Парс компактов нейронов, ДАТЫ была локализованы в основном для грубой и гладкой эндоплазматической сети, комплекс Гольджи и мультивезикулярных органов, выявление вероятных участков синтеза, модификации, транспорт и деградации.
Генетика и регуляция
Ген для DAT, известный как DAT1 , расположен на хромосоме 5p15. Кодирующая белок область гена имеет длину более 64 т.п.н. и включает 15 кодирующих сегментов или экзонов . Этот ген имеет тандемный повтор с переменным числом (VNTR) на 3'-конце ( rs28363170 ) и еще один в области 8-го интрона . Было показано, что различия в VNTR влияют на базальный уровень экспрессии переносчика; следовательно, исследователи искали ассоциации с расстройствами, связанными с дофамином.
Nurr1 , ядерный рецептор, который регулирует многие гены, связанные с дофамином, может связываться с промоторной областью этого гена и вызывать экспрессию. Этот промотор также может быть мишенью фактора транскрипции Sp-1 .
В то время как факторы транскрипции контролируют, какие клетки экспрессируют DAT, функциональная регуляция этого белка в значительной степени осуществляется киназами . MAPK , CAMKII , PKA и PKC могут модулировать скорость, с которой переносчик перемещает дофамин, или вызывать интернализацию DAT. Совместно локализованный TAAR1 является важным регулятором переносчика дофамина, который при активации фосфорилирует DAT посредством передачи сигналов протеинкиназы A (PKA) и протеинкиназы C (PKC). Фосфорилирование любой протеинкиназой может привести к интернализации DAT ( неконкурентное ингибирование обратного захвата), но одно фосфорилирование, опосредованное PKC, вызывает функцию обратного переносчика ( отток дофамина ). Ауторецепторы дофамина также регулируют DAT, прямо противодействуя эффекту активации TAAR1.
Переносчик дофамина человека (hDAT) содержит внеклеточный сайт связывания цинка с высоким сродством, который при связывании цинка ингибирует обратный захват дофамина и усиливает индуцированный амфетамином отток дофамина in vitro . Напротив, переносчик серотонина человека (hSERT) и переносчик норэпинефрина человека (hNET) не содержат сайтов связывания цинка. Добавка цинка может снизить минимальную эффективную дозу амфетамина, когда он используется для лечения синдрома дефицита внимания и гиперактивности .
Биологическая роль и нарушения
Скорость, с которой DAT удаляет дофамин из синапса, может иметь огромное влияние на количество дофамина в клетке. Об этом лучше всего свидетельствуют тяжелые когнитивные нарушения, двигательные нарушения и гиперактивность мышей без переносчиков дофамина. Эти характеристики имеют поразительное сходство с симптомами СДВГ .
Различия в функциональном VNTR были определены как факторы риска биполярного расстройства и СДВГ. Данные выяснилось , что позволяет предположить , что также является объединение с более сильным снятие симптомов от алкоголизма , хотя это вызывает споры. Аллель гена DAT с нормальным уровнем белка связано с не-курения поведения и легкость отказа от курения. Кроме того, подростки мужского пола, особенно из семей с высоким риском (в тех семьях, где мать не вовлечена в процесс и отсутствует материнская привязанность), которые несут 10-аллельный повтор VNTR, демонстрируют статистически значимое сродство с антисоциальными сверстниками.
Повышенная активность DAT связана с несколькими различными расстройствами, включая клиническую депрессию .
Было показано, что мутации в DAT вызывают синдром дефицита переносчика дофамина , аутосомно-рецессивное двигательное расстройство, характеризующееся прогрессирующим ухудшением дистонии и паркинсонизма .
Фармакология
Переносчик дофамина является мишенью для субстратов , высвобождающих дофамин , ингибиторов транспорта и аллостерических модуляторов .
Кокаин блокирует DAT, связываясь непосредственно с транспортером и снижая скорость транспорта. Напротив, амфетамин попадает в пресинаптический нейрон непосредственно через нейрональную мембрану или через DAT, конкурируя за обратный захват с дофамином. Попав внутрь, он связывается с TAAR1 или входит в синаптические пузырьки через VMAT2 . Когда амфетамин связывается с TAAR1, он снижает скорость возбуждения постсинаптического нейрона и запускает передачу сигналов протеинкиназы A и протеинкиназы C , что приводит к фосфорилированию DAT. Затем фосфорилированный DAT либо действует в обратном направлении, либо уходит в пресинаптический нейрон и прекращает транспорт. Когда амфетамин попадает в синаптические пузырьки через VMAT2, дофамин высвобождается в цитозоль. Амфетамин также вызывает отток дофамина посредством второго TAAR1-независимого механизма, включающего CAMKIIα-опосредованное фосфорилирование переносчика, которое предположительно возникает в результате активации DAT-связанных кальциевых каналов L-типа амфетамином.
Считается, что дофаминергические механизмы каждого препарата лежат в основе приятных ощущений, вызываемых этими веществами.
Взаимодействия
Было показано, что переносчик дофамина взаимодействует с:
- Альфа-синуклеин ,
- PICK1 и
- TGFB1I1 .
Помимо этих врожденных белок-белковых взаимодействий, недавние исследования продемонстрировали, что вирусные белки, такие как белок Tat ВИЧ-1, взаимодействуют с DAT, и это связывание может изменять гомеостаз дофамина у ВИЧ-положительных людей, что является фактором, способствующим развитию нейрокогнитивных расстройств, связанных с ВИЧ. .
Смотрите также
использованная литература
внешние ссылки
- Ассоциации, связанные с переносчиками дофамина, эксперименты, публикации и клинические испытания
- Dopamine + Transporter в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH)
- Обзор всей структурной информации, доступной в PDB для UniProt : Q7K4Y6 ( Натрийзависимый переносчик дофамина Drosophila melanogaster) в PDBe-KB .